
- •1. Определение понятия фермент. Ферменты - это белки (установлено в 1922г), которые действуют как катализаторы в биологических системах.
- •2. Химическую природу, физико-химические свойства и биологическая роль ферментов.
- •3. Особенности ферментативного катализа. Сравнение каталитического действия ферментов и неорганических катализаторов
- •4.Строение простых, сложных ферментов: активный и аллостерический центры. Определение понятий: холофермент, апофермент, кофермент, кофактор, субстрат, метаболит, продукт.
- •5. Изоферменты. Строение, биологическую роль, диагностическое значение определения. Изоферменты лактатдегидрогеназы (лдг), креатинкиназы (кк)
- •6. Локализация и компартментализация ферментов в клетке и тканях: ферменты общего назначения, органоспецифические и органеллоспецифические (маркерные) ферменты.
- •7. Механизм и стадии ферментативного катализа: теории Фишера, Кошланда, переходных состояний.
- •9..Ингибирование активности ферментов, виды ингибирования: обратимое, необратимое, конкурентное, неконкурентное, определение вида ингибирования с использованием Км.
- •10. Механизмы специфической регуляции активности ферментов: аллостерический, ковалентная модификация, на генетическом уровне (индукция, репрессия)
- •1). Аллостерическая регуляция каталитической активности ферментов
- •III. Механизмы регуляции количества ферментов
- •Вторичные посредники (мессенджеры)
- •12.Классификацию и номенклатуру ферментов: систематические и рабочие названия. Коферментный состав ферментов различных классов
- •1. Оксидоредуктазы
- •2. Трансферазы
- •4. Лиазы
- •5. Изомеразы
- •6. Лигазы (синтетазы)
- •13.Энзимопатии: понятие, классификация, молекулярные причины возникновения и механизмы развития, последствия, биохимическая диагностика.
- •I. Энзимопатология
- •1. Наследственные энзимопатии
- •Наследственные энзимопатии по типу нарушений метаболизма делят на:
- •2. Приобретенные энзимопатии
- •14.Принципы, направления и объекты энзимодиагностики: а) энзимологическое определение количества метаболитов, б) определение активности ферментов. Причины и механизмы развития ферментемий.
- •1) Определение активности органо-, органеллоспецифических ферментов и их изоферментов.
- •2) Определение активности ферментов и их констант (Km, t, pH).
- •3) Определение концентрации органических веществ с помощью ферментов.
- •15. Основные принципы и методы энзимотерапии. Биохимические основы энзимотерапии: особенности применения, пути введения.
- •16. Биологическое окисление (бо) совокупность окислительно-восстановительных реакций, которые протекают во всех живых клетках.
- •17. Оксидазный путь потребления кислорода протекает в митохондриях, потребляет 90% о2 и обеспечивает процесс окислительного фосфорилирования.
- •18. Этапы унифицирования энергии пищевых веществ и образования субстратов тканевого дыхания
- •19. Митохондрии - органеллы клеток. Они имеют 2 мембраны наружную гладкую и внутреннюю с многочисленными складками – кристами, внутреннее пространство митохондрий заполнено матриксом.
- •20. Цикл Кребса
- •21. Состав, локализацию, последовательность расположения дыхательных комплексов в электронтранспортной цепи (этц). Хемиосмотическую теорию Митчелла
- •Хемиосмотическая теория Митчелла
- •22. Механизмы сопряжения и разобщения окисления и фосфорилирования. Коэффициент р/0. Понятие - дыхательный контроль. Эндогенные и экзогенные разобщители.
- •Дыхательный контроль
- •Коэффициент окислительного фосфорилирования
- •Диоксигеназные реакции
- •Использование активных форм кислорода в организме
- •Повреждающее действие активных форм кислорода в организме
- •25. Биохимические механизмы ферментативной и неферментативной антиоксидантной защиты (аоз), возрастные особенности. Природные и синтетические прооксиданты и антиоксиданты, понятия.
- •1. Ферментативная антиоксидантная защита
- •2. Неферментативная антиоксидантная защита
16. Биологическое окисление (бо) совокупность окислительно-восстановительных реакций, которые протекают во всех живых клетках.
Субстрат БО – вещество, способное отдавать электрон. (Любые вещества, способные вступать в реакции окисления).
Биохимик В.И. Палладин создал теорию дыхания, как совокупности ферментативных процессов. Он предположил, что окисление субстратов может происходить в 2 фазы:
1). Анаэробная фаза. В этой фазе особые вещества хромогены (R) отщепляют Н от субстратов и восстанавливаются (RH2).
2). Аэробная фаза. Восстановленные хромогены RH2 передают Н на О2.
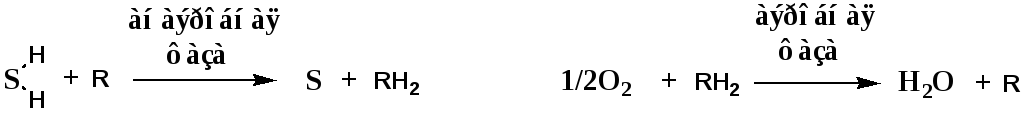
Субстрат БО - в-во, способное отдавать электроны (в-ва, способные вступать в реакции окисления).
Пути использования кислорода в клетке
В настоящее время выделено 4 основные пути использования кислорода в организме:
1. Оксидазный путь - окислительное фосфорилирование. Протекает в митохондриях, является основным источником АТФ в аэробных тканях. Потребляет 90% кислорода.
2. Монооксигеназный путь. Обеспечивает включение 1 атома кислорода в молекулу субстрата. Используется для синтеза новых веществ (стероидные гормоны), обезвреживания ксенобиотиков и токсических продуктов обмена в митохондриях и ЭПР.
3. Диоксигеназный путь. Обеспечивает включение молекулы кислорода в молекулу субстрата. Используется для деградации АК и синтеза новых веществ.
4. Пероксидазный и радикальный пути. Кислород участвует в образовании перекисей и активных радикалов, которые необходимы в пероксисомах для внутриклеточного пищеварения, разрушения макрофагами бактерий, вирусов, регуляции метаболизма и т.д. Перекиси и активные кислородные радикалы оказывают также повреждающее воздействие на структуры клеток и тканей, активируя ПОЛ. Разрушение перекисей и инактивация свободных радикалов осуществляется с помощью ферментативной и неферментативной антиокидантной системы.
17. Оксидазный путь потребления кислорода протекает в митохондриях, потребляет 90% о2 и обеспечивает процесс окислительного фосфорилирования.
Окислительным фосфорилированием называют синтез АТФ из АДФ и Н3РО4 за счет энергии движении электронов по дыхательной цепи.
Окислительное фосфорилирование является основным источником АТФ в аэробных клетках.
МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ
Окислительное фосфорилирование состоит из процессов окисления и фосфорилирования, которые между собой сопряжены.
Процесс окисления происходит при движении электронов по дыхательной цепи от субстратов тканевого дыхания на кислород. Дыхательная цепь окислительного фосфорилирования состоит из 4 белковых комплексов, встроенных во внутреннюю мембрану митохондрий и небольших подвижных молекул убихинона и цитохрома С, которые циркулируют в липидном слое мембраны между белковыми комплексами.
Комплекс I – НАДН2 дегидрогеназный комплекс
Комплекс II – СДГ.
Комплекс III – Комплекс b
Комплекс IV – Цитохромоксидазный комплекс
Коэнзим Q (убихинон
Компоненты дыхательной цепи располагаются в мембране в порядке повышения их редокс-потенциала. При переходе е- от комплекса с низким редокс-потенциалом к комплексу с более высоким редокс-потенциалом происходит выделение свободной энергии. При окислении 1 НАДН2 выделяется 220 кДж/моль свободной энергии.
I, III и IV комплексы дыхательной цепи используют 65-70% этой свободной энергии для переноса Н+ из матрикса митохондрий в межмембранное пространство, 30-35% свободной энергии рассеивается в виде тепла.
