
Сосудистая хирургия часть 1
.pdfГлава 32. Артериальная эмболия конечностей и техника эмболэктомии |
395 |
|
|
Первая фаза. Фаза ишемии или деваскуляризации характеризуется четырьмя классическими симптомами: мучительная боль, резко выраженная ишемия тканей, ригидность конечности и массивный отек. Кроме выраженности боли самым значимым из этих симптомов является ригидность конечности. Этот знак, который я считаю самым важным сигналом тревоги, всегда появляется многими часами раньше других клинических и лабораторных признаков, и заставляет думать о природе лежащего в основе патологического процесса. Через 10–12 ч от начала эпизода острой артериальной окклюзии у пациента появляется олигурия, азотэмия и миоглобинурия вместе с метаболическим ацидозом различной степени выраженности.
Во время фазы реваскуляризации клиническая картина и метаболические нарушения, даже если они не были заметны в острую фазу, проявляются особенно тяжело. Вскоре после восстановления кровотока появляются гигантские пузыри, наполненные жидкостью, массивный отек конечности, отмечается потепление кожи, но вместе с тем возникает гангрена дистальных отделов конечности и некроз икроножных мышц. Часто, даже после успешной эмболэктомии, сохраняется отек мышц. Нарастающая фасциальная компрессия икроножных мышц может обернуться развитием гангрены, поэтому в таких случаях обязательно выполнение одной или нескольких фасциотомий для ослабления давления и уменьшения отека мышц. Это может стать операцией, спасающей конечность.
Во время реперфузии ишемизированных мышц исследование метаболизма показало снижение pH крови, низкое напряжение кислорода венозной крови (Po2) и закономерно высокое напряжение углекислого газа венозной крови (Pco2), а также повышение уровня сывороточного калия и концентрации креатинфосфокиназы, и изменение уровней других ферментов, имеющих отношение к поперечно-полосатым мышцам, таких как лактатдегидрогеназа и сывороточная глутаматоксалоацететдегидрогеназа.
Для отражения хронологической последовательности патологических событий мной был предложен термин «мионефропатический метаболический синдром» [11–13, 49] (см. гл. 40).
Успех лечения этих метаболических осложнений существенным образом зависит от того, как быстро они диагностируются. Необходимо восстановить электролитный баланс, особенно снизить уровень сывороточного калия до нормальных значений, если необходимо, то даже проведением гемодиализа. Введение содового раствора для купирования ацидоза должно выполняться без отлагательств. Такое лечение еще более настоятельно рекомендуется проводить, если есть или подозревается миоглобинурия, так как в кислой среде миоглобин легче и быстрее осаждается в почечных канальцах. Использование бикарбоната необходимо для предотвращения почечных осложнений. При развитии почечной недостаточности следует проводить гемодиализ до тех пор, пока не восстановится функция почек. При наличии мышечного отека необходимо выполнять фасциотомию, как упоминалось выше. Уровень сывороточной креатинфосфокиназы коррелирует со степенью некроза мышц. Для предотвращения дальнейшего высвобождения этого метаболита обычно сразу же назначается маннитол и трометамин. Ампутация необходима в случае массивной гангрены конечности, но также может быть показана только при наличии ишемического поражения мышц без гангрены, в качестве профилактической меры, для устранения источника метаболических нарушений, каким являются некротизированные скелетные мышцы.
Литература
1.Mosny E, Dumont J. Embolie femorale au cours d'un restrecissement mitral pur. Arteriotomie. Guerison. Bull Acad Med (Paris) 1911; 66: 358.
2.Key E. Embolectomy in the treatment of circulatory disturbances in the extremities. Surg Gynecol Obstet 1923; 36: 309.
3.Key E. Embolectomy of the vessels of the extremities. Br J Surg 1936; 24: 350.
4.Haimovici H. Les embolies arterielles des membres. Paris: Masson et Cie, 1937.
5.Lerman J, Miller FR, Lund Cc. Arterial embolism and embolectomy. JAMA 1930; 94: 1128.
6.Crawford ES, DeBakey ME. The retrograde flush procedure in embolectomy and thrombectomy. Surgery 1956; 40: 737.
7.Kartchner MM. Retrograde arterial embolectomy for limb salvage. Arch Surg 1972; 104: 532.
8.Murray DWG, Best CH. The use of heparin in thrombosis. Ann Surg 1938; 108: 163.
9.Murray DWG. Heparin in thrombosis and embolism. Br J Surg 1940; 27: 567.
10.Fogarty TJ, Cranley JJ, et al. A method for extraction of arterial emboli and thrombi. Surg Gynecol Obstet 1963; 116: 241.
11.Haimovici H. Arterial embolism with acute massive ischemic myopathy and myoglobinuria: evaluation of a hitherto unreported syndrome with report of two cases. Surgery 1960; 47: 739.
12.Haimovici H. Arterial embolism, myoglobinuria and renal tubular necrosis. Arch Surg 1970; 100: 639.
13.Haimovici H. Muscular, renal and metabolic complications of acute arterial occlusions: myonephropathicmetabolic syndrome. Surgery 1979; 85: 461.
14.Freund D, Romanoff H, Floman Y. Mortality rate following lower limb arterial embolectomy: causative factors. Surgery 1975;
77:201.
15.Green RM, DeWeese JA, Rob CG. Arterial embolectomy before and after the Fogarty catheter. Surgery 1975; 77: 24.
16.Haimovici H, Moss CM, Veith FJ. Arterial embolectomy revisited [editorial]. Surgery 1975; 78: 209.
17.Blaisdell FW, Steele M, Allen RE. Management of acute lower extremity arterial ischemia due to embolism and thrombosis. Surgery 1978; 84: 822.
18.Warren R, Linton RR. The treatment of arterial embolism N Engl J Med 1948; 238: 421.
19.Haimovici H. Peripheral arterial embolism. A study of 320 unselected cases of embolism of the extremities. Angiology 1950;
1:20.
20.Darling RC, Austen WG, Linton RR. Arterial embolism. Surg Gynecol Obstet 1967; 124: 106.
21.Haimovici H. Arterial embolism: peripheral and visceral. In: Haimovici H, ed. The surgical management of vascular diseases. Philadelphia: JB Lippincott, 1970: 71.
22.Daley R, Mattingly TW, et al. Systemic arterial embolism in rheumatic heart disease. Am Heart J 1951; 42: 566.
23.Hara M, Williams GO. Multiple arterial emboli. Surgery 1966;
60:804.
24.Gore I, Collins DP. Spontaneous atheromatous embolization: review of the literature and a report of 16 additional cases. Am J Clin Pathol 1960; 32: 415.
25.Wagner RB, Martin AS. Peripheral atheroembolism: confirmation of a clinical concept, with a case report and review of the literature. Surgery 1973; 73: 353.

396 Раздел V. Окклюзионные заболевания артерий
26.Kwaan JHM, Conolly JE. Peripheral atheroembolism. Arch Surg 1977; 112: 987.
27.Kempczinski RF. Lower extremity arterial emboli from ulcerating atherosclerotic plaques. JAMA 1979; 241: 807.
28.Haimovici H. Atheroembolism. In: Haimovici H, ed. Vascular emergencies. New York: Appleton-CenturyCrofts, 1982: 205.
29.Turnipseed WD, et al. J Vasc Surg 1986; 3: 437.
30.Haimovici H. Late arterial embolectomy. Surgery 1959; 46: 775.
31.Amer NC, Schaefer HC, et al. Aortic dissection presenting as iliac arterial occlusion: aid to early diagnosis. N Engl J Med 1962;
266:1040.
32.Eriksson I, Holmberg JT. Analysis of factors affecting limb salvage and mortality after embolectomy. Acta Chir Scand 1977;
143:237.
33.Baird RJ, Lajos TZ. Emboli to the arm. Ann Surg 1964; 160: 905.
34.Champion HR, Gill W. Arterial embolus to the upper limb. Br J Surg 1973; 60: 505.
35.MacGowan WAL, Mooneeram R. A review of 174 patients with arterial embolism. Br J Surg 1973; 60: 11.
36.Raithel D. Surgical treatment of acute embolization and acute arterial thrombosis: a review of 342 cases. J Cardiovasc Surg 1973: 61.
37.Sachatello CR, Ernst CB, Griffen WOo The acutely ischemic upper extremity: selective management. Surgery 1974; 76: 1002.
38.Savelyev VS, Zatevakhin II, Stepanov NY. Artery embolism of the upper limbs. Surgery 1977; 81: 367.
39.Haimovici H. Cardiogenic embolism of the upper extremity. J Cardiovasc Surg 1982; 23: 3.
40.Ammann J, Seiler H, Vogt B. Delayed arterial embolectomy: a plea for a more active surgical approach. Br J Surg 1976; 63: 73.
41.Robbs JV, Baker LW. Late revascularization ofthe lower limb following acute arterial occlusion. Br J Surg 1979; 66: 129.
42.Jarrert F, Dacumos GC, et al. Late appearance of arterial emboli: diagnosis and management. Surgery 1979; 86: 898.
43.Jackson BB. Venous aspiration as an adjunct in the management of late arterial embolectomy. Surgery 1965; 57: 358.
44.Blaisdell FW, Lim RD Jr, et al. Pulmonary microembolism: a cause of morbidity and death after major vascular surgery. Arch Surg 1966; 93: 776.
45.Foster JH, Carter JW, et al. Arterial injuries secondary to the use ofthe Fogarty catheter. Ann Surg 1970; 171: 971.
46.Rob C, Battle S. Arteriovenous fistula after Fogarty catheterthrombectomy. Arch Surg 1972; 105: 90.
47.Dainko EA. Complications of the use of the Fogarty balloon catheter. Arch Surg 1972; 105: 79.
48.Byrnes G, MacGowan WAL. The injury potential of Fogarty balloon catheters. J Cardiovasc Surg (Torino) 1975; 16: 590.
49.Haimovici H. Metabolic syndrome secondary to acute arterial occlusions. In: Haimovici H, ed. Vascular emergencies. New York: Appleton-Century-Crofts, 1982: 267.

Глава 33
Тромбоэмболэктомия под контролем рентгеноскопии
Эван К. Липситц, Франк Дж. Вайт и Такао Ооки
Историческая справка
К настоящему моменту накоплен уже почти вековой опыт по выполнению артериальной эмболэктомии. Первую успешную эмболэктомию из бедренных артерий выполнили в 1911 г. Kee из Стокгольма и Labey из Парижа [1]. Достижения в некоторых областях медицины способствовали более успешному лечению сосудистой патологии и особенно усовершенствовали выполнение тромбэктомии. Среди этих достижений — использование антикоагулянтов, в частности гепарина, введение в клиническую практику антитромбоцитарных веществ, усовершенствование хирургического инструментария и техники наложения швов, а также анестезиологического пособия и реанимационной помощи пациентам с сосудистыми заболеваниями.
Тромбоэмболии и связанные с их возникновением состояния характеризуются высокой заболеваемостью и смертностью. Уровни операционной смертности при лечении острой артериальной тромбоэмболии колеблются от 10% до 50% [2–6]. Расходы на лечение пациентов с этими состояниями, включая длительную госпитализацию, реабилитацию с учетом потенциальной потери конечности, могут быть весьма существенными. По ряду причин за последние несколько десятилетий лечение острой ишемии конечности, возникшей вследствие тромбоэмболии, стало более комплексным. Самым важным является то, что существенно снизилась доля молодых пациентов с ревматическим поражением клапанов сердца и/или фибрилляцией желудочков. У этой группы пациентов имеются относительно интактные артерии с сохраненной пульсацией, за исключением пораженной конечности. Диагностика и лечение тромбоэмболических состояний у таких пациентов значительно менее сложны, чем у пожилых пациентов с генерализованным атеросклерозом. Эмболы у них обычно мягкие и не фик-
сируются к артериальной стенке, что дает возможность легко их удалить. Отмечается значительное увеличение доли пожилых пациентов с выраженным атеросклерозом. Эти пациенты имеют отягощенный коморбидный фон, что существенно осложняет как выполнение операции, так и периоперативное лечение артериальной тромбоэмболии. И наконец, имеется большое число пациентов с протезированными мелкими и крупными сосудами. Лечение тромбоза или окклюзии протеза, возникающих при недостаточном притоке крови, плохих путях оттока или из-за самого протеза, становится обычным делом, и в нем все чаще возникает необходимость по мере установки протезов в сомнительных участках.
Fogarty и соавторы впервые применили баллонный катетер для эмболэктомии в 1963 г. [7]. Применение этого катетера позволило извлекать тромбы из удаленных областей через одну или несколько маленьких артериотомий, что предпочтительнее прямого выделения заинтересованной артерии. За последние 20 лет появление тромболитиков открыло новые возможности лечения окклюзий артерий и протезов без механической тромбэктомии. Также созданы новые технологии тромбэктомии и, хотя они применяются все шире, им не удалось вытеснить баллонный катетер. Ни хирургическая техника тромбоэмболэктомии, ни конструкция катетера значительно не изменились за последние 40 лет его применения. Тем не менее использование интраоперационного рентгенологического контроля во многих случаях существенно улучшило результаты лечения. Интраоперационная рентгеноскопия позволяет выполнить более контролируемую тромбэктомию и помогает определить необходимость дополнительных процедур, таких как ангиопластика со стентированием или шунтирование. Они могут быть выполнены во время тромбоэмболэктомии, что делает лечение более эффективным, полным и простым.
398 Раздел V. Окклюзионные заболевания артерий
Тромбоэмболэктомия под контролем рентгеноскопии
Существует множество причин, почему стандартная тромбэктомия не является оптимальной:
1)не всегда возможно пройти баллонным катетером через извилистые, пораженные артерии;
2)иногда сложно оценить адекватность выполненной тромбэктомии;
3)из-за комплексной природы этого процесса изменения, лежащие в основе тромбоза, могут быть не замечены. В такой ситуации существует большая вероятность развития повторного эпизода тромбоза in situ, особенно если повреждение произошло при самой тромбэктомии;
4)форсированная тракция или перераздувание балонного катетера может привести к повреждению как нормальных, так и измененных артериальных сосудов;
5)без рентгеноскопического визуального контроля проникновение катетера субинтимально, диссекция интимы или отрыв крупной бляшки могут остаться недиагностированными;
6)и наконец, тромбэктомия может быть связана с такими поздними осложнениями, как аневризма или артериовенозная фистула, когда возникшие во время выполнения процедуры повреждения остаются незамеченными и не лечатся [8].
Ввыполнении тромбоэмболэктомии под контролем рентгеноскопии есть ряд соответствующих преимуществ. Во-первых, значительно снижается вероятность образования больших интимальных диссекций или разрыва бляшки в просвете сосуда. Это объясняется тем, что, если и возникают такие проблемы, они обычно сразу определяются при рентгеноскопическом контроле, что ограничивает степень повреждения. Более того, если возникает вызывающая опасения диссекция, всегда есть возможность выполнить баллонную ангиопластику и стентирование. Хотя маленькие баллонные катетеры имеют эластичный кончик для предупреждения повреждения интимы, этот механизм ненадежен, особенно если сосуды небольшого диаметра и поражены. Во-вторых, если баллон частично раздуть контрастом и направить катетер к месту окклюзии, то по растяжению или суже-
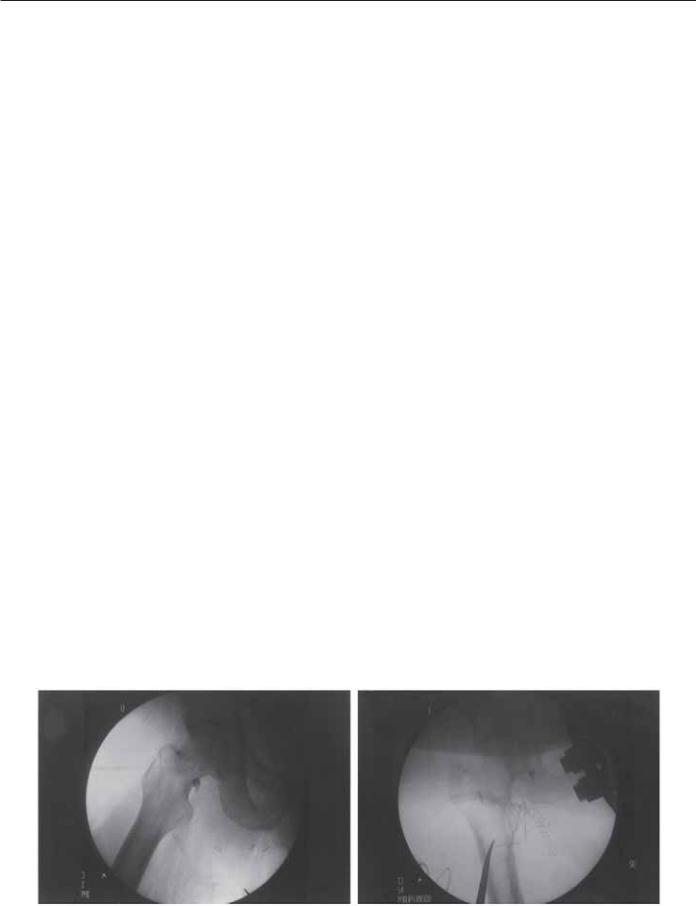
нию баллона можно определить области поражения в просвете сосуда (рис. 33.1А и Б). Если есть какое-то препятствие продвижению катетера в ретроградном направлении, что подтверждается сгибанием катетера при флюороскопии, катетер может быть извлечен, кончик выпрямлен и предпринята следующая попытка проведения катетера. Тромбоэмболэктомия под контролем рентгеноскопии также позволяет идентифицировать и локализовать как сопутствующее атеросклеротическое поражение, так и организованный старый тромб. Так как наполненный контрастом баллон проходит внутри артерии, он деформируется в соответствии с формой подлежащей поверхности. Эти поражения сразу отображаются при ангиографии, а затем могут быть немедленно коррегированы или баллонной ангиопластикой с возможной установкой внутрисосудистого стента, или выполнением повторной тромбоэмболэктомии (рис. 33.2А–Г). Если необходимо, может быть выполнена операция по шунтированию сосудов, намеченных при интраоперационной ангиографии. Тромбоэмболэктомия под контролем рентгеноскопии может также оказать существенную помощь в определении характера поражения. При атеросклеротических поражениях деформация баллона приобретает острые формы. Хронический тромб вызывает более мягкую деформацию баллона, который приобретает более округлые очертания. Свежий тромб вообще не вызывает деформацию баллонного катетера. Это, конечно, только приблизительно оценивает причину, лежащую в основе поражения. Возможно, самое значимое преимущество тромбоэмболэктомии под контролем рентгеноскопии состоит в том, что она позволяет оперирующему хирургу напрямую видеть и контролировать степень раздувания баллона, существенно снижая риск повреждения стенки артерии (рис. 33.3). Такая визуализация дополняет мануальное ощущение сопротивления баллона катетера при его соприкосновении с интимой сосуда. Если визуализация отсутствует, и хирург полагается только на собственное ощущение при вытягивании катетера, то еще до появления этого ощущения может возникнуть значительное перерастяжение артериальной стенки, что Parsons с соавторами и продемонстрировали в своем исследовании [9]. При выполнении тромбоэмболэктомии под контролем рентгеноскопии также можно оценить размер сосуда, используя маркированные катетеры или проводники, а также баллон для ангиопластики.
A |
|
Б |
|
|
|
Рис. 33.1. (А) Коническая деформация баллона, наполненного контрастом, в области избыточной гиперплазии интимы. (Б) Сужение баллона, наполненного контрастом, в менее пораженном сегменте.
Глава 33. Тромбоэмболэктомия под контролем рентгеноскопии |
399 |
|
|
A |
|
Б |
|
|
|
В |
|
Г |
|
|
|
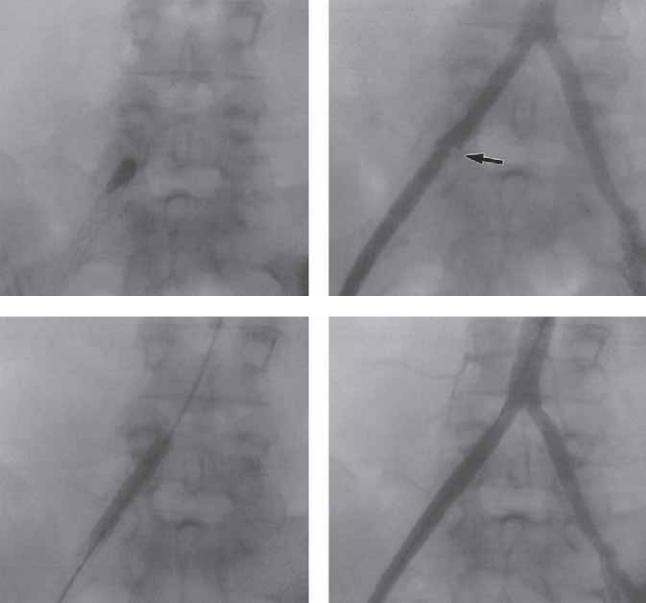
Рис. 33.2. Тромбоэмболэктомия под контролем рентгеноскопии при тромбозе подвздошных артерий, возникшем спустя 1 неделю после ангиопластики и стентирования. (А) Деформация баллона, наполненного контрастом, в проксимальном участке стента. (Б) Ретроградная артериограмма демонстрирует явную флотацию интимы сразу проксимальнее стента в подвздошной артерии (указано стрелкой). (В) Второй стент прижимает флотирующую интиму к стенке сосуда. (Г) Контрольная артериограмма демонстрирует исправленный дефект и хороший кровоток по артерии.
При необходимости шунтирования, при рентгеноскопическом контроле также можно определить уровень наложения проксимального анастомоза. Кроме того, контрольная цифровая ангиография в операционной позволяет оценить полноту тромбэктомии. Без рентгеноскопии об эффективности тромбэктомии можно судить по субъективной оценке фрагментов тромбоэмбола, антеградного и ретроградного кровотока. Плавно суживающийся к концу тромб обычно свидетельствует о полной тромбэктомии, в то время как неровный и оторванный — о неполной тромбэктомии. Однако это не всегда так в случаях с пораженными артериями. Заключительная ангиография также позволяет оценить дистальное русло и определить проходимость артерий и шунтов.
Техника
ПОДГОТОВКА ОПЕРАЦИОННОЙ
Успешное выполнение тромбоэмболэктомии под рентгеноскопическим контролем зависит от наличия соответствующего оборудования в операционной. Так как сосудистые хирурги используют эндоваскулярные методы и все чаще включают их в хирургическую практику, многие центры уже оборудованы для выполнения тромбоэмболэктомии под рентгеноскопическим контролем. На самом деле, в сравнении со многими эндоваскулярными процедурами, такими как эндоваскулярное лечение аневризм брюшной аорты и чрескожная транслюминальная ангиопластика с или без стентирования, оборудование, требующееся для тромбоэмболэктомии
400 |
Раздел V. Окклюзионные заболевания артерий |
|
|
|
|
|
|
|
|
|
|
|
|
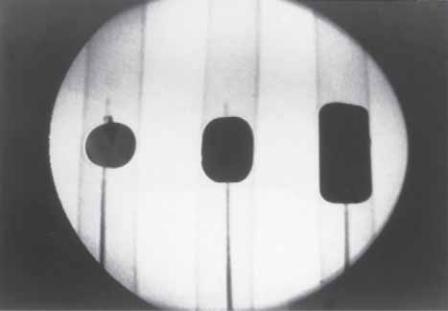
Рис. 33.3. Различные формы баллона, на- |
|
|
|
|
полненного контрастом, в системе in vitro, |
|
|
|
|
при рентгеноскопии. (А) При минимальном |
|
|
|
|
раздутии баллон принимает округлую фор- |
|
|
|
|
му и неплотно примыкает к стенкам сосуда. |
|
A |
Б |
B |
(Б) При дальнейшем раздутии баллон при- |
|
|
|
|
нимает овальную форму, превращается в до- |
|
|
|
|
статочно жесткую структуру, плотно приле- |
|
|
|
|
гающую к стенкам сосуда. (В) После |
|
|
|
|
перераздутия баллон принимает практиче- |
|
|
|
|
ски прямоугольную форму и оказывает зна- |
|
|
|
|
чительное радиально-ориентированное да- |
|
|
|
|
вление на стенки сосуда. |
под рентгеноскопическим контролем, относительно простое. Тем не менее необходимо иметь в распоряжении полный набор интродьюсеров, катетеров, проводников, баллонных катетеров и стентов, так как операция может стать многокомпонентной.
Очевидно, что наличие в операционной высококачественного цифрового флюороскопа является обязательным. Это обрудование должно иметь функцию запоминания последнего кадра, возможность повтора снятого изображения, вычитания и функцию роадмэппинга, а также быть доступным в любое время. Хирург должен легко владеть техникой работы с флюороскопом и не зависеть в этом от специалистов-радиологов. Такое требование является очень важным, так как большое количество подобных ситуаций случается ночью и в выходные, когда штатного персонала может и не быть. Также очень желателен рентген-прозрачный операционный стол, которым хирург может управлять, используя ножную педаль или ручное управление. Плавающий стол может упростить позиционирование под флюороскопом, но все же он несколько громоздкий по ширине, а из-за его ограниченной возможности регулироваться по высоте и углу наклона может потребоваться более сложная открытая операция.
Артериальная тромбоэмболэктомия
После выполнения продольной артериотомии подбирается подходящий по размеру баллонный катетер и продвигается в проксимальном направлении с целью обеспечить приток крови. Если катетер проходит без сопротивления, под флюороскопическим контролем баллон раздувается раствором, содержащим четверть или половину контрастного вещества (рис. 33.4). Это позволяет визуализировать баллон по всему ходу. Если ощущается сопротивление или катетер не проводится, то для прохождения через препятствие можно использовать проводник или направляющий катетер с ангиографическим и рентгеноскопическим контролем. После преодоления препятствия можно завести по проводнику баллонный катетер для последующей эмболэктомии (рис. 33.5). Или же интродьюсер может быть проведен по проводнику и помещен за областью обструкции. Затем буж интродьюсера удаляется, а однопросветный катетер для люминальной баллонной эм-
болэктомии, примыкающий по всей длине к проводнику, помещается в интродьюсер (рис. 33.6А–В). Раздутый контрастом баллон и интродьюсер извлекаются под рентгеноскопическим контролем.
По мере того как баллон раздут, его осторожно вытягивают, контролируя ощущение трения баллона и оценивая рентген-изо- бражение. Неровности контура баллона отображаются на экране. После того как достигается оптимальное удаление тромбов, выполняется контрольная ангиография и коррегируются любые оставшиеся гемодинамически значимые поражения.
После того как восстановлен приток крови, катетер (обычно меньшего размера) заводится в дистальном направлении и выполняется нужное количество аналогичных действий под рентгеноскопическим контролем, который оказывает даже большую помощь в предупреждении перерастяжения баллона и повреждения сосуда в отношении меньших по диаметру, более дистально расположенных сосудов.
Вэкспериментальном исследовании на собаках Parsons и соавторы [9] обнаружили, что без использования рентгеноскопического контроля на всех этапах эксперимента отмечалось значительное перерастяжение сосудов. Чем меньше по диаметру сосуд, тем
вбольшем проценте случаев он перерастягивается (23% — в подвздошных артериях и 40% — в поверхностных бедренных артериях). Случалось, что катетер был ошибочно заведен в ветви аорты, и создавалась опасная ситуация, о чем хирург даже не подозревал. Наконец, было замечено, что при извлечении баллона из аорты через меньшие по диаметру подвздошные артерии возникала значительная деформация баллона, указывающая на то, что на стенки сосуда прилагается значительная радиальная сила.
Внекоторых случаях в просвете артерии отмечается плотно фиксированный пролонгированный тромб. Это особенно характерно для крупных сосудов, таких как подвздошные артерии. В подобных случаях баллонный катетер может не справиться с удалением тромба, что делает обычную тромбэктомию малоэффективной [10]. В таких ситуациях может возникнуть необходимость
виспользовании специального катетера для удаления фиксированных тромбов (Baxter Vascular Systems, Irvine, CA) [11]. Это устройство имеет регулируемый, упругий, покрытый латексом, спиральный кончик на дистальном конце, который управляется
Глава 33. Тромбоэмболэктомия под контролем рентгеноскопии |
401 |
|
|
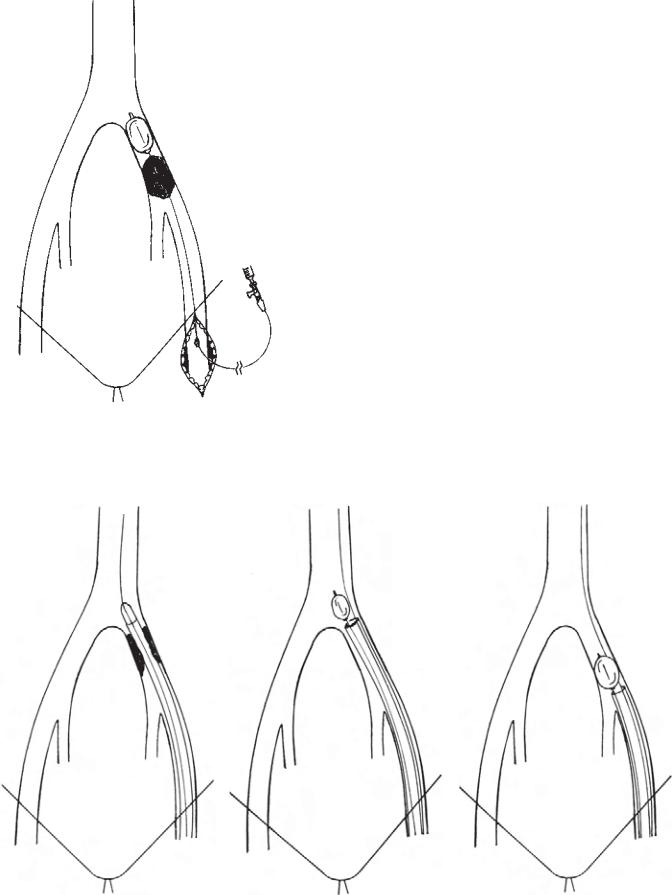
Рис. 33.4. Баллонный катетер легко проводится через область локализации тромба. Баллон раздувается и выполняется тромбоэмболэктомия.
Рис. 33.5. Проводник и направляющий катетер, введенные через интродьюссер, были проведены через пораженный сегмент. Эмболэктомический баллон-катетер на проводнике был проведен через тромб и выполнена тромбоэмболэктомия.
A |
|
Б |
|
B |
|
|
|
|
|
Рис. 33.6. (А) Интродьюсер-гайд проведен по проводнику за область поражения. (Б) Баллонный катетер для эмболэктомии был проведен через интродьюсер параллельно проводнику. (В) Баллон вместе с интродьюсером низводятся, оставляя на месте проводник.
402 Раздел V. Окклюзионные заболевания артерий
соответствующей ручкой. Так как это устройство значительно более жесткое по сравнению со стандартным баллонным катетером, оно способно отделять те тромбы, которые невозможно сместить обычным катетером. Однако и риск повреждения артерии при манипуляциях с таким катетером пропорционально увеличивается. Использование рентгеноскопии в таком случае дает возможность большего контроля и позволяет видеть дистальный конец катетера во время тромбэктомии, что увеличивает шансы на выполнение адекватной тромбэктомии, минимизируя риск повреждения сосуда.
Тромбэктомия из протеза
Тромбоз протеза является довольно частым осложнением реконструктивных операций. Другой специализированный катетер — катетер для тромбэктомии из протеза (Baxter Vascular Systems, Irvine, CA) — предназначен для удаления плотно адгезированных неоинтимальных масс, нарастающих внутри протеза. Этот катетер состоит из двух непокрытых, закрученных вокруг стилета проволок. Степень раскрытия проволок регулируется рычагом. И опять, это устройство позволяет удалить плотные тромботические наложения, но существует риск повреждения протеза и собствен-
A |
|
Б |
|
|
|
В |
|
Г |
|
|
|
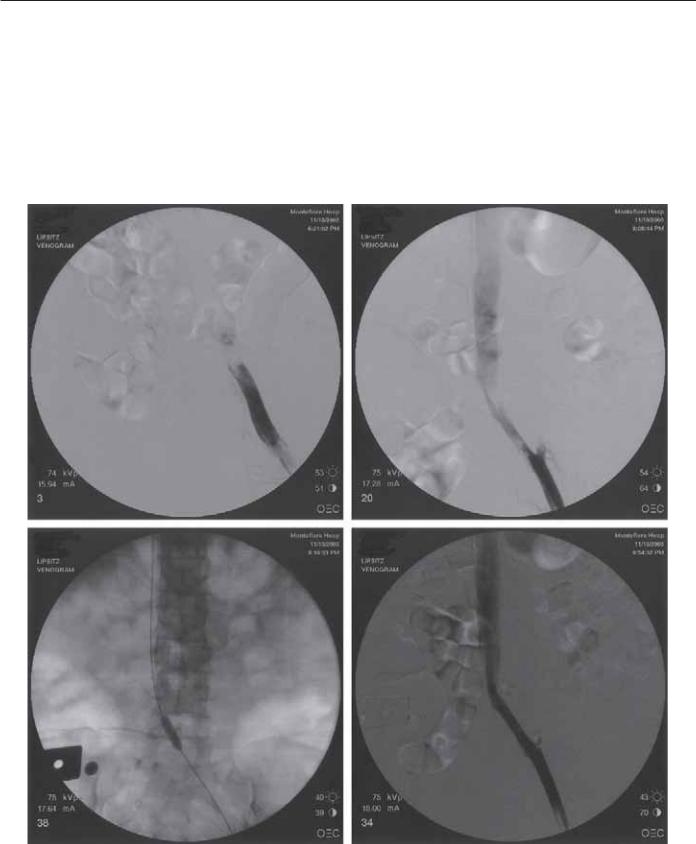
Рис. 33.7. Тромбоэмболэктомия под контролем рентгеноскопии выполняется при остром илиофеморальном венозном тромбозе при угрозе потери конечности. (А) Первичная венограмма демонстрирует окклюзию левой подвздошной вены. (Б) Последующая тромбэктомия, кровоток из подвздошных вен в нижнюю полую вену восстановлен, тем не менее отмечен остаточный дефект в месте слияния подвздошной и полой вен. (В) Эта область не подходит для тромбэктомии и должна подвергаться ангиопластике и стентированию. (Г) Контрольная венограмма демонстрирует улучшение кровотока через подвздошные вены в нижнюю полую вену. С иллюстративной целью показана только левосторонняя венография.
Глава 33. Тромбоэмболэктомия под контролем рентгеноскопии |
403 |
|
|
но артерии при работе в зоне анастомозов. Использование во время процедуры рентгеноскопии также способствует снижению риска повреждения протеза и сосуда.
Сейчас появилось много новых устройств для выполнения чрескожной механической тромбэктомии [11, 12]: устройства для аспирационной тромбэктомии, фрагментирующей тракционной тромбэктомии, ротационной и реолитической тромбэктомии. Эти приспособления имеют различные преимущества и недостатки, но, будучи предназначенными для чрескожного применения, все они используются под рентгеноскопическим контролем. Все эти устройства могут также применяться для тромбэктомий из вен [13]. Опыт, приобретенный в тромбоэмболэктомии под рентгеноскопическим контролем, может облегчить использование этих систем.
Венозная тромбэктомия
Острая ишемия конечности может возникнуть и в результате острого тромбоза глубоких вен, особенно илиофеморального тромбоза. В большинстве случаев синяя флегмазия «отвечает» на антикоагулянтную терапию и возвышенное положение конечности, однако при утрате неврологических функций и угрожающей гангрене конечности требуется фасциотомия и венозная тромбэктомия. В этой ситуации следует выполнять венографию. Если предстоит выполнение хирургической тромбэктомии, то рентгеноскопический контроль дает определенные преимущества и должен выполняться в большинстве случаев венозной тромбэктомии по тем же причинам, что и при артериальной тромбоэмболэктомии [14, 15]. Техника аналогична описанной для артериальной тромбоэмболэктомии с ренгеноскопическим контролем, за исключением того что поперечная венотомия выполняется проксимальнее сафенофеморального соустья. Оставшиеся дефекты в венозной системе также легко коррегируются ангиопластикой и стентированием [16]. Многие из этих дефектов лежат в основе «обострений хронического» тромбоза (рис. 33.7A–Г). Более дистально расположенные тромбы в таких случаях удаляются путем наложения повязки Эсмарха на конечность от стопы и выше.
Заключение
Ведение пациентов с тромбоэмболическими состояниями становится более сложным как в плане анатомии, так и в плане сопутствующих заболеваний, поэтому требуется более тщательный и внимательно спланированный подход, что обеспечило бы успешность лечения и уменьшение заболеваемости и смертности. Хотя сложно доказать, что тромбоэмболэктомия под контролем рентгеноскопии улучшает конечные исходы тромбоэмболэктомии, рентгеноскопический контроль все чаще и чаще используется при
этих и других сосудистых операциях, что во многих случаях дает огромное преимущество как для выполнения самой тромбоэмболэктомии, так и для планирования сопутствующих или последующих дополнительных вмешательств.
Литература
1.Braithwaite BD, Earnshaw JJ. Arterial embolectomy: a century and out. Br J Surg 1994; 81: 1705–1706.
2.KendrikJ, Thompson B, et al: Arterial embolectomy in the leg: results in a referral hospital. Am J Surg 1981; 142: 739–743.
3.Panetta T, Thompson J. et al: Arterial embolectomy: a 34-year experience with 400 cases. Surg Clin North Am 1986; 66: 339–353.
4.Abbott W. Maloney R, et al. Arterial embolism: a 44-year perspective. Am J Surg 1982; 143: 460–464.
5.Green R. DeWeese J, Rob C. Arterial embolectomy before and after the Fogarty catheter. Surgery, 1975; 77: 24–33.
6.Haimovici H, Moss C, Veith F. Arterial embolectomy revisited. Surgery 1975; 78: 409–410.
7.Fogarty T, Cranley J, et al. A method for extraction of arterial emboli and thrombi. Surg Gynecol Obstet 1963; 116: 241–244.
8.Albrechtsson U, Einarsson E, Tylen U. Complications secondary to thrombectomy with the Fogarty balloon catheter. Cardiovasc Intervent Radiol 1981; 4(1): 14–16.
9.Parsons RE, Marin ML, et al. Fluoroscopically assisted thromboembolectomy: an improved method for treating acute arterial occlusions. Ann Vase Surg 1996; 10: 201–210.
10.Radoux JM, Maiza D, Coffin O. Long-term outcome of 121 iliofemoral endarterectomy procedures. Ann Vasc Surg 2001; 15(2): 163–170.
11.Hill BB, Fogarty TJ. Thrombectomy catheters: basic concepts, design, and types. In Endovascular Surgery, 3rd edn. (Eds: Moore WS, Ahn SS). Philadelphia, PA: WB Saunders, 2001: 75–86.
12.Kasirajan K, Marek JM, Langsfeld M. Mechanical thrombectomy as a first-line treatment for arterial occlusion. Semin Vasc Surg 2001; 14(2): 123–131.
13.Delomez M, Beregi JP, et al. Mechanical thrombectomy in patients with deep venous thrombosis. Cardiovasc Intervent Radiol 2001; 24(1): 42–8.
14.Comerota AJ. Venous thromboembolism. In Vascular Surgery, 4th edn. (Ed: Rutherford RB). Philadelphia, PA: WB Saunders, 1995: 1785–1814.
15.Eklof B, Kistner RL. Surgical treatment of acute iliofemoral thrombosis. In Current Therapy in Vascular Surgery, 3rd edn. (eds Ernst CB, Stanley JC). St Louis, MO: Mosby, 1995: 932–935.
16.Semba CP, Dake MD: Catheter-directed thrombolysis for iliofemoral venous thrombosis. Semin Vasc Surg 1996; 9: 26–33.

Глава 34
Чрескожная аспирационная тромбоэмболэктомия
Родни А. Уайт
Чрескожная аспирационная тромбоэмболэктомия является одной из техник, которые могут использоваться для удаления тромбов и фрагментов атероматозных масс из просвета сосуда. Аспирационная тромбэктомия для растворения острых и хронических тромбов выполняется реже, чем тромболизис; она обычно используется во время интервенционной процедуры, когда эмболизирующий материал непосредственно занимает аспирационный катетер для тромбэктомии. Аспирационная тромбэктомия наиболее эффективна для рыхлого тромботического материала, который образуется во время ангиопластики или назначения тромболитической терапии [1], и сравнимого с размельченными фрагментами организованного тромба, фиброзных волокон или атеросклеротической бляшки, образующихся во время атерэктомии.
Хотя в упрощенном варианте аспирационная тромбэктомия подразумевает под собой внедрение в тромб и аспирацию части или всего материала в просвет полого катетера, разработаны модификации этой техники, включая и транслюминальную экстракционную атерэктомию (Транслюминальный экстракционный катетер, Интервенционные технологии, Сан Диего, СА) или другие методы размельчения тромба, включая ультразвуковые устройства или устройства с бьющей струей воды [2]. В этой главе описаны методы, используемые для выполнения аспирационной тромбэктомии, и представлен краткий обзор литературных источников, подтверждающих целесообразность ее выполнения.
Тромбоэмболии во время эндоваскулярных процедур
Замечено, что артериальная эмболия случается примерно в 5% процедур ангиопластики [3] и в 12,5–25% случаев местного тром-
болизиса с инфузией стрептокиназы или урокиназы [4]. Тромбоэмболы более часто образуются во время дилатации окклюзивных поражений, потому что мягкие тромбы, скапливающиеся вокруг недавних окклюзий, легко фрагментируются и мигрируют в дистальное русло. Если планируется ангиопластика, то симптомы, свидетельствующие о недавней окклюзии, должны настораживать в отношении возможных тромбоэмболических осложнений. Системная антикоагулянтная терапия и частое промывание катетеров во время чрескожных вмешательств помогает предупредить тромбоэмболические осложнения. Некоторые авторы предлагают проводить предварительную фибринолитическую терапию перед процедурами ангиопластики в качестве меры, уменьшающей частоту тромбоэмболий во время процедуры [5], в то время как другие авторы опасаются геморрагических осложнений такой терапии.
Чрескожная транскатетерная аспирационная техника
Чрескожная аспирационная эмболэктомия выполняется с использованием катетеров с большим просветом для удаления периферических эмболов или специально сконструированных катетеров для манипуляций в легочной артерии. Применение техники на периферических сосудах оправдано только для артериальных окклюзий ниже паховой связки. Таким образом, пациенты, являющиеся кандидатами на чрескожную эмболэктомию, должны иметь проходимые подвздошные артерии и пульсацию на бедренных артериях. Доступ к легочному кругу кровообращения осуществляется трансвенозно через бедренную или яремную вены под местной анестезией и рентгеноскопическим контролем.
