
- •6. Определение компонентного состава газов методом хроматографии
- •6.1. Физические основы и аппаратная реализация метода газовой хроматографии
- •Принципиальная схема хроматографа
- •Система подготовки газа–носителя
- •Дозирующие устройства
- •Хроматографические колонки
- •Детекторы
- •Система термостатирования
- •Программирование температуры
- •Регистрация результатов анализа
- •Газ–носитель
- •Неподвижная фаза
- •6.2. Хроматографический метод определения компонентного состава газов
- •Сущность метода
- •Аппаратура
- •Отбор и хранение проб
- •Отбор проб газа на анализ
- •Подготовка и проведение анализа
- •Обработка результатов
- •Точность метода
- •6.3. Задание для самостоятельной работы
- •6.4. Расчетная часть
- •6.4.1. Способы выражения состава смесей и связь между ними [27]
- •6.4.2. Расчет свойств газа по компонентному составу [27]
- •6.5. Приложение
- •Контрольные вопросы
Точность метода
Сходимость. Два результата определений, полученные одним исполнителем в одной лаборатории, признаются достоверными (с 95%-й вероятностью), если расхождение между ними не превышает значений, указанных в табл. 6.5.
Воспроизводимость. Два результата определений, полученные в двух разных лабораториях, признаются достоверными (с 95%-й вероятностью), если расхождение между ними не превышает значений, указанных в табл. 6.5.
Таблица 6.5
|
Объемная доля компонента |
Допускаемые расхождения между результатами двух определений, не более | |
|
сходимость |
воспроизводимость | |
|
от 0 до 0,1 свыше 0,1 до 0,5 свыше 0,5 до 1,0 свыше 1,0 до 5,0 свыше 5,0 до 25,0 свыше 25,0 |
0,02 0,05 0,08 0,15 0,50 1,00 |
0,04 0,10 0,15 0,30 0,80 1,50 |
6.3. Задание для самостоятельной работы
По рассчитанному из хроматограммы объемному (мольному) составу газа, вычислить:
состав газа в массовых единицах,
молярную массу смеси газов,
плотность смеси газов при нормальных и стандартных условиях тремя способами,
относительную плотность смеси газов при нормальных и стандартных условиях,
рассчитать и построить температурную зависимость плотности газа, считая его идеальным, при давлении 2 МПа и температурах 0, 10, 20, 40, 50 °С,
рассчитать и построить температурную зависимость плотности газа, считая его реальным, при давлениях 2 и 20 МПа и температурах 0, 10, 20, 40, 50 °С,*
сделать вывод по влиянию учета состояния (идеальный, реальный) газа на величину его плотности.
* – Температурные зависимости плотности для идеального и реального газов при давлении 2 МПа построить на одном графике.
Полученные результаты по расчету свойств газа представить в сводной табл. 6.6.
Таблица 6.6
Свойства исследованного газа
|
Свойства |
Размерность |
Значение | |
|
Плотность |
при н.у. |
кг/м3 |
|
|
при с.у. |
кг/м3 |
| |
|
Относительная плотность |
– |
| |
|
Молекулярная масса |
г/моль |
| |
Расчет температурной зависимости плотности газа представить в виде отдельных таблиц (табл. 6.9, 6.10).
6.4. Расчетная часть
6.4.1. Способы выражения состава смесей и связь между ними [27]
Массовая доля– массаi-го компонента, отнесенная к общей массе системы:
 (6.7)
(6.7)
Молярная (мольная) доля– число молейi-го компонента, отнесенное к общему числу молей в системе:
 (6.8)
(6.8)
Моль– количество вещества в граммах, численно равное его молекулярной массе.
Число молейравно массе веществаmi, деленной на молекулярную массуMi:
![]() (6.9)
(6.9)
Тогда:
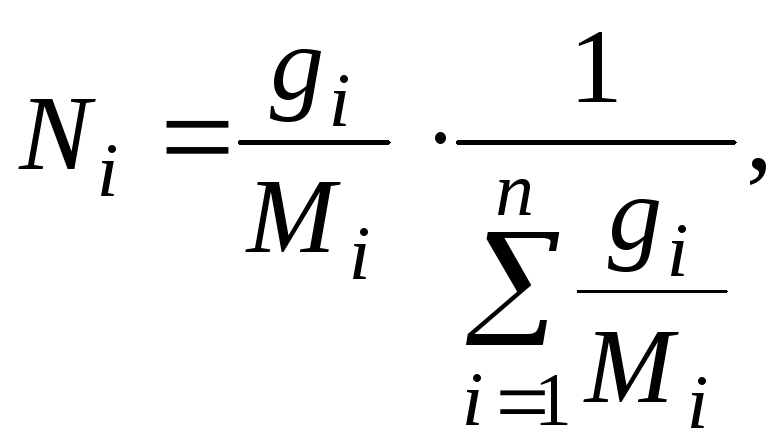 (6.10)
(6.10)
 (6.11)
(6.11)
 (6.12)
(6.12)
Объемная доля– отношение объемаi-го компонента в системе к общему объему системы:
 (6.13)
(6.13)
Тогда:
 (6.14)
(6.14)
 (6.15)
(6.15)
По закону Авогадро при одинаковых давлении и температуре 1 мольлюбого газа занимает одинаковый объем:
при н.у. – 273 К и 0,101 МПа – 22,414 л, при с.у. – 293 К и 0,101 МПа – 24,055 л.
Отсюда для газовых смесей
![]() (6.16)
(6.16)
объемный состав является и молярным составом.
