
- •Тема 3. Биосинтез аминокислот. Особенности обмена глицина, серина, серусодержащих и ароматических аминокислот.
- •3.1. Биосинтез аминокислот в тканях.
- •3.2. Обмен серина и глицина. Образование и перенос одноуглеродных групп.
- •3.3. Обмен метионина и реакции трансметилирования.
- •3.4. Биосинтез креатина и его последующие превращения.
- •3.5. Обмен фенилаланина и тирозина.
3.2. Обмен серина и глицина. Образование и перенос одноуглеродных групп.
3.2.1. Главную роль в реакциях обмена серина и глицина играют ферменты, в состав которых в качестве кофермента входит тетрагидрофолиевая кислота (ТГФК). ТГФК образуется в организме в результате восстановления фолиевой кислоты (витамина Вс).
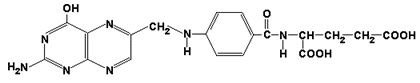 фолиевая
кислота
фолиевая
кислота
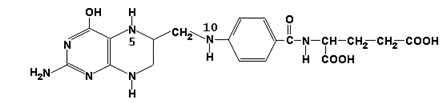 ТГФК
ТГФК
3.2.2. Реакционноспособными центрами в молекуле ТГФК являются атомы азота в положениях 5 и 10. Атомы водорода при N5 и N10 могут замещаться на различные одноуглеродные группы: метильную (-СН3), метиленовую (-СН2-), метенильную (=СН-), формильную (-СН=О) и некоторые другие. Основными источниками одноуглеродных групп в клетке служат серин и глицин.
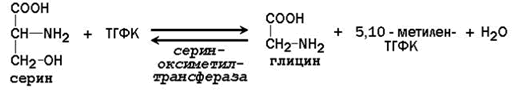
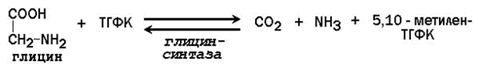
5,10-Метилен-ТГФК используется как донор метильной группы в реакциях биосинтеза тимидилового нуклеотида.
При окислении 5,10-метилен-ТГФК образуются 5,10-метенил-ТГФК и 10-формил-ТГФК. Эти производные ТГФК служат источниками атомов углерода в процессе биосинтеза пуриновых нуклеотидов (аденилового и гуанилового).
При восстановлении 5,10-метилен-ТГФК образуется 5-метил-ТГФК. Это соединение интересно тем, что может поставлять метильную группу для регенерации метионина из гомоцистеина (см. далее).
3.2.3. Аминокислота глицин, помимо участия в синтезе белка и образовании различных одноуглеродных групп, является предшественником ряда специализированных биомолекул:
оба атома углерода и атом азота глицина могут включаться в структуру пуринового ядра (атомы С4, С5 и N7);
глицин является главным предшественником порфиринов (простетической группы гемоглобина, миоглобина, цитохромов);
глицин участвует в синтезе креатина - предшественника креатинфосфата, участвующего в биоэнергетике мышечной и нервной ткани;
глицин входит в состав пептидного кофермента глутатиона;
участвует в образовании конъюгатов (гликохолевая кислота, гиппуровая кислота).
3.3. Обмен метионина и реакции трансметилирования.
3.1.1. Метильная группа метионина, связанная с атомом серы, также представляет собой подвижную одноуглеродную группу, способную участвовать в реакциях трансметилирования (переноса метильной группы). Активной формой метионина, принимающей непосредственное участие в этих превращениях, является S-аденозилметионин, который образуется при взаимодействии метионина с АТФ.
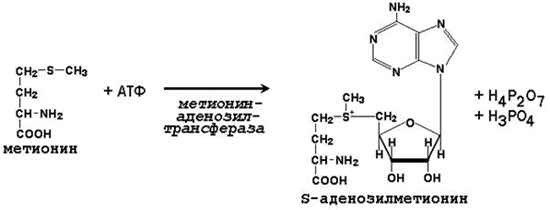
Примеры реакций трансметилирования с участием S-аденозилметионина приводятся в таблице 3.1.
Таблица 3.1
Использование метильной группы S-аденозилметионина в реакциях трансметилирования
|
Субстрат |
Метилированный продукт |
|
Норадреналин |
Адреналин |
|
Адреналин |
Метоксиадреналин |
|
Гуанидинацетат |
Креатин |
|
Карнозин |
Ансерин |
|
Гистамин |
N-метилгистамин |
|
Фосфатидилэтаноламин |
Фосфатидилхолин |
Вот некоторые примеры этих реакций.
1) Образование фосфатидилхолина из фосфатидилэтаноламина - ключевая реакция синтеза фосфолипидов:
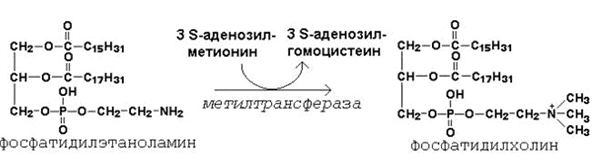
Фосфатидилхолин – главный фосфолипидный компонент биологических мембран; он входит в состав липопротеинов, принимает участие в транспорте холестерола и триацилглицеролов; нарушение синтеза фосфатидилхолина в печени приводит к жировой инфильтрации.
2) Образование адреналина из норадреналина - заключительная реакция синтеза гормона мозгового вещества надпочечников:
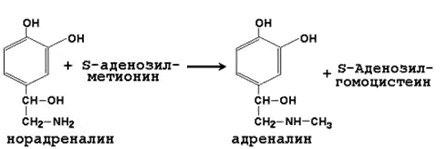
Адреналин выделяется в кровь при эмоциональном стрессе и участвует в регуляции углеводного и липидного обмена в организме.
3) Реакции метильной конъюгации - один из этапов обезвреживания чужеродных соединений и эндогенных биологически активных веществ:
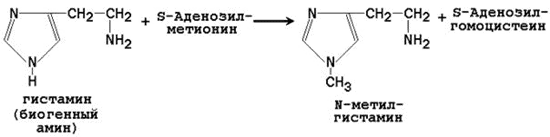
В результате метилирования блокируются реакционноспособные SH- и NН-группы субстратов. Продукты реакции не обладают активностью и выводится из организма с мочой.
3.3.3. После отдачи метильной группы S-аденозилметионин превращается в S-аденозилгомоцистеин. Последний расщепляется на аденозин и гомоцистеин. Гомоцистеин может вновь превращаться в метионин за счёт метильной группы 5-метил-ТГФК (см. предыдущий параграф):

В этой реакции в качестве кофермента участвует метилкобаламин – производное витамина В12. При недостатке витамина В12 нарушается синтез метионина из гомоцистеина и накапливается 5-метил-ТГФК. Так как реакция образования 5-метил-ТГФК из 5,10-метилен-ТГФК необратима, одновременно возникает дефицит фолиевой кислоты.
3.3.4. Другим путём использования гомоцистеина, как уже упоминалось, является участие в синтезе цистеина. Биологическая роль цистеина:
входит в состав белка, где может образовывать дисульфидные связи, стабилизирующие пространственную структуру макромолекулы;
участвует в синтезе глутатиона, причём цистеиновая SH-группа определяет реакционную способность этого кофермента;
является предшественником тиоэтаноламина в молекуле HS-КоА;
служит предшественником таурина в конъюгированных желчных кислотах;
является источником атома серы в органических сульфатах (хондроитинсульфат, гепарин, ФАФС).
