
Вьюник. Лекция № 3
.pdf
Хiмiчна термодинамiка |
Енергетичнi ефекти процесiв |
Незворотнi та зворотнi процеси |
Внутрiшня енергiя та ентальпiя
Ентальпiя
Суть H можна пояснити слiдуючим чином. Якщо газ знаходиться в цилiндрi, де вiн "замкнутий "невагомим поршнем, тодi енергiя газу i поршня з вагою (вантажем) буде дорiвнювати U+PSH, де PSH потенцiальна енергiя поршня з вагою. SH = V, тодi PSH = PV.
Якщо дати можливiсть поршню вiльно перемiщуватися, то газ виконає роботу. Тому H можна розглядати як енергiю розширеної системи.
h |
s |
p |
11/30
Хiмiчна термодинамiка |
Енергетичнi ефекти процесiв |
Незворотнi та зворотнi процеси |
Енергетичнi ефекти процесiв
Енергетичнi ефекти процесiв. Хiмiчнi процеси протiкають або з видiленням, або з поглинанням тепла, вiдповiдно екзота ендотермiчнi процеси.
Наприклад: H−H + Cl−Cl = H−Cl + H−Cl, H < 0.
Цей процес екзотермiчний: виграш утворення 2- зв‘язкiв H−Cl (2 · 431 Кдж/моль) перекриває витрату енергiї на розрив зв‘язкiв H−H (434.2Кдж/моль) та Cl−Cl (242.4 Кдж/моль)
2 · 431 > 434.2 + 242.4
Кiлькiсть видiленого або поглинутого тепла називається тепловим ефектом процесу (теплом).
Тепловий ефект необхiдно характеризувати не тiльки абсолютною величиною, але i знаком. Тепловий ефект ендотермiчних процесiв (+), а екзотермичних (−), вiдповiдно > 0 та < 0. Вiдносять до 1 моль речовини.
12/30
Хiмiчна термодинамiка |
Енергетичнi ефекти процесiв |
Незворотнi та зворотнi процеси |
Енергетичнi ефекти процесiв
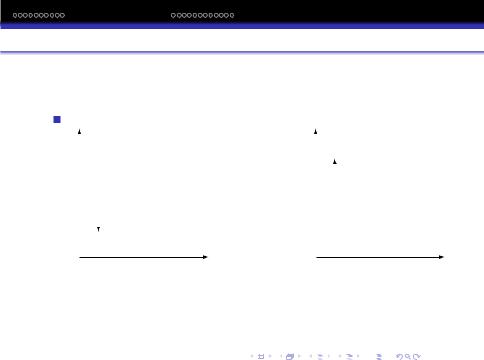
Ентальпiйна дiаграма:
H |
|
|
Реагенти |
|
H1 |
H |
|
|
|
Продукти |
||||
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H2 |
|
|
|
|
|
ΔH<0 |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
ΔH>0 |
|||
|
|
|
|
|
|
H2 |
|
|
|
|
|
|
|
H1 |
|
|
|
|
|
|
|||||||||
|
|
|
Продукти |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
Реагенти |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Екзотермiчна реакцiя |
Ендотермiчна реакцiя |
|||||||||||||
13/30
Хiмiчна термодинамiка |
Енергетичнi ефекти процесiв |
Незворотнi та зворотнi процеси |
Енергетичнi ефекти процесiв
Тепловi ефекти виражають в Кдж/моль ( Ккал/моль ). Зазвичай тепловi ефекти вiдносять до стандартних умов (P = 1 атм, T = 298K ) P,T = CONST iзобарно-iзотермiчний процес.
Термохiмiчнi рiвняння – запис хiмiчних реакцiй з безпосередньою вказiвкою в них теплового ефекта.
H |
2 (г.) |
+ 1 O |
2 (г.) |
= H |
O |
(рiд.) |
−285 Кдж. |
|
||||||||||||
|
|
2 |
|
|
|
|
2 |
|
|
|
|
|
||||||||
1 H |
2 (г.) |
+ |
1 Cl |
2 (г.) |
= HCl |
|
ΔH = −92 |
Кдж. |
||||||||||||
2 |
|
|
|
2 |
|
|
|
|
|
(г.) |
|
|
|
|
моль |
|||||
ΔH = E |
− |
Cl |
− 1 |
(E |
− |
H |
+ E |
|
− |
Cl |
) = −92 |
Кдж. |
||||||||
|
|
|
|
H |
|
|
|
2 |
|
H |
|
|
Cl |
|
моль |
|||||
Енергетичнi ефекти хiмiчних реакцiй вивчає термохiмiя. Термохiмiя - роздiл хiмiї, в якому вивчаються тепловi ефекти рiзних процесiв (утворення речовин, їх згоряння, взаємодiї, розчинення, плавлення i т.iнше).
14/30
Хiмiчна термодинамiка |
Енергетичнi ефекти процесiв |
Незворотнi та зворотнi процеси |
Енергетичнi ефекти процесiв
Тепловi ефекти вимiрюють експериментально за допомогою калориметрiв.
Калориметр – прилад у якого вiдсутнiй теплообмiн з навколишнiм середовищем. ΔH = C·ΔT, де c – питома теплоємнiсть складових частин калориметра.
Знаки теплових ефектiв в термохiмiї та в термодинамiцi рiзнi: для екзотермiчного ефекта в термохiмiї (+), в термодинамiцi (−).
15/30
Хiмiчна термодинамiка |
Енергетичнi ефекти процесiв |
Незворотнi та зворотнi процеси |
Термохiмiчнi розрахунки. Закон Гесса
Теплоти процесiв можна розрахувати.
Термохiмiчнi розрахунки. Закон Гесса. В основi розрахункiв використовується закон, сформульований в 1840р. росiйським вченим Гессом.
Формулiровка: Сумарний тепловий ефект ряду послiдовних хiмiчних реакцiй дорiвнює тепловому ефекту любого другого ряду реакцiй з тими ж самими початковими та кiнцевими продуктами.
Другими словами тепловий ефект реакцiї (процесу) не залежить вiд шляху по якому протiкає (вiдбувається) процес (перехiд), а визначається лише початковим та кiнцевим станом системи.
16/30
Хiмiчна термодинамiка |
Енергетичнi ефекти процесiв |
Незворотнi та зворотнi процеси |
Термохiмiчнi розрахунки. Закон Гесса
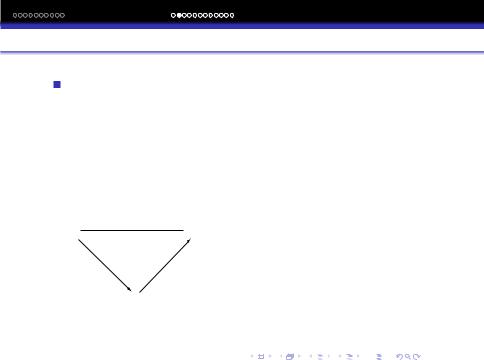
Суть цього положення можна зрозумiти, розглянувши реакцiї одержання CO2:
1.C(гр.) + O2 (г.) = CO2 (г.), ΔH
2.C(гр.) + 12 O2 (г.) = CO(г.) , ΔH1 CO(г.) + 12 O2 (г.) = CO2(г.), ΔH2
ΔH = ΔH1 + ΔH2 При T(поч.) = T(кiнц.), P(почат.) = P(кiнц.)
тепловi ефекти будуть однаковими.
ΔH
C(гр)
ΔH |
ΔH |
1 |
|
|
CO(г) |
 CO2(г)
CO2(г)
2
Термодинамiчний (термохiмiчний) цикл.
17/30
Хiмiчна термодинамiка |
Енергетичнi ефекти процесiв |
Незворотнi та зворотнi процеси |
Термохiмiчнi розрахунки. Закон Гесса
Застосування:
а) H1 = H − H2 Можна визначити H1. Експеримен-
тальним шляхом визначити неможливо.
1
б) H = EHCl − 2(EH−H + ECl−Cl)
Закон Гесса є одним iз наслiдкiв ЗЗМ. Наслiдки iз закону Гесса:
1Тепловий ефект хiмiчної реакцiї дорiвнює рiзницi мiж сумою теплоутворення продуктiв реакцiї i сумою теплоутворення
реагентiв. ΔHхр. = ( ΔHутв.)пр.р − ( ΔHутв.)реаг.
2Тепловий ефект хiмiчної реакцiї дорiвнює рiзницi мiж сумами теплот згоряння та продуктiв реакцiї:
Hхр. = ( Hзгор.)реаг. − ( Hзгор.)пр. реак.
18/30
Хiмiчна термодинамiка |
Енергетичнi ефекти процесiв |
Незворотнi та зворотнi процеси |
Термохiмiчнi розрахунки. Закон Гесса
При алгебраїчних розрахунках необхiдно враховувати стехiометричнi коефiцiєнти компонентiв: AA+BB+··· = CC+ DD · ··
ΔHхр = (C(ΔHутв.)C + D(ΔHутв. )D + ···) − (AΔHутв.)A + B(ΔHутв.)B + ···).
Закон Гесса та його наслiдки не можуть бути використанi, якщо ми не домовимося, який змiст вкладати в поняття теплоутворення та теплозгоряння.
Пiд теплоутворенням розумiють тепловий ефект реакцiї утворення 1 моля речовини iз простих речовин, стiйких в стандартних умовах.
Позначення змiни ентальпiй утворення за стандартних умов:
ΔH0утв.,298, ΔH0f ,298
Для простих речовин стiйких в стандартних умовах ΔH0f,298 приймають рiвними 0.
19/30
Хiмiчна термодинамiка |
Енергетичнi ефекти процесiв |
Незворотнi та зворотнi процеси |
Термохiмiчнi розрахунки. Закон Гесса
Пiд теплозгорянням зазвичай розумiють тепловий ефект реакцiї згоряння 1 моля речовини до CO2 та H2O. Для решти елементiв для кожного конкретного випадку вказують продукти окиснення.
ΔHзгор. негорючих речовин прирiвнюють 0.
ΔH0згор.(H2O) = 0
Складено таблицi стандартних теплових ефектiв. Вiдомi
Hутв0 .,298 приблизно для 4000 сполук. Це дає можливiсть шляхом розрахунку одержати тепловi ефекти для рiзних
речовин.
При термохiмiчних розрахунках припускається, що газуватi речовини володiють властивостями iдеальних газiв.
20/30
