
Вариант 7.
1. Какова электронная конфигурация иона Fe2+?
А. 1s22s22p63s23p64s23d4
B. 1s22s22p63s03p0
C. 1s22s22p63s23p64s03d6
D. 1s22s22p63s23p0
E. 1s22s22p63s23p4
2. В организме человека многие d-элементы образуют комплексные соединения. Выберите соединение, в состав которого входит медь (Cu).
А. гемоглобин
В. Витамин В12
С. Карбоангидраза
D. ксантиноксидаза
Е. гемоцианин
3. Какое количество молей FеСl3 содержится в 200 мл 0,1М раствора?
А. 0,2 моля
В. 0,02моля
С. 0,1 моль
D. 0,01моль
Е. 1 моль
4. Определите координационное число комлексообразователя в соединении [Со(NН3)6]Cl3.
А. 2
В. 4
С. 3
D. 6
Е. 5
5. Определите степень окисления иона комплексообразователя в соединении К4[Fe(CN)6].
А. +2
В. +4
С. +3
D. -2
Е. -3
6. Рассчитайте рН раствора и определите тип реакции среды, если концентрация ионов водорода в растворе
[Н+] = 1·10-5 М.
А. рН=5, кислая
В. рН=5, основная
С. рН=9, основная
D. рН=9, кислая
Е. рН=5, нейтральная
7. У пациента с избыточной кислотностью желудочного сока нарушаются процессы переваривания белков. Каким в норме должно быть рН в желудке?
А. 3,5-4,0
В. 4,5-5,0
С. 2,5-3,1
D. 0,1-0,5
Е. 1,5-2
8. Какие соединения являются компонентами фосфатного буфера:
А. NaH2PO4 и Н2О
В. NaH2PO4 и Na2HPO4
С. NaH2PO4 и Н3PO4
D. H3PO4 и Н2О
Е. NaH2PO4 и H2CO3
9. Какое математическое выражение позволяет рассчитать значение осмотического давления раствора электролита:
А. π = СRT
В. π = iСRT
С. π = iКкрСm
D. π = iКкр
Е. π = Ккр(Т2-Т1)
10. Растворы веществ в воде замерзают при температуре более низкой, чем чистая вода. Рассчитайте температуру замерзания 5% раствора NaCl в воде. (ККР = 1,86)
А. -1,75 ºC
В. -3,35 ºC
С. -5 ºC
D. -1,6 ºC
Е. -3,2 ºC
11. Какой из растворов равной концентрации имеет наименьшее осмотическое давление при 298 К ?
A раствор Al2(SO4)3
B раствор NaCl
C раствор глюкозы
D раствор MgCl2
E раствор AlCl3
12. Явления гемолиза и плазмолиза наблюдаются при помещении эритроцитов в раствор, в котором концентрация ионов не соответствует таковой в плазме крови. В каком из приведенных растворов эритроциты будут подвергаться плазмолизу?
А. 0,1% NaCl
В. 0,9% NaCl
С. 0,09% NaCl
D. 0,05 % NaCl
Е. 1,2% NaCl
13. Для реакции N2(газ) + 3Н2(газ) →2NН3(газ) имеются следующие данные:
ΔΗº N2(газ) = 0 кДж/моль
ΔΗº Н2(газ) = 0кДж/моль
ΔΗº NН3(газ )= 46кДж/моль
Рассчитайте изменение энтальпии для этой реакции.
А. - 92 кДж
В. 92 кДж
С. - 46 кДж
D. 46 кДж
Е. 0 кДж
14. Выберите математическое выражение для константы равновесия данной реакции:
Н2(газ) + 3N2 (газ) → 2NH3 (газ)
А.
![]()
В.
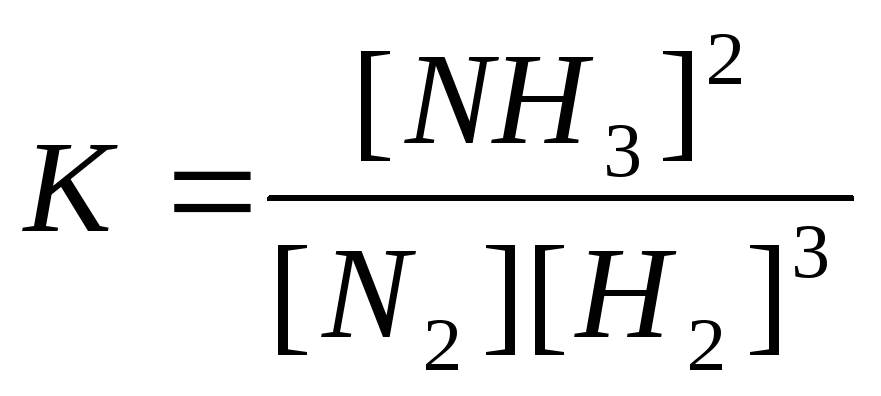
С.
![]()
D.
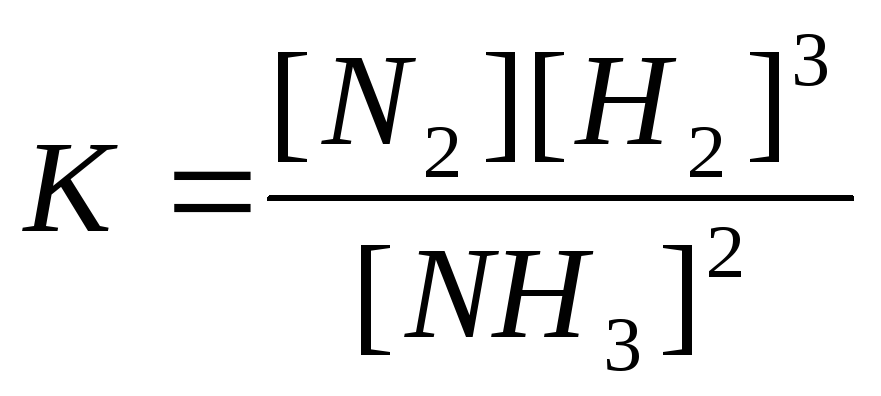
Е.
![]()
15. Определите, какой из ионов имеет большую адсорбционную способность.
А. SO42-
В. I-
С. Вr-
D. Cl-
Е. PO43-
16. Определите, какой из растворов обладает наименьшим поверхностным натяжением?
А. 0,1М СН3ОН
В. 0,1М С2Н5ОН
С. 0,1М С3Н7ОН
D. 0,1М С4Н9ОН
Е. Спирты не являются ПАВ
17. Агрегативная устойчивость коллоидных растворов это:
A Способность сохранять распределение частиц
B Способность сохранять размер частиц
C Оседание частиц под действием силы тяжести
D Коагуляция под действием электролита
E Способность проходить через поры обычных фильтров
18. Лиофобный золь ВаSO4 был получен при действии избытка ВаCl2 на раствор Na2SO4:
ВаCl2(изб) + Na2SO4 → ВаSO4↓ + 2NaCl.
Определите противоион в полученной мицелле.
А. Ва2+
В. SO42-
С. Na+
D. Cl-
Е. Н+
19. Определите, какой из ионов обладает максимальным коагулирующим действием на золь с положительно заряженной гранулой?
A Mg2+
B Al3+
C Na+
D CI-
E SO42-
20. К раствору белка добавили раствор (NH4)2SО4. Какой процесс наблюдался в результате?
А. Увеличение растворимости белка
В. Уменьшение растворимости белка
С. Высаливание
D. Изменение заряда белка
Е. Уменьшение гидрофильной способности белка
