
- •1. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
- •1.1.Основные понятия и определения
- •1.1.1.Термодинамическая система
- •1.1.2.Термодинамический процесс
- •1.1.3.Термодинамические функции состояния
- •1.2.Тепловые эффекты физико-химических процессов
- •1.2.2.Первое начало термодинамики
- •1.2.3.Тепловой эффект химической реакции
- •1.2.4.Термохимические расчеты
- •1.2.5.Зависимость теплового эффекта реакции от температуры
- •1.3. Направление и пределы протекания химического процесса
- •1.3.1.Второе начало термодинамики
- •1.3.2.Энтропия
- •1.3.3.Направление химического процесса
- •1.3.4. Химический потенциал
- •2. КИНЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
- •2.1. Механизм химической реакции
- •2.1.1.Частицы, участвующие в химической реакции
- •2.1.2.Классификация химических реакций
- •2.2. Элементарная химическая реакция
- •2.2.1.Скорость химической реакции
- •2.2.2.Зависимость скорости химической реакции от концентрации реагирующих веществ
- •2.2.3. Константа скорости химической реакции
- •2.3.Формальная кинетика гомогенных реакций
- •2.3.1.Кинетическое уравнение необратимой реакции первого порядка
- •2.3.2. Кинетическое уравнение необратимой реакции второго порядка
- •2.3.3.Реакции нулевого и высших порядков
- •2.3.4. Зависимость скорости реакции от температуры
- •2.3.5.Определение кинетических параметров реакции
- •2.3.6.Кинетическое уравнение обратимой реакции первого порядка
- •2.4.Цепной механизм химической реакции
- •2.5.Индуцированные реакции
- •2.5.1. Фотохимические реакции
- •2.5.2.Радиационно–химические процессы
- •2.6.Макрокинетика
- •2.6.1.Гетерогенные реакции
- •2.6.2.Горение и взрыв
- •2.7.Катализ
- •2.7.1.Гомогенный катализ
- •2.7.2.Гетерогенный катализ
- •3. ХИМИЧЕСКОЕ РАВНОВЕСИЕ
- •3.1.Термодинамическое условие химического равновесия
- •3.1.1. Изобара реакции
- •3.1.2. Изотерма реакции
- •3.3. Расчет равновесного состава газовой смеси
- •3.4. Равновесия в растворах
- •3.4.1.Растворы
- •3.4.2. Электролитическая диссоциация
- •3.4.3.Ионное произведение воды. Водородный показатель
- •3.4.4.Растворы кислот и оснований
- •3.4.5.Буферные растворы
- •3.4.6. Гидролиз солей
- •3.4.7.Обменные реакции с образованием осадка
- •3.5. Фазовые равновесия
- •3.5.1. Правило фаз Гиббса
- •3.5.2.Диаграмма состояния однокомпонентной системы
- •3.5.3. Диаграмма состояния двухкомпонентной системы
- •3.5.4. Кипение и кристаллизация растворов
газообразных, например при перемешивании системы.
Смешанный режим. Скорости химической реакции и диффузии сравнимы по величине, поэтому общая скорость процесса будет определяться как вероятностью активных столкновений частиц, так и процессами массопереноса.
2.6.2.Горение и взрыв
Быстропротекающие экзотермические реакции химического превращения веществ (взрывчатые превращения) могут осуществляться в режимах горения или взрыва. При их протекании отдельные части системы имеют различную температуру и различный химический состав. Реакции, возникающие в какой-либо части системы, самоускоряются, достигают максимально возможной скорости и распространяются на всю систему.
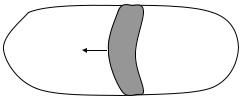
При протекании взрывчатых превращений в системе можно выделить три области (рис.2.12): область исходных веществ, область химической реакции и область продуктов реакции. Необходимо отметить, что исходные вещества и продукты реакции можно рассматривать как системы, находящиеся в состоянии термодинамического равновесия. В относительно узкой зоне – области химических реакций – происходит инициирование процесса и собственно процесс превращения исходных веществ в продукты реакции. Эта область движется по объему вещества с большой скоростью.
Исходные |
|
Продукты |
вещества v |
Т2, |
реакции |
Т1, р1 |
р2 |
Т3, р3 |
|
|
Область
химической
реакции
Рис. 2.12. Схема развития процесса горения и взрыва: v – скорость и направление движения области химической реакции; Т1, р1 – температура и давление в области исходных веществ, Т2, р2 – в области химической реакции, Т3, р3 – в области продуктов реакции
Для того чтобы процесс был самораспространяющимся, температура исходных веществ, находящихся вблизи области химической реакции, должна достигнуть определенной величины. Это осуществляется относительно медленно в случае горения, когда температура исходных веществ повышается за счет теплопередачи от продуктов реакции. Повышение температуры исходных веществ и соответственно инициирование реакций может происходить также при распространении ударной волны (волны
74
сжатия), которая, сжимая вещество, разогревает его. Ударная волна вызывается увеличением давления в области протекания реакции (р2) за счет роста температуры Т2 и образования большого количества газообразных продуктов.
Линейная скорость (v) движения области химических реакций при горении составляет величину 10-3-102 м/с, а при взрыве достигает ~ 103- 104 м/с (максимальная скорость распространения ударной волны равна скорости звука в веществе).
Инициирование и развитие взрывчатого превращения, распространение области химических реакций определяются как процессами теплопередачи, так и диффузией различных веществ, содержащихся в реагирующих веществах, в промежуточных и конечных продуктах химического превращения.
Частицы промежуточных продуктов реакции могут служить активными центрами ее развития, и поэтому скорость их переноса часто оказывает решающее влияние на скорость распространения взрывчатого превращения. Особое значение эти процессы имеют при инициировании и развитии взрывчатого превращения за счет протекания цепных реакций с разветвленными цепями (цепной взрыв).
Рассмотрим условия протекания взрывчатого превращения при тепловом инициировании (тепловой взрыв). Н.Н. Семенов показал, что если в замкнутой системе протекает экзотермическая реакция, то температура вещества будет зависеть от скорости поступления тепла за счет химической реакции (теплоприход) и скорости отвода тепла в окружающую среду за счет теплопередачи (теплоотвод).
Теплоприход Q+ увеличивается экспоненциально с ростом температуры, поскольку экспоненциально растет скорость химической реакции:
|
|
− |
Eак |
|
− |
Eак |
|
Q ~ v |
r |
H , v~ const e |
R T |
, |
Q ~ const e |
R T |
, |
+ |
|
|
|
+ |
|
|
v – скорость химической реакции; rH < 0 – тепловой эффект реакции; Eак – энергия активации химической реакции.
Теплоотвод Q- за счет теплопередачи через поверхность площадью S линейно зависит от разности температур системы Т и окружающей среды
Т0:
Q− ~ αS (T–T0),
α – коэффициент теплопередачи. Так как температура окружающей среды – величина постоянная (Т0-const), теплоотвод линейно увеличивается с ростом температуры.
В зависимости от природы взрывчатых веществ и условий осуществления взрывчатого превращения возможны следующие соотношения скоростей теплоприхода и теплоотвода (рис.2.13).
75
