
Изотермический процесс
Если в некотором процессе не изменяются масса и температура газа, то такой процесс называется изотермическим.
При m = const T = const P1V1 = P2V2 или PV = const.
Полученное PV = const уравнение называется уравнением изотермического процесса.
Это уравнение было получено английским физиком Робертом Бойлем в 1662 году и французским физиком Эдмоном Мариоттом в 1676г.
Уравнение Р1 / Р2 = V2 / V1 называется уравнением Бойля-Мариотта.
Состояние газа характеризуется тремя макропараметрами:
P — давлением,
V — объёмом,
T — температурой.
При графическом изображении процесса можно указать только два параметра, которые изменяются, поэтому один и тот же процесс можно представить в трёх координатных плоскостях: (Р – V), (V – T), (P – T).
График изотермического процесса называется изотермой. Изотерма, изображенная в прямоугольной системе координат (P – V), по оси ординат которой отсчитывается давление газа, а по оси абсцисс — его объем, является гиперболой (рис.3).
Изотерма, изображенная в прямоугольной системе координат (V – T), является прямой, параллельной оси ординат (рис.4).
Изотерма, изображенная в прямоугольной системе координат (P – T), является прямой, параллельной оси ординат (рис.5).
Графики изотермического процесса изображаются так:
Рис.3

Рис.4
Рис.5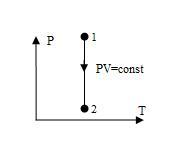
ИЗОХОРНЫЙ ПРОЦЕСС
Изохорным процессом называется процесс, протекающий при постоянном объёме (V = const) и при условии m = const и М = const.
При этих условиях из уравнения состояния идеального газа для двух значений температуры Т0 и Т следует:
P0V = m RT0
РV = МRT или Р / Р0 = Т / Т0
Для газа данной массы отношение давления к температуре постоянно, если объем газа не меняется. При P1 / P2 = T1 / T2 (это уравнение называется законом Шарля), оно применимо для изохорного процесса: V =const.
Это уравнение изохорного процесса.
Если V — объем газа при абсолютной температуре Т, V0 — объем газа при температуре 00 С; коэффициент а, равный 1/273 K-1, называемый температурным коэффициентом объемного расширения газов, то уравнение для изохорного процесса можно записать как P = P0 × a ×T.
Кривая изохорного процесса называется изохорой.
Изохора, изображенная в прямоугольной системе координат (P – V), по оси ординат которой отсчитывается давление газа, а по оси абсцисс — его объем, является прямой, параллельной оси ординат (рис.6).
Изохора, изображенная в прямоугольной системе координат (V – T), является прямой, параллельной оси абсцисс (рис.7).
Изохора, изображенная в прямоугольной системе координат (P – T), по оси ординат которой отсчитывается давление газа, а по оси абсцисс — его абсолютная температура, является прямой, проходящей через начало координат (рис.8).
Экспериментальным путем зависимость давления газа от температуры исследовал французский физик Жак Шарль в 1787г.
Изохорный процесс можно осуществить, например нагреванием воздуха при постоянном объеме.
Графики изохорного процесса изображаются так:
Рис. 6
Рис. 7
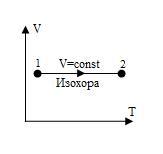
Рис. 8
