
- •Гидравлика
- •Поверхностное натяжение.
- •Давление жидкостей.
- •Отстаивание в поле центробежной силы (центрифугирование)
- •Фильтрование
- •Фильтрование с образованием несжимаемого осадка на несжимаемой перегородке
- •Транспорт дисперсных частиц
- •Гидравлическое сопротивление неподвижного слоя при ламинарном режиме движения жидкости.
- •Гидравлическое сопротивление неподвижного слоя при турбулентном режиме движения жидкости
- •Определение скорости начала псевдоожижения
- •I. Перемешивание
- •Констукции мембранных аппаратов
- •Кристаллизация из растворов
- •3.Теплосодержание () влажного воздуха
- •Материальный и тепловой баланс сушки
- •Тепловой баланс простой сушилки
- •Расчет простой сушилки
- •Адсорбция
Тепловой баланс простой сушилки
Тепловой баланс
![]()
![]()
![]()
![]()
![]()
![]() - потери тепла с уходящим материалом
- потери тепла с уходящим материалом
![]() - удельный расход а.с.в.
- удельный расход а.с.в.
![]()
Удельные потери тепла:
![]() ;
;
![]() ;
;![]() ;
;![]()
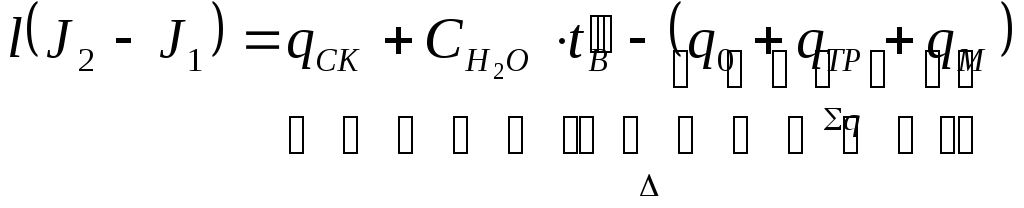
![]() -
суммарные удельные потери тепла
-
суммарные удельные потери тепла
![]() - уравнение реального процесса сушки
- уравнение реального процесса сушки
![]() характеризует отклонение реального
процесса сушки от идеального
характеризует отклонение реального
процесса сушки от идеального
|
|
- уравнение идеального процесса сушки |
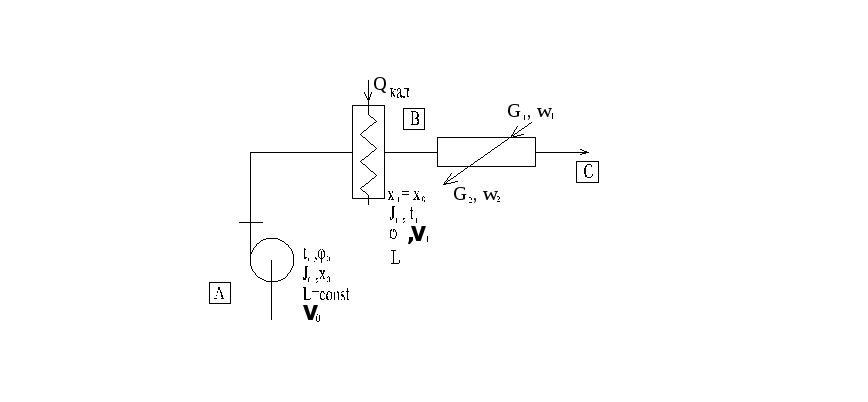
Расчет простой сушилки
Дано:G1,W1,W2
t0,φ0 t1 t2
|
|
А |
B |
Cтеор |
Cдейств |
|
x, |
x0 |
x1= x0 |
(x2)T |
(x2)g |
|
t,0C |
t0 |
t1 |
t2 |
t2 |
|
φ,% |
φ0 |
φ1 |
(φ2)T |
(φ2)g |
|
J, |
J0 |
J1 |
J2= J1 |
(J2)g |

АВ – процесс нагрева воздуха в калорифере
ВСТ– теоретический процесс сушки
ВСg– действительный процесс сушки
Δ=qCK+CH![]() Ot
Ot![]() -
-![]() ;
пусть Δ>0, тогдаJ2-J1=
;
пусть Δ>0, тогдаJ2-J1=![]() иJ2>J1
иJ2>J1
Расчет:
1.W=G1![]()
2l =![]() ;
;![]()
3. L![]() =l·W
=l·W
4.
![]() ,
Vy=f(x0,t0)
,
Vy=f(x0,t0)![]()
5. Расход тепла в калорифереQкал=L(J1-J0)[квт]
Основы теории массообмена
В технологии водоподготовки и очистки сточных вод важное условие имеют процессы массообмена, которые характеризуются переходом одного или нескольких веществ из одной фазы в другую. Путем переноса одного или более компонентов из фазы в фазу можно разделять как гомогенные так и гетерогенные системы.
Виды процессов массопередачи:
Абсорбция – поглощение газа жидкостью, обратный процесс- десорбция.
Экстракция (в системе жидкость-жидкость)- извлечение вещества, растворенного в жидкости, другой жидкостью, практически не смешивающейся с первой. Обратный процесс- реэкстракция.
Перегонка – разделение гомогенных жидких смесей путем взаимного обмена компонентами между жидкостью и паром, полученным испарением разделяемой смеси.
Адсорбция – поглощение компонента газа , пара или раствора твердым пористым поглотителем. Обратный процесс – десорбция.
Разновидностью адсорбции является ионный обмен – хемосорбция.
Сушка-удаление влаги из твердых материалов путем испарения.
Кристаллизация – выделение твердой фазы в виде кристаллов из растворов или расплавов.
Выщелачивание – переход твердой фазы в жидкую за счет избирательного растворения.
Массопередача включает в себя перенос вещества внутри одной фазы, перенос через поверхность раздела фаз и перенос в пределах другой фазы.
Массоперенос между фазами осуществляется до достижения равновесия , которое характеризуется равенством скоростей прямого и обратного процессов.
Фазовое равновесие на примере жидкостной экстракции
↓ ↓
Фазовое равновесие в жидкостной экстракции
Системы с взаимной нерастворимостью фаз
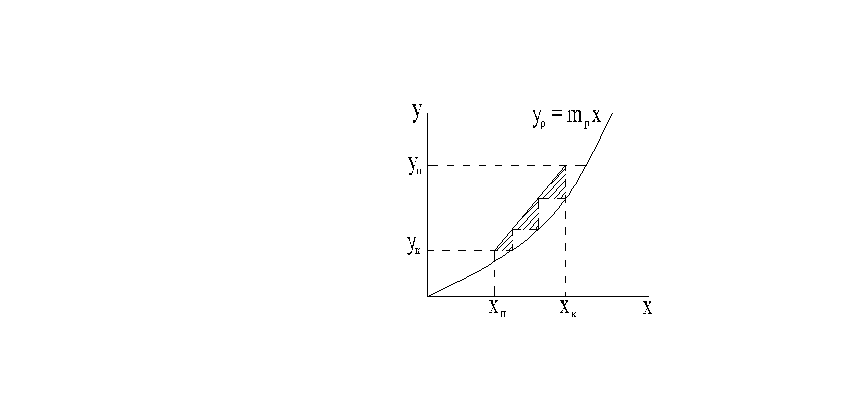
Равновесные кривые для системы вода-бензойная кислота-керосин

ур=mpх
mp- отношение равновесных концентраций переходного компонента (ПК) в экстракте и рафинате
Системы с частично взаимной разностью фаз.
Фазовое равновесие таких систем изображено в треугольной диаграмме
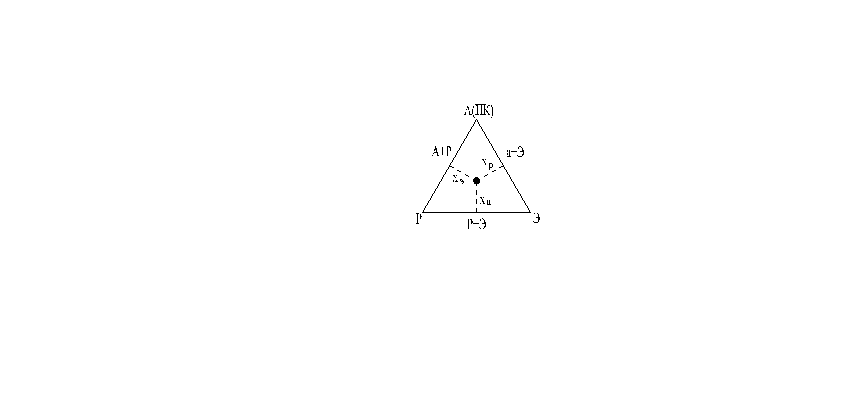
Вершины характеризуют индивидуальные компоненты
Стороны – бинарные смеси
М - тройная система , где хн+хр+хэ=1
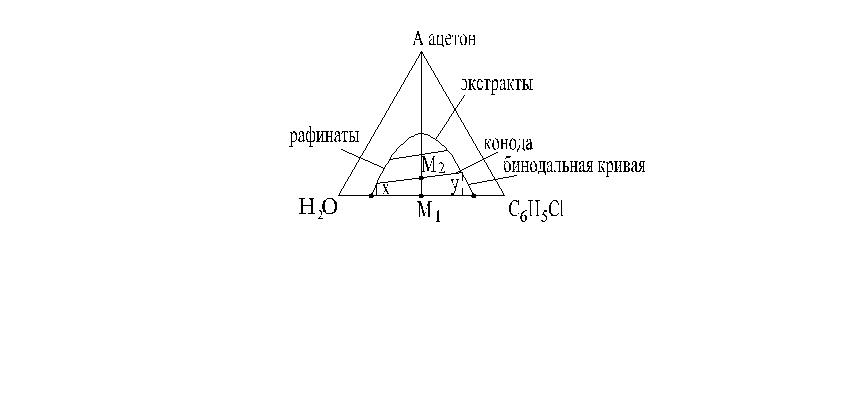
АМ1-смешение,
конода-линия равновесных концентраций, mp=у/х;
бинода- линия расслаивания, делит треугольник на 2 области – гомогенных растворов I и гетерогенной области – область расслаивания
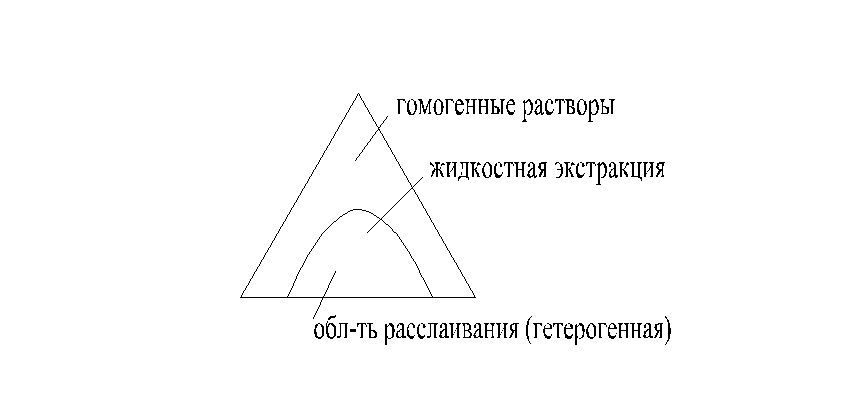
Внешнее давление не влияет на фазовое равновесие при жидкостной экстракции (ЖЭ).

С ростом температуры уменьшается гетерогенная область, т.к. увеличивается взаимная разность фаз, t3>t2> t1 ,
Непрерывная противоточная экстракция при взаимной нерастворимости фаз.

Материальный баланс по потокам:
WхH+DУ=Wх+DуК
Линия, характеризующая изменение концентраций в процессе массообмена называется рабочей линией и описывается уравнением:
у=![]() (х-хн)+ук
– рабочая линия
(х-хн)+ук
– рабочая линия
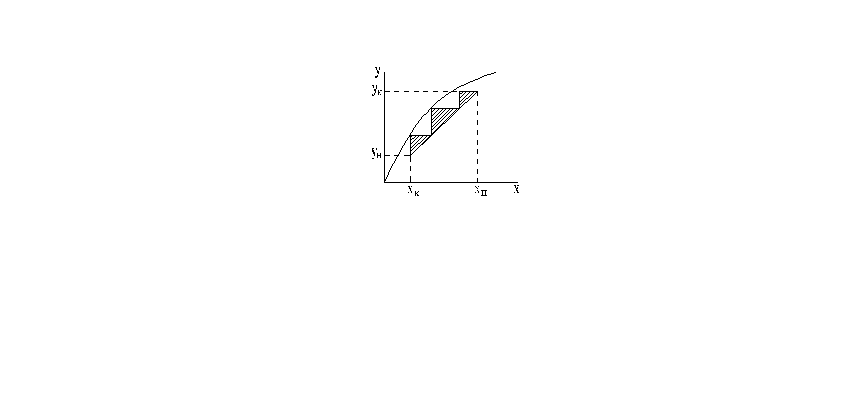
Процесс массообмена характеризуется равновесной и рабочей линиями, которые изображены на графике:
Адсорбция
Селективное поглощение твердых или жидких компонентов из жидкой и газовой среды с помощью твердых сорбентов называется адсорбцией. Адсорбция применяется при малых концентрациях извлекаемых веществ.
Требования к сорбентам:
Селективность.
Высокая емкость по поглощаемому компоненту
Легкость регенерации.
Прочность гранул сорбента.
Сорбенты –
высокопористые вещества, активная
поверхность пор достигает 100÷5000![]() ,
размер пор 20 А0.
,
размер пор 20 А0.
По характеру взаимодействия поглощающего компонента и сорбента различают физическую, химическую (хемосорбция) адсорбцию и капиллярную конденсацию.
При физической адсорбции возникает разность во взаимном притяжении молекул в объеме и на границе раздела фаз, проявляется за счет изменения сил Вандер-Ваальса.
Капиллярная конденсация – адсорбция из газовых, паровых сред
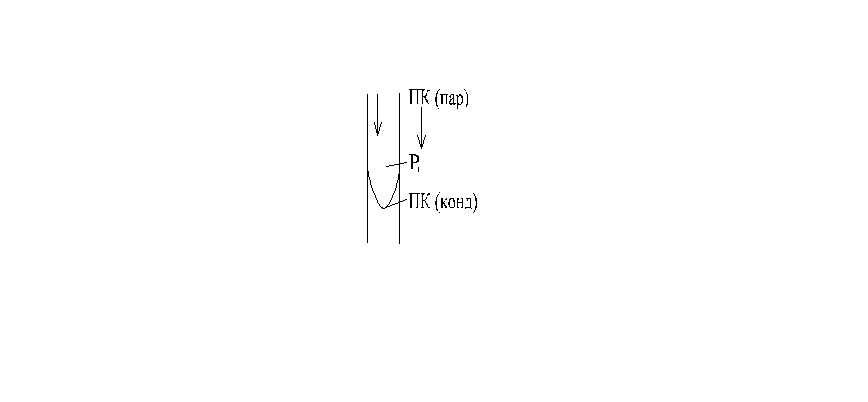
Промышленные сорбенты:
Активированные угли (АУ) , активная поверхность пор Sакт=600÷2000 м2/г
Селикагели (Si2O·nH2O)
Алюмогели [Al(OН)3+Al2O3] активная поверхность пор Sакт = 600 м2/г
Цеолиты – молекулярные сита, поглощают молекулы, размеры которых соответствуют размерам пор, характеризуются наибольшей селективностью.
Иониты – ионообменные смолы (хемосорбция)
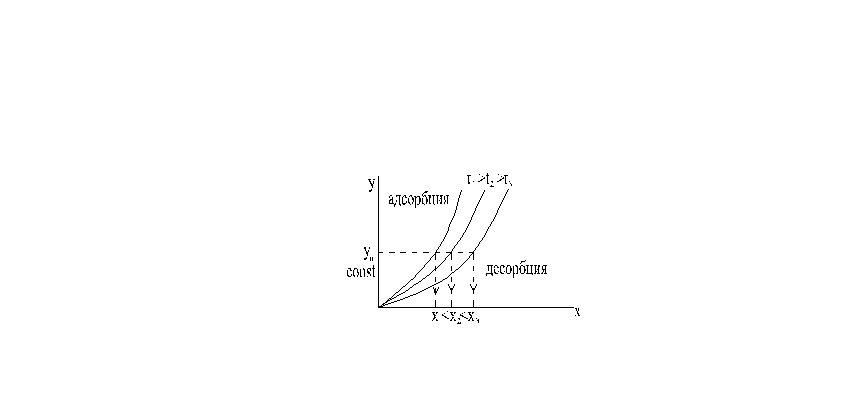
Фазовое равновесие при физической адсорбции
![]() -
равновесная концентрация в растворе;
-
равновесная концентрация в растворе;
х=[![]() ]
- равновесная концентрация на сорбенте;
]
- равновесная концентрация на сорбенте;
С ростом температуры поглощающая способность уменьшается.

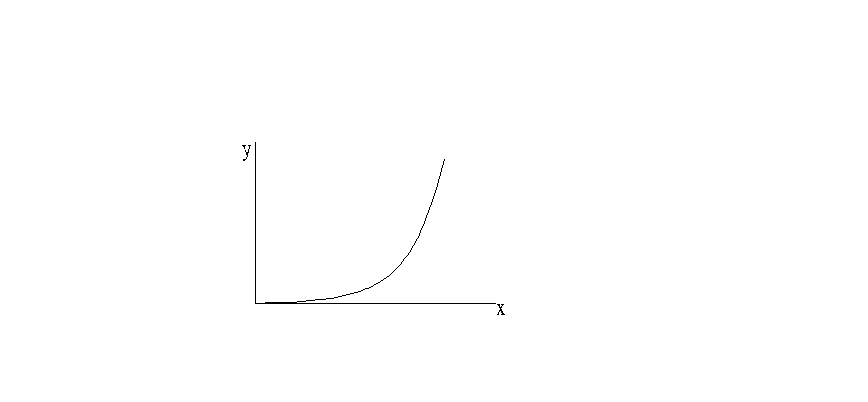
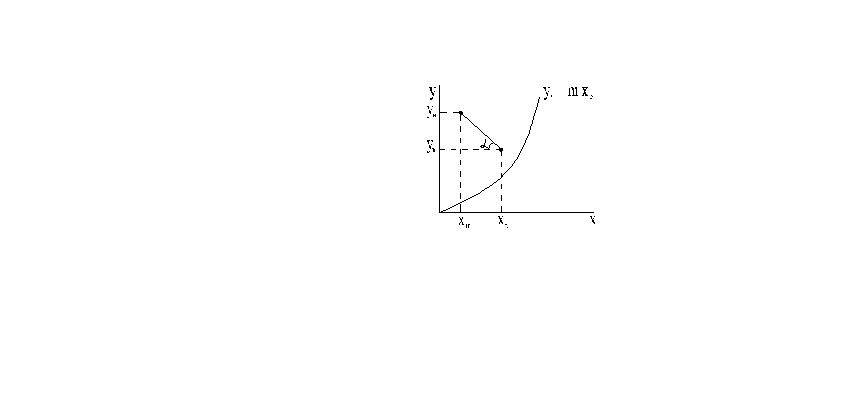
В области низких концентраций равновесные состояния описывает уравнение Фрейндлиха:
У=кХn ,
к и n – константы, которые могут быть определены экспериментально.
Изотермы сорбции приведены на рисунке:
При хемосорбции При капиллярной конденсации

Рабочие диаграммы процессов
Прямоток Противоток

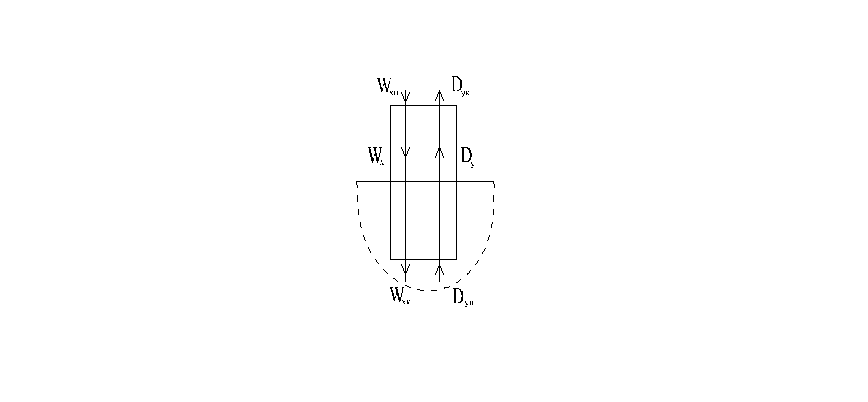
W, D – потоки инертов х, у – концентрации.
![]()
Матбаланс по переходному компоненту
![]()
![]()
![]()
![]()
Уравнение рабочей линии – геометрическое место сопряженных концентраций.
Сопряженные концентрации – концентрации переходного компонента в потоках, встречающихся в одном сечении аппарата
|
|
W=const D= const
|
|
D=const W= const
|
Совмещение линии равновесия и рабочей линии
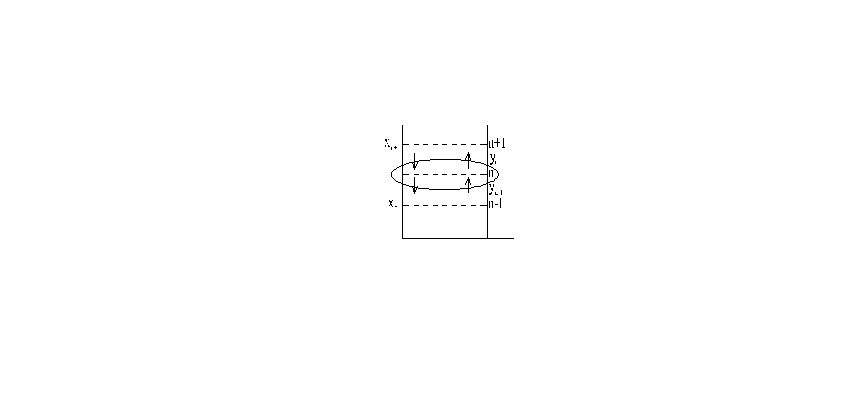
Эффективность массообменных процессов оценивается числом теоретических тарелок (ступеней)
Теоретическая
тарелка – гипотетическое устройство,
где
![]() или
или![]() ,
что приводит к достижению равновесия
,
что приводит к достижению равновесия
|
|
xnиyn– равновесие концентрации→линия равновесия.
|
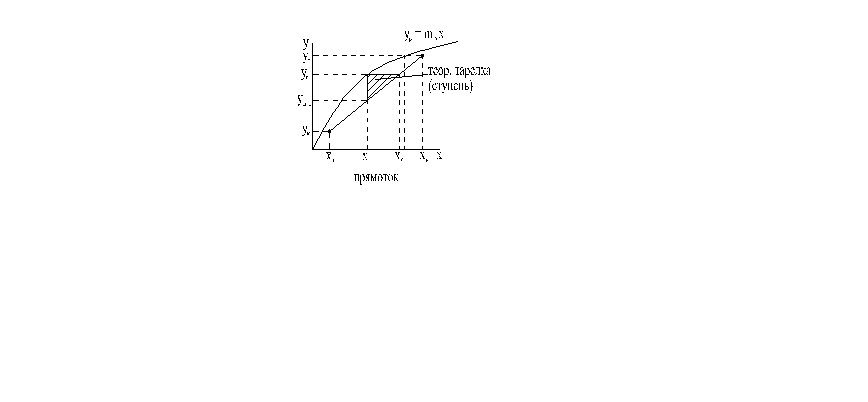 противоток
противоток
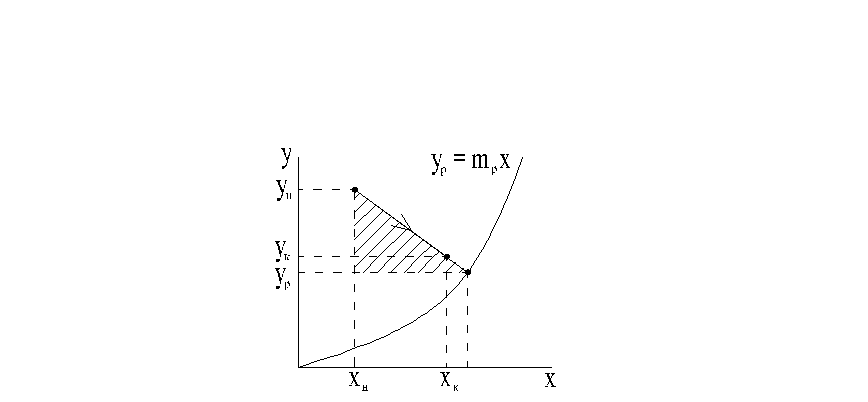
Для прямотока
О<Nтеор
![]() О<Nтеор
О<Nтеор
![]()
Число действ.
тарелок Ng=![]()
![]()
Число действительных тарелок определяется графическим методом, базируясь на реальную рабочую линию – построенную по реальному профилю концентраций .
Основное уравнение массопередачи
Количество вещества, которое переходит из одной фазы в другую в процессе массообмена пропорционально площади контакта, движущей силе и коэффициенту массопередачи.
М=Коу(Δу)срF= Кох(Δхср)F ,
где М – количество передаваемой массы, К коэффициенты массопередачи по фазе х или у; Δуср ; Δхср – движущие силы процесса, F- поверхность массообмена.
М=W(хН-хК)=D(yK-yH) – материальный баланс при массообмене
Коэффициенты массопередачи зависят от коэффициентов массоотдачи
Коу=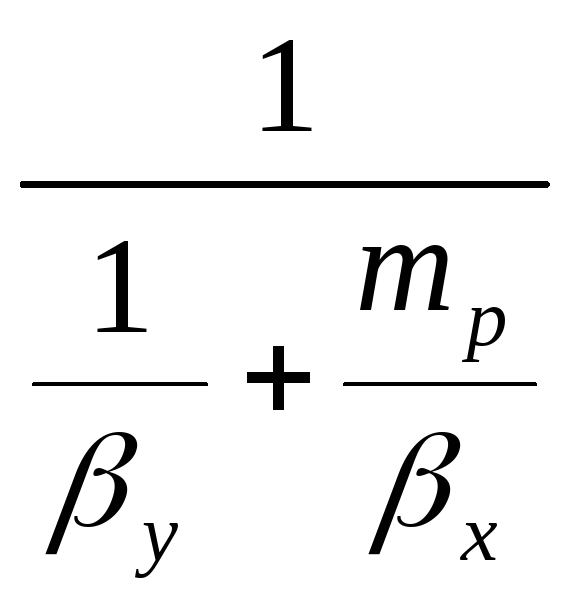 ;
;
Кох=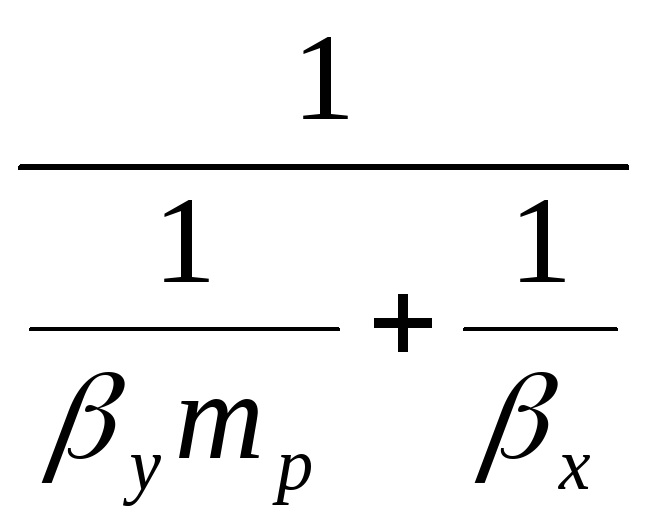
Частные коэффициенты
массоотдачи
![]() и
и![]() определяются на основе теории подобия
(моделирование массообменных процессов)
определяются на основе теории подобия
(моделирование массообменных процессов)
Средняя движущая сила массообменных процессов
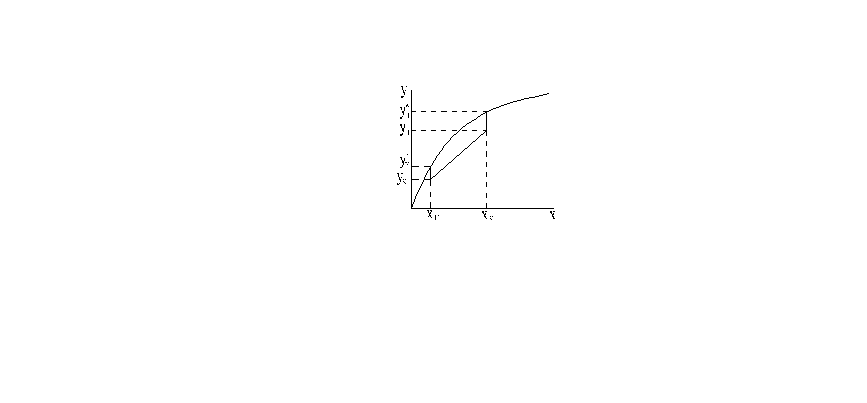
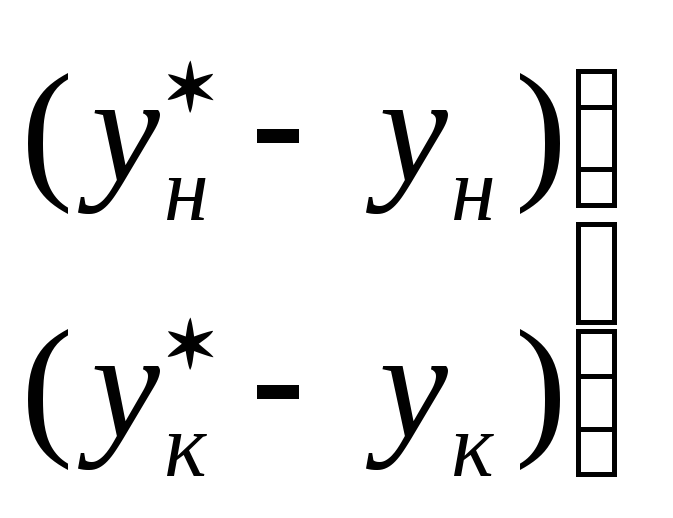 движущие
силы
движущие
силы
Локальные значения, меняются по длине и высоте аппарата
(Δу)ср=![]() mp
mp![]() const
const
(Δx)ср=![]()
Sx и Sу – число единиц переноса (ЧЕП)
Sу=![]()
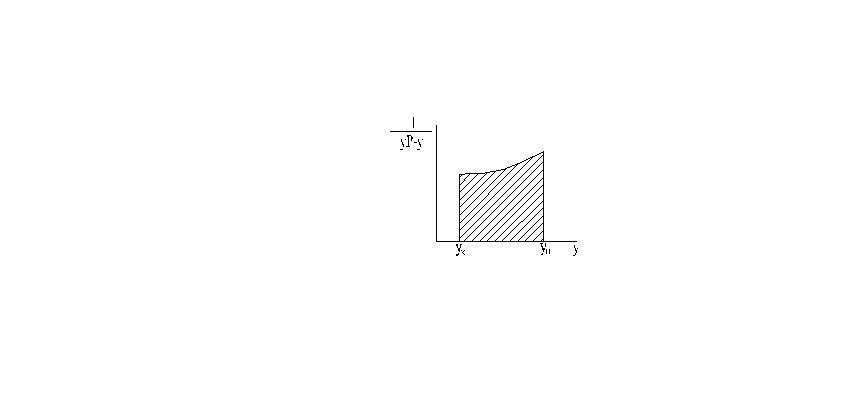
(Δу)ср=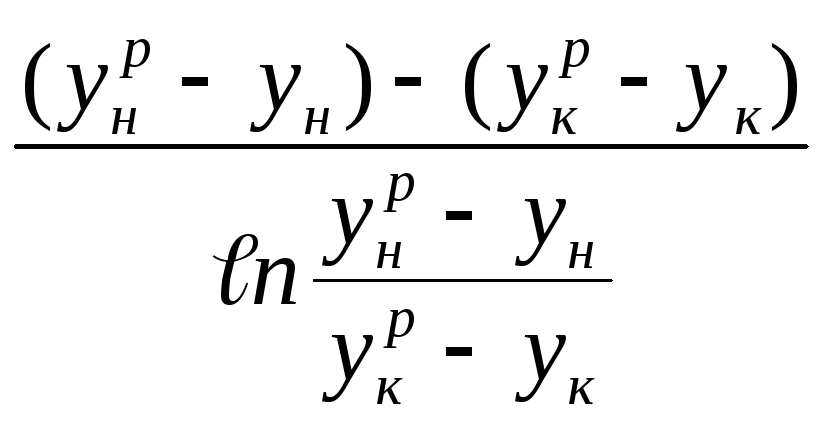 (Δx)ср=
(Δx)ср=
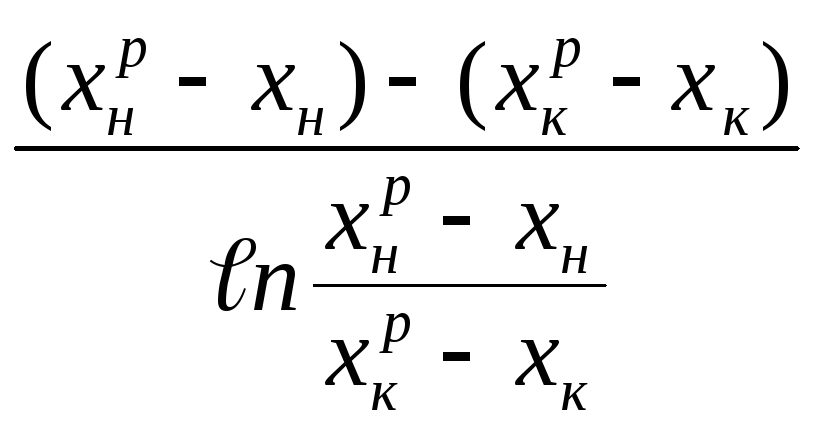



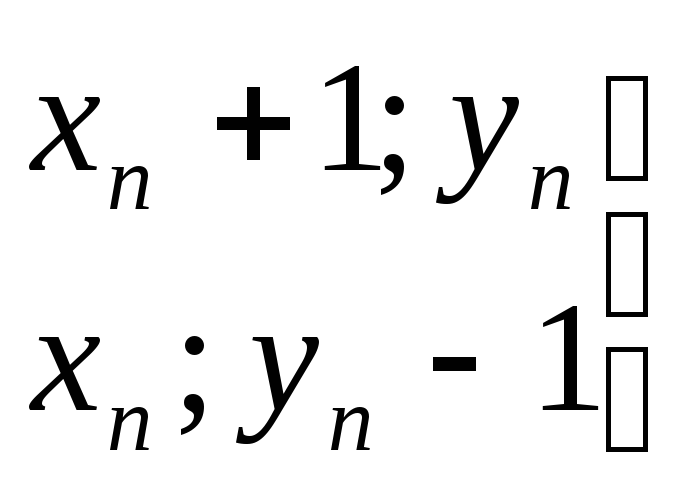 концентрации
потоков, встречающихся в одном сечении
концентрации
потоков, встречающихся в одном сечении