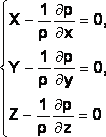- •Получение сернистого газа сжиганием серы, сероводорода и других видов сырья
- •Коксование каменных углей
- •Химические методы получения гидроксида натрия
- •Известковый метод
- •Ферритный метод
- •Электрохимические методы получения гидроксида натрия
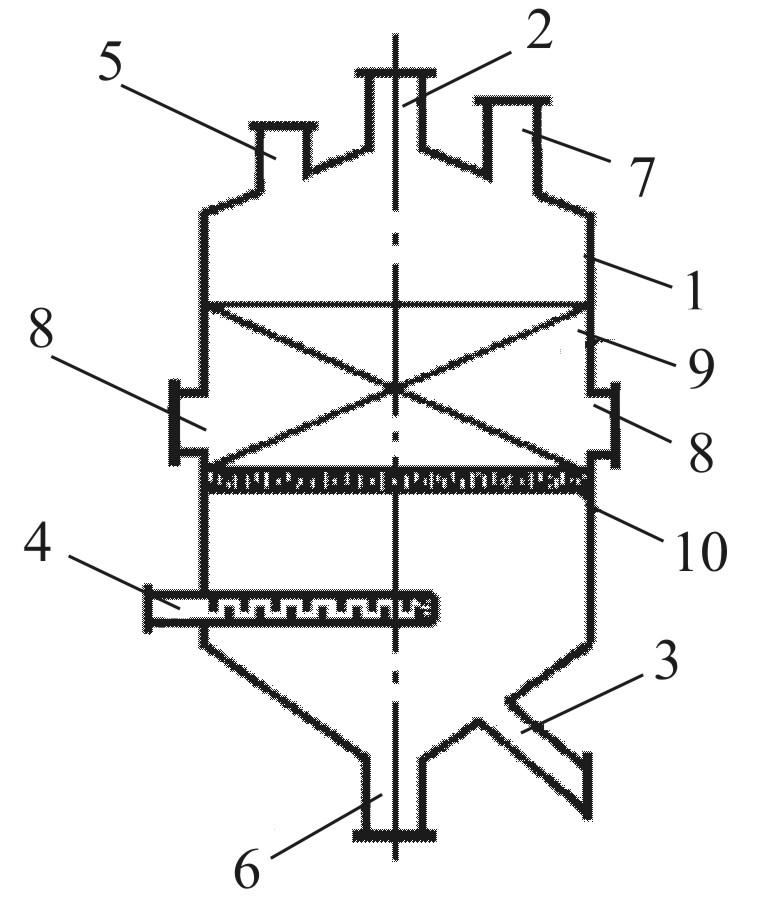
- •Контактный аппарат для окисления оксида серы(IV) в кипящем слое: 1 – выравнивающие решетки; 2 – катализатор; 3 – газораспределительные решетки; 4 – теплообменные элементы
- •Получение азота
- •13. Аммиак. Синтез аммиака.
- •14. Азотная кислота. Абсорбция нитрозных газов при атмосферном давлении.
- •15. Получение чугуна
- •16.Абсорбция серного ангидрида. Получение могогидрата и олеума
- •17. Получение этилена, ацетилена.
- •Получение пиролизом
- •20. Ректификация нефти.
- •23.Каталитический крекинг.
- •22. Выплавка стали.
- •24.Получение цемента сухим способом.
- •Производство цемента сухим способом
- •25. Технология получения соды.
- •26. Получение водорода из водяного пара
- •27. Получение стекла
- •28. Получение карбамида
- •29. Получение капролактама. Капрон.
- •9. Топливо. Электроэнергия.
- •10. Уравнение теплопроводности.
- •11. Уравнение Эйлера для гидродинамических условий.
- •12. Насосы. Компрессоры.
- •13. Сушка. Виды сушилок.
- •15. Теплообменники.
- •22. Ректификация. Ректификационная колонна.
- •21. Закон сохранения массы для любого разреза аппарата.
- •20. Выпарки. Упаривание методом противотока
- •19. Выпарки. Упаривание методом прямотока.
- •18. Экстракция. Экстракторы.
- •17. Уравнение Бернулли.
- •16. Критерии Рейнольдса.
28. Получение карбамида
Карбамид (мочевина) (NH2)2CO – наиболее ценное азотное удобрение. Карбамид применяется также в сельском хозяйстве в качестве подкормки для скота. В промышленности из него готовят карбамидные смолы, идущие на производство ценных пластмасс, древесностружечных плит, синтетических клеев, составов для пропитки тканей и др. Карбамид применяется в фармацевтической промышленности, при очистке нефтепродуктов, да я приготовления синтетического волокна урилона и т.п.
Сырьем для производства карбамида служат диоксид углерода и аммиак. Синтез карбамида протекает в две стадии. В первой стадии происходит образование карбаминово-кисло- го аммония (карбамата):
CO2 + 2NH3 ---> NH2 -- COONH4 + 150кДж
Затем карбамат дегидратируется с образованием карбамида:
NH2 -- COONH4 ---> CO (NH2)2 + H2O - 258 кДж
Суммарно получение карбамида представляет собой гетерогенный процесс в системе «Г – Ж», протекающий в кинетической области.

В промышленности синтез карбамида ведут при +180... 200 °С, давлении 20 МПа при 100%-м избытке аммиака. Этот синтез протекает в толстостенной колонне. В дистилляционной колонне от плава карбамида отгоняются избыточный аммиак и продукты разложения аммонийных солей угольной кислоты.
Раствор карбамида упаривают в выпарном аппарате, затем кристаллизуют в кристаллизаторах, отделяют кристаллы от маточного раствора на фильтровальном оборудовании или гранулируют в грануляционной башне. Газы после дистилляции направляются на регенерацию и дальнейшее использование для производства аммиачной селитры.
К жидким азотным удобрениям относятся либо растворы, содержащие аммиак в воде (аммиачная вода), либо растворы, включающие кроме аммиака аммиачную селитру или мочевину.
29. Получение капролактама. Капрон.
Капролактам представляет собой Белые кристаллы, хорошо растворимые в воде, спирте, эфире, бензоле. При нагревании в присутствии небольших количеств воды, спирта, аминов, органических кислот и некоторых других соединений капролактам полимеризуется с образованием полиамидной смолы, из которой получают волокно капрон. Важное свойство Капролактам - способность полимеризоваться с образованием ценного полимера - поликапроамида
Основное промышленное применение капролактама - производство полиамидных (нилоновых) волокон и нитей (полиамид 6). Кроме того, капролактам применяется в производстве инженерных пластиков, полиамидных пленок. В небольших количествах капролактам может использоваться в образовании полиуретана и синтезе лизина, жесткие текстильные подкладки, покрытия для пленок, синтетические кожи, пластификаторы, растворители для красок.
Технология производства капролактама
В промышленности капролактам получают из бензола, фенола или толуола по схемам:

В промышленности наибольшее распространение получил метод синтеза капролактама из бензола. Технологическая схема включает гидрирование бензола в циклогексан в присутствии Pt/Al2O3 или никель-хромового катализатора при 250-350 и 130-220 °С, соответственно. Жидкофазное окисление циклогексана в циклогексанон осуществляют при 140-160 °С, 0,9-1,1 МПа в присутствии нафтената или стеарата Со. Получающийся в результате окисления циклогексанол превращают в циклогексанон путем дегидрирования на цинк-хромовых (360-400 °С), цинк-железных (400 °С) или медь-магниевых (260-300 °С) смешанных катализаторах. Превращение в оксим проводят действием избытка водного раствора сульфата гидроксиламина в присутствии щелочи или NH3 при 0-100°С. Завершающая стадия синтеза капролактама. - обработка циклогексаноноксима олеумом или конц. H2SO4 при 60-120 °С (перегруппировка Бекмана). Выход капролактама в расчете на бензол 66-68%. При фотохимическом методе синтеза капролактама из бензола циклогексан подвергают фотохимическому нитрозированию в оксим под действием NOCl при УФ облучении. Метод синтеза капролактама из фенола включает гидрирование последнего в циклогексанол в газовой фазе над Pd/Al2O3 при 120-140 °С, 1-1,5 МПа, дегидрирование полученного продукта в циклогексанон и дальнейшую обработку как в методе синтеза из бензола. Выход 86-88%.
Метод синтеза капролактама из толуола включает: окисление толуола при 165°С в присутствии бензоата Со; гидрирование получающейся бензойной кислоты при 170°С, 1,4-1,5 МПа в присутствии 5%-ной взвеси Pd на мелкодисперсном угле; нитрозирование циклогексанкарбоновой кислоты под действием нитрозилгидросульфата (нитрозилсерной к-ты) при 75 80 °С до капролактама-сырца. Некоторые стадии этой схемы недостаточно селективны, что приводит к необходимости сложной очистки получаемого капролактама. Выход капролактама 71% в расчете на исходный продукт.
Полученный любым из перечисленных методов капролактам предварительно очищают с помощью ионообменных смол, NaClO и КМnО4, а затем перегоняют. Побочный продукт производсства (NH4)2SO4 (2,5-5,2 т на 1 т К.), который используется в сельском хозяйстве в качестве минерального удобрения. Известны также методы получения капролактама из неароматического сырья (фурфурола, ацетилена, бутадиена, этиленоксида), которые не нашли промышленного применения.
Твердый капролактам транспортируют в бумажных пятислойных мешках с полиэтиленовым вкладышем, жидкий - в специально оборудованных цистернах с обогревом в атмосфере азота (содержание кислорода в азоте не должно превышать 0,0005%). Температура воспламенения - 135°С, т. самовоспламенения - 400 °С, нижний предел воспламенения 123°С; ЛД50 450 мг/м3 (мыши, вдыхание паров), ПДК 10 мг/м3.
В мире капролактам получают преимущественно из бензола - 83,6%, из фенола - 12%, из толуола - 4,4%.
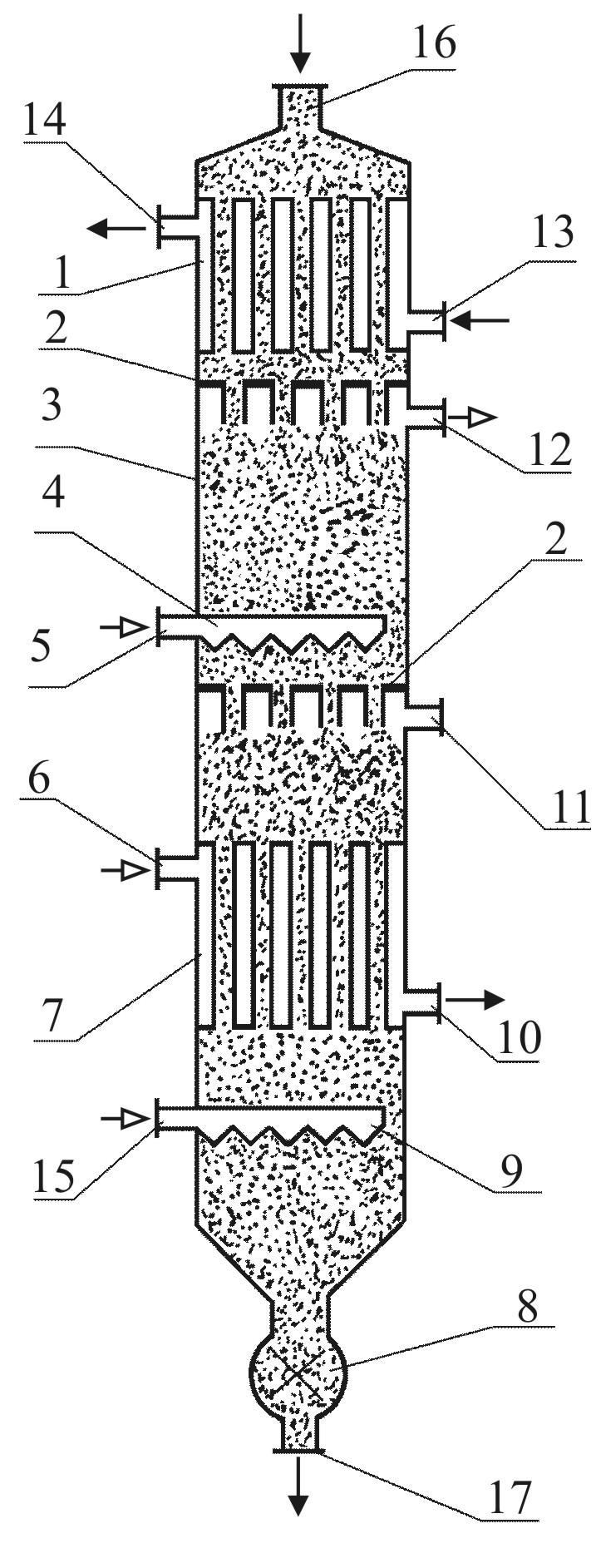
Для получения капрона сначала при пониженных давлении и температуре фенолпутёмгидрированияпревращают вциклогексанон. Другим, принципиально отличным методом получения циклогексанона стал разработанный позже фенольного процессгидрированияи последующегоокислениябензола. Затем циклогексанон действиемгидроксиламинапереводят в оксим циклогексанона (1→2 на рисунке ниже), а из него в ходе бекмановской перегруппировки под действиемсерной кислотыполучаюткапролактам(2→3 на рисунке):
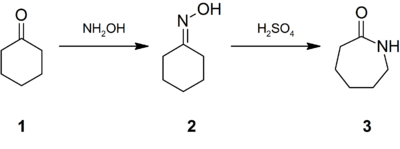
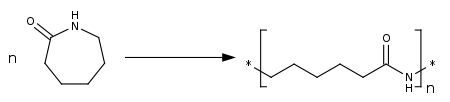
Синтез поликапролактама (то есть капрона) проводится гидролитической полимеризацией расплава капролактама по механизму «раскрытие цикла — присоединение»:
Химическая технология.
Химическая технология - это наука о наиболее экономичных способах и средствах массовой переработки природного сырья в продукты потребления и/или промежуточные продукты, применяемые в различных областях материального производства.
Формирование химической технологии как отдельной науки вызвано особенностями материального производства, например:
– стремительные темпы роста и постоянно меняющийся характер промышленного производства;
– многообразие ассортимента химической продукции и технологических процессов их получения;
– разработка научной классификации и создание теоретических основ химических процессов.
Современное химическое производство перерабатывает огромные объемы сырья с использованием большого количества энергии различных видов и огромных капитальных затрат.
Поэтому одно из главных требований к современному производству – экономичность. Эту особенность химической технологии четко определил еще Д. И. Менделеев.
Химическая технология не может быть сведена только к методам химической переработки, т.к. в химическом производстве химическим превращениям сопутствуют разнообразные физические, физико-химические и механические процессы.
Химическая технология – это наука, изучающая такие производственные процессы переработки, которые хотя бы на одной стадии связаны с изменением состава, строения и свойств веществ, т.е. с превращением их в другие вещества.
Т.е. Химическая технология – это наука о химическом производстве. Химическое производство – это сложное производство, в котором можно выделять уровни протекания процесса:
– молекулярный уровень, на котором механизм химических превращений описывается как взаимодействие молекул (микрокинетика);
– уровень малого объема, на котором явления описываются как взаимодействие частиц (гранул, капель, пузырьков газа, зерен катализатора и т.д.). Для анализа явлений на этом уровне и описания процесса применяется понятие «макрокинетика», задачей которой является изучение влияния на скорость процесса химического превращения при переносе масс исходных и конечных продуктов, процесса массопередачи и влияния состояния катализатора.
– уровень потока, на котором описание явлений дается как взаимодействие совокупности частиц, с учетом характера их движения в потоке (ламинарное, переходное, турбулентное) и изменения температуры и концентрации реагентов по фронту потока;
– уровень реактора, на котором описание явлений дается с учетом конструкции аппарата (реактора), в котором реализуется технологический процесс.
Химическая технология базируется на материале целого ряда наук: инженерных и химических, математике, физике, механике, гидродинамике, минералогии и др.
В то же время сама химическая технология составляет основу экономических наук, изучающих химическую технологию, ее данные используют при изучении экологических проблем, научно-инженерной этики и т. д.
Абсорбция. Абсорбционные аппараты
Абсорбция процесс избирательного поглощения компонентов газовой смеси жидким поглотителем (абсорбентом) Т.е. растворение (или поглощение) газов жидкостями.
Процесс абсорбции происходит если парциальное давление извлекаемого компонента в газовой смеси Рг выше, чем в жидком абсорбенте Рж, т.е. для протекания абсорбции необходимо, чтобы газ и абсорбент не находились в состоянии равновесия. Разность этих давлений – это движущая сила ΔР, под действием которой происходит поглощение (абсорбция) данного компонента жидкой фазой из газовой фазы. Чем больше движущая сила, тем интенсивнее переходит этот компонент из газовой фазы в жидкую. Т.о., при ΔР>0 происходит абсорбция, при ΔР<0 – десорбция, при Рж=Рг система достигает равновесия и процесс прекращается.
Различают два вида абсорбции: физическую, при которой извлечение компонентов из газа происходит благодаря их растворимости в абсорбентах и химическую (хемосорбцию), основанную на химическом взаимодействии извлекаемых компонентов с активной частью абсорбента. Скорость физической абсорбции определяется диффузионными процессами, скорость хемосорбции зависит от скорости диффузии и химической реакции.
Поглощение компонентов газовой смеси при абсорбции сопровождается выделением тепла, величина которого пропорциональна массе и теплоте растворения qA поглощенных компонентов.
Процесс абсорбции обратимый, поэтому он используется не только для получения растворов газов в жидкостях, но и для разделения газовых смесей. При этом после поглощения одного или нескольких компонентов газа из газовой смеси необходимо произвести выделение из абсорбента поглощенных компонентов, т.е. десорбцию.
При выборе абсорбента учитывают состав разделяемого газа, давление и температуру процесса, производительность установки. Выбор абсорбента определяется также его селективностью, поглотительной способностью, коррозионной активностью, стоимостью, токсичностью и другими факторами.
Например, в нефтяной и газовой промышленности процесс абсорбции применяется для разделения, осушки и очистки углеводородных газов. Из природных и попутных нефтяных газов путем абсорбции извлекают этан, пропан, бутан и компоненты бензина; абсорбцию применяют для очистки природных газов от кислых компонентов — сероводорода, используемого для производства серы, диоксида углерода, серооксида углерода, сероуглерода, тиолов (меркаптанов) и т.п.
Процессы абсорбции и десорбции обычно осуществляют на одной установке, включающей абсорбер и десорбер.

схема абсорбционно-десорбционной установки:
/ — абсорбер; 2 — холодильник; 3 — подогреватель; 4 — десорбер; 5 — конденсатор; 6 — емкость; 7 — теплообменник. Потоки: I — сырой газ; II — сухой (тощий) газ; III — насыщенный абсорбент; IV — регенерированный абсорбент; V — извлеченные компоненты; V7 — несконденсированные газовые компоненты; VII — жидкий продукт.
При абсорбционных процессах массообмен происходит на поверхности соприкосновения фаз. Поэтому абсорбционные аппараты должны иметь развитую поверхность соприкосновения между газом и жидкостью. Исходя из этого, абсорбционные аппараты можно подразделить на следующие группы:
а) Поверхностные абсорберы, в которых поверхностью контакта между фазами создается за счет фиксированной поверхности, например зеркало жидкости (собственно поверхностные абсорберы) или поверхность текущей пленки жидкости (пленочные абсорберы). К этой же группе относятся насадочные абсорберы, в которых жидкость стекает по поверхности загруженной в абсорбер насадки из тел различной формы (кольца., кусковой материал и т. д.), и механические пленочные абсорберы. Для поверхностных абсорберов поверхность контакта в известной степени определяется геометрической поверхностью элементов абсорбера (например, насадки), хотя во многих случаях и не равна ей.

Схемы насадочных абсорберов:
а - со сплошным слоем насадки; б - с секционной загрузкой насадки: 1 - корпус; 2 - распределитель жидкости; 3 - насадка; 4 -опорные решетки; 5 - перераспределитель жидкости; 6 - гидравлические затворы; в - эмульгационная насадочная колонна: 1 - насадка; 2 - сетка, фиксирующая насадку; 3 - гидравлический затвор; 4 - опорная решетка; 5 - распределитель газа.
Виды насадок: седловидная, кольцевая, спиральная.
б) Барботажные абсорберы, в которых поверхность контакта развивается потоками газа, распределяющегося в жидкости в виде пузырьков и струек. Тaкое движение газа (барботаж) осуществляется путем пропускания его через заполненный жидкостью аппарат (сплошной барботаж) либо в аппаратах колонного типа с колпачковыми, ситчатыми или провальными тарелками. Подобный характер взаимодействия газа и жидкости наблюдается также в насадочных абсорберах с затопленной насадкой. В эту же группу входят барботажные абсорберы с перемешиванием жидкости механическими мешалками. В барботажных абсорберах поверхность контакта определяется гидродинамическим режимом (расходами газа и жидкости).
в) Распыливающие абсорберы, в которых поверхность контакта образуется путем распыления жидкости в массе газа на мелкие капли. Поверхность контакта определяется гидродинамическим режимом (расходом жидкости). К этой группе относятся абсорберы, в которых распыление жидкости производится форсунками (форсуночные, или полые, абсорберы), в токе движущегося с большой скоростью газа (скоростные прямоточные распыливающие абсорберы) или вращающимися механическими устройствами (механические распыливающие абсорберы).
Уравнение Эйлера для гидростатических условий.
Одно из основных уравнений гидродинамики идеальной жидкости.
Система уравнений Эйлера (уравнения равновесия) определяет закон распределения давления в покоящейся жидкости вдоль соответствующей оси координат.
|
|
здесь X,Y,Z – напряжения массовых сил в проекциях на соответствующие оси координат x, y, z, p – давление в соответствующей точке жидкости, ρ - плотность жидкости.
|
Из уравнений Эйлера можно получить следующий вид основного дифференциального уравнения равновесия жидкости:dP=P(Xdx+Ydy+Zdz)
Если ввести силовую (потенциальную) функцию U, такую, что X=ðU/ðx; Y=ðU/ ðy; Z= ðU/ ðz, то для несжимаемой жидкости дифференциальное уравнение равновесия примет вид: d(P/ρ)=dU
Основное уравнение гидростатики. В однородном поле силы тяжести при постоянстве плотности жидкости: dU=gdz, тогда dp= – ρgdz,
Проинтегрировав, получим основное уравнение гидростатики: p=p0+ρgh, где h=(z0-z) - расстояние по вертикали между рассматриваемыми двумя точками (нулевой и точкой, в которой определяется давление).
Вода. Очистка воды
Вода – наиболее распространенное вещество на Земле. Можно выделить следующие виды воды: атмосферная, наземная, подземная. При этом основная масса воды сосредоточена в мировом океане, и это соленая вода, которая для промышленности практически не пригодна без опреснения. При этом почти 99 % пресной воды – это подземные воды и ледники вместе со снежным покровом.
Химическое производство – одно из крупнейших потребителей воды. Это объясняется рядом достоинств воды, например:
– наличие комплекса ценных физических свойств (высокая теплоемкость, малая вязкость, низкая температура кипения и др.);
– доступность и дешевизна;
– нетоксичность;
– удобство транспортировки и использования в производстве.
В химической промышленности вода используется в следующих направлениях.
1. Для технологических целей в качестве:
– растворителя, среды для проведения некоторых физических и механических процессов;
– промывной жидкости для газов;
– экстрагента и абсорбента;
– для перекристаллизации;
– для флотации;
– катализатора или инициатора каталитического процесса.
2. В качестве теплоносителя в виде горячей воды и перегретого водяного пара и хладоагента.
3. В качестве сырья или реагента для производства разнообразной химической продукции.
Объемы потребления воды химическим производством зависят от типа производимой продукции и колеблются в широких пределах.
Основные показатели качества воды для химической технологии. Вода, используемая в хим. промышленности, должна удовлетворять по качеству определенным требованиям. Оно определяется совокупностью физических и химических характеристик: жесткость, окисляемость, рН, доля примесей.
Жесткость – это свойство воды, связанное с присутствием в ней растворенных солей кальция и магния. Жесткость (Жо) характеризуют концентрацией ионов Са2+ и Mg2+ и измеряют в миллимолях на литр воды. По значению Жо вода бывает мягкой (Жо< 2), средней жесткости (Жо = 2–10) и жесткой (Жо >10).
Окисляемостью называют свойство воды, связанное с присутствием в воде неорганических веществ, легкоокисляющихся соединений железа и сероводорода, способных окисляться различными окислителями, и измеряется количеством КМпО4 или эквивалентным количеством кислорода, затраченным на окисление 1 л воды, т.е. миллиграмм на литр (мг/л).
Активная реакция воды характеризует ее кислотность или щелочность (рН). Она определяется присутствием в воде некоторых газов: хлор, оксид углерода (II), гидрокарбонатов, силикатов, реже карбонатов и других, а также растворимых гуминовых кислот и веществ, вносимых в водоем промышленными стоками. Большинство природных вод имеют рН = 6,5–8.
Примеси в природных и сточных водах присутствуют во взвешенном, коллоидном или растворенном состоянии. Примеси во взвешенном состоянии – это эмульсии или суспензии. Они кинетически неустойчивы. Примеси в коллоидном состоянии – это гидрофильные и гидрофобные минеральные и органические коллоидные частицы.
Промышленная водоподготовка(очистка воды). Это комплекс мероприятий по улучшению качества воды для технологических целей. В нее включают операции по удалению механических примесей, умягчению, осветлению и дегазации.
Осветление – это отстаивание воды с последующей фильтрацией через зернистый материал. Для коагуляции коллоидных примесей и абсорбции окрашенных частиц к ней добавляют электролиты – сульфаты Al или Fe.
Обеззараживание воды проводят хлором или озоном.
Дегазацию (удаление из воды растворенных газов) ведут химическим способом, при котором газы поглощаются химическими реагентами (например, в случае диоксида углерода или сероводорода воду обрабатывают моноэтаноламином или раствором гашеной извести). Применяют также физические методы, например термическую деаэрацию на воздухе либо в вакууме.
Обессоливание применяют в тех производствах, где предъявляются повышенные требования к товарным продуктам на содержание различных металлов, имеющихся в воде. Обессоливание ведут ионным обменом, дистилляцией, электродиализом.
Перемешивание. Мешалки.
Перемешивание - один из самых распространенных процессов на предприятиях пищевой и химической промышленности. При перемешивании частицы жидкости или сыпучего материала многократно перемещаются в объеме аппарата или емкости друг относительно друга под действием импульса, который передается перемешиваемой среде от механической мешалки или струи жидкости, газа или пара.
Цели перемешивания:
1.ускорение течения химических реакций или процессов;
2.обеспечение равномерного распределения твердых частиц в жидкости;
3.обеспечение равномерного распределения жидкости в жидкости;
4.интенсификация нагревания или охлаждения;
5.обеспечение стабильной температуры по всей жидкости.
При подборе перемешивающего устройства или способа перемешивания используются следующие основные понятия:
Степень перемешивания или степень взаимного распределения двух или более веществ или жидкостей после окончания перемешивания всей системы. Степень перемешивания, иногда называемая показателем однородности, определяется опытным путем на основании взятых проб и используется для определения эффективности перемешивания.
Интенсивность перемешивания, выражаемая с помощью определенных величин, таких как частота вращения мешалки, расходуемая на перемешивание мощность, приведенная к единице объема или плотности продукта.
Эффективность перемешивания, определяемая возможностью достижения требуемого качества перемешивания за кратчайшее время и с минимальными затратами энергии.
Известны несколько видов перемешивания: механическое; циркуляционное; барботажное.
Барботажное перемешивание осуществляется путем барботажа инертного газа или газообразных веществ через жидкость.
Циркуляционное перемешивание происходит за счет больших скоростей движения (насосом).
Механическое перемешивание в жидкой среде, а также в вязких материалах осуществляется с помощью мешалок, которые по конструктивной форме, в зависимости от устройства лопастей, разделяются на: 1) лопастные; 2) листовые; 3) якорные; 4) рамные; 5) турбинные; 6) пропеллерные; 7) специальные.
Все они состоят из трех основных частей: вала, на котором закреплена мешалка; мешалки, являющейся рабочим элементом; и привода, с помощью которого вал приводится в движение за счет механической энергии.
В зависимости от числа оборотов мешалки условно делят на тихоходные и быстроходные. К тихоходным относят лопастные, рамные, якорные и листовые, имеющие скорость более 80—100 об/мин. К быстроходным — турбинные и пропеллерные.
При выборе типа мешалки и ее параметров учитывают требования технологического процесса, свойства жидкости, наличие осадков, форму аппарата и другие факторы.
Лопастные мешалки. Наиболее простыми по устройству являются мешалки с плоскими лопастями из полосовой или угловой стали, установленными перпендикулярно или наклонно к направлению их движения. Это механизм, состоящий из двух и более числа лопастей, прямоугольной формы. Импеллер с лопастями крепится на вращающемся валу, вертикальном или наклонном. К лопастным мешалкам специального назначения так же относятся рамные (якорные) и листовые мешалки. Среди основных достоинств мешалок лопастного типа следует назвать относительно небольшую стоимость изготовления и несложность конструкции, удобство и простоту в обслуживании. Частота кружения подобных мешалок колеблется от 18 до 80 об/мин; при повышении частоты вращения выше указанной результативность перемешивания резко уменьшается и растет расход энергии.
Недостаток лопастных мешалок – это слабый осевой поток, который не обеспечивает полного перемешивания всего объема жидкости в емкости или аппарате. Из-за незначительного создания осевого потока, лопастная мешалка перемешивает в основном те слои жидкости, которые расположены вблизи от лопастей мешалки. В объеме перемешиваемой жидкости развитие турбулентности происходит медленно и циркуляция жидкости невелика. Поэтому лопастные мешалки рекомендуется использовать для перемешивания низковязких жидкостей до 100 сПз, они непригодны для перемешивания легко расслаивающихся веществ.
Рамные мешалки. Они представляют собой комбинацию лопастных мешалок с вертикальными и наклонными лопастями. Эти мешалки применяются в тех же случаях, что и лопастные, а также при перемешивании значительных объемов вязких материалов. Поэтому диаметр ее максимально приближен к диаметру сосуда, что позволяет захватывать при смешивании оседающие осадочные частицы, не допускает залипания на стенках и перегрева жидкости. Если в процессе производства возникает необходимость в перемешивании менее вязкой жидкости, то рамная мешалка легко превращается в якорную мешалку методом исключения из конструкции поперечных элементов.
Пропеллерные мешалки. Рабочей частью пропеллерной мешалки является пропеллер - устройство с несколькими фасонными лопастями, изогнутыми по профилю гребного винта. Наибольшее распространение получили трехлопастные пропеллеры. На валу мешалки, который может быть расположен вертикально, горизонтально или наклонно, в зависимости от высоты слоя жидкости устанавливают один или несколько пропеллеров. Пропеллерные мешалки создают преимущественно осевые потоки перемешиваемой среды и, как следствие этого,- большой насосный эффект, что позволяет существенно сократить продолжительность перемешивания.

 1-лопастная.
2-рамная
1-лопастная.
2-рамная
Адсорбция. Адсорбционные аппараты.
Адсорбцией называют избирательное поглощение одного или нескольких компонентов из газовых или жидких сред твердым поглотителем - адсорбентом. Поглощаемый компонент, содержащийся в сплошной среде (газе, жидкости), назывют адсорбтивом, а содержащийся в сорбенте - адсорбатом.
Адсорбцию газов и паров применяют для глубокой осушки природных газов, воздуха, газовых потоков в каталитических процессах, а также в неорганическом и основном органическом синтезах для выделения компонентов с высокой степенью чистоты, для очистки вентиляционных выбросов от вредных или ценных компонентов и в других производствах. Адсорбцию компонентов из жидких сред применяют для извлечения (рекуперации) растворителей, а также для очистки сточных вод.
Различают физическую адсорбцию и сорбцию, основанную на силах химического взаимодействия (хемосорбцию). Физическая адсорбция обусловлена силами межмолекулярного взаимодействия. Хемосорбционный процесс - это химический процесс, протекающий на поверхности раздела фаз. В отличие от физической адсорбции при хемосорбции не сохраняется индивидуальность адсорбтива и адсорбента. При сближении молекул адсорбтива с поверхностью адсорбента происходит перераспределение их электронов с образованием химической связи.
После проведения адсорбции, как правило, осуществляют десорбцию адсорбата. Это позволяет извлечь из адсорбента поглощенный компонент, который часто представляет собой целевой продукт, и снова использовать освобожденный от него адсорбент. Промышленный адсорбент часто используется многократно. После десорбции, как правило, проводят активацию адсорбента, чтобы восстановить его адсорбционные свойства.
Аппараты, в которых осуществляется процесс адсорбции, называются адсорберами. По состоянию слоя адсорбента в аппарате адсорберы можно разделить на три группы: 1 – адсорберы с неподвижным слоем адсорбента (аппараты периодического действия); 2 – адсорберы с псевдоожиженным слоем адсорбента; 3 – адсорберы с движущимся плотным слоем адсорбента. Последние две группы относятся к аппаратам непрерывного действия.
Адсорбер периодического действия с неподвижным слоем адсорбента.
|
|
1.корпус 2 3 4 5 6 7 8 9 10
|
Периодические процессы часто осуществляют в четыре стадии.
Первая
стадия ![]() собственно
адсорбция, т.е. насыщение адсорбента
поглощаемым компонентом. Исходная
газовая смесь подается в корпус 1 аппарата
через штуцер 2, проходит через слой
адсорбента 9 и очищенные газы выходят
через штуцер 3.
собственно
адсорбция, т.е. насыщение адсорбента
поглощаемым компонентом. Исходная
газовая смесь подается в корпус 1 аппарата
через штуцер 2, проходит через слой
адсорбента 9 и очищенные газы выходят
через штуцер 3.
Вторая
стадия ![]() десорбция
поглощенного компонента из адсорбента.
Подача исходной смеси газов прекращается,
и в аппарат подается водяной пар через
барботер 4. Смесь паров десорбированного
компонента и воды удаляется через штуцер
5. Конденсат водяного пара отводится из
аппарата после десорбции через штуцер
6.
десорбция
поглощенного компонента из адсорбента.
Подача исходной смеси газов прекращается,
и в аппарат подается водяной пар через
барботер 4. Смесь паров десорбированного
компонента и воды удаляется через штуцер
5. Конденсат водяного пара отводится из
аппарата после десорбции через штуцер
6.
Третья
стадия ![]() сушка
адсорбента. Перекрывается вход и выход
водяного пара, после чего влажный
адсорбент сушится горячим воздухом,
поступающим в аппарат через штуцер 2 и
выходящим из аппарата через штуцер 3.
сушка
адсорбента. Перекрывается вход и выход
водяного пара, после чего влажный
адсорбент сушится горячим воздухом,
поступающим в аппарат через штуцер 2 и
выходящим из аппарата через штуцер 3.
Четвертая
стадия ![]() охлаждение
адсорбента. Прекращается подача горячего
воздуха, после чего адсорбент охлаждается
холодным воздухом, поступающим в аппарат
через штуцер 2 и выходящим через штуцер
3.
охлаждение
адсорбента. Прекращается подача горячего
воздуха, после чего адсорбент охлаждается
холодным воздухом, поступающим в аппарат
через штуцер 2 и выходящим через штуцер
3.
По окончании четвертой стадии цикл работы аппарата начинается снова со стадии адсорбции. Загрузку и выгрузку адсорбента производят периодически через люки 7 и 8.
Адсорбер с псевдоожиженным слоем адсорбента.
|
|
Адсорбер с псевдо-ожиженным слоем адсорбента: 1 – корпус; 2 –газораспределительная решетка; 3 – сепаратор; 4 – штуцер для отвода очищенных газов; 5 – штуцер для подвода исходной газовой смеси; 6 – труба для подвода свежего адсорбента; 7 – труба для отвода отработанного адсорбента; 8 – псевдоожиженный слой адсорбента.
|
Исходная газовая смесь поступает в аппарат через штуцер 5, проходит через газораспределительную решетку 2 и создает псевдоожиженный слой (разд. 5.5.5) адсорбента 8. Адсорбент поглощает из газовой смеси адсорбтив, а очищенные газы входят в сепаратор 3, где очищаются от уносимых потоком газа частиц адсорбента, далее очищенные газы выходят из аппарата через штуцер 4. В аппарат непрерывно подается свежий адсорбент по трубе 6 и непрерывно из него отводится отработанный адсорбент по трубе 7. В случае, если заданной степени очистки в одном аппарате достигнуть нельзя, то устанавливается последовательно несколько аппаратов либо используются многоступенчатые адсорберы.
|
|
Адсорбер с движущимся плотным слоем адсорбента: 1 2 – распределительные тарелки; 3 4 – распределительное устройство для исходной газовой смеси; 5 6,10 7 8 – затвор-отводник адсорбента; 9 – распределительное устройство для острого водяного пара; 11 12 13,
14 15 – патрубок для ввода острого водяного пара; 16 17
|
Распределительные тарелки в адсорбере служат для равномерного распределения адсорбента по поперечному сечению аппарата и препятствуют переходу газовой фазы из одной зоны в другую. Холодильник 1 предназначен для охлаждения нагретого регенерированного адсорбента, который движется по трубкам, а в межтрубном пространстве движется холодная вода. Подогревание десорбционной зоны 7 применяется для нагревания адсорбента в процессе десорбции.
Адсорбент движется по трубам, а в межтрубное пространство поступает горячий теплоноситель. При движении сверху вниз адсорбент вначале охлаждается до указанной температуры в трубах холодильника 1 и через распределительную тарелку поступает в адсорбционную секцию 3. Здесь он взаимодействует с исходной газовой смесью, которая поступает из распределительного устройства 4 и движется противотоком к направлению движения адсорбента, т.е. вверх. Очищенные от поглощаемого компонента газы выходят через штуцер 12.
7. Уравнение неразрывности оплошности потока

8. Сырьё. Обработка сырья.
Сырьем называют природные материалы, используемые в производстве промышленной продукции. Сырье – это главный элемент производства, от которого зависит его экономичность, выбор технологии, аппаратуры и также качество продукции. В химической технологии используют сырье, производимое нефтяной, газовой, горнорудной, коксохимической, лесной, целлюлозно-бумажной, пищевой отраслями промышленности, черной и цветной металлургией. Химическое сырье классифицируют по происхождению, химическому составу, ресурсам и агрегатному состоянию. Подобная классификация представлена в таблице 2.1.
Таблица 2.1
Классификация химического сырья
По агрегатному состоянию
По химическому состоянию
По видам запасов
По происхождению
Твердое
Неорганическое
Возобновляемое
Минеральное, в т.ч.:
– рудное,
– нерудное,
– горючее
Жидкое
Органическое
Невозобновляемое
Растительное и животное
Газообразное,Вода,Воздух
Кроме того, химическое сырье делится также на первичное и вторичное:
первичное сырьё извлекают из природных источников;
вторичное сырьё – это промежуточные и побочные продукты промышленного производства и потребления. При этом следует отметить, что капитальные вложения в переработку вторичного сырья в среднем в четыре раза меньше, чем для переработки первичного сырья. Не случайно поэтому в промышленно развитых странах повторное использование металлов и сплавов составляет, % масс.: стали – 70; меди – 55; алюминия и олова – по 45; цинка – 21.
Еще один принцип классификации сырья предполагает его деление на природное и искусственное (полученное при промышленной обработке природного сырья).
К химическому сырью предъявляется ряд общих требований. Оно должно обеспечивать.
– малостадийность производственного процесса;
– агрегатное состояние системы, обеспечивающее минимальные затраты энергии для создания оптимальных условий протекания технологического процесса;
– минимальные потери подводимой энергии в окружающую среду;
– минимальные потери энергии с продуктами процесса;
– возможно более мягкие условия процесса (температура, давление, время контакта) и минимальный расход энергии на изменение агрегатного состояния реагентов и осуществление технологического процесса;
– максимальный выход целевого продукта.
Все ресурсы химического сырья делятся на запасы, т.е. выявленные и изученные, и на потенциальные ресурсы. В свою очередь по степени изучен-ности и пригодности к эксплуатации запасы сырья делятся на три категории:
– категория А – это запасы, детально разведанные и подготовленные к разработке;
– категория В – это запасы, установленные в результате геолого-разведочных работ;
– категория С – это запасы, определенные по результатам геофизической разведки и изучения по естественным выходам на поверхность.
Возможность использования сырья для промышленного производства определяется его ценностью, доступностью и концентрацией полезного ком-понента. Ценность сырья зависит от уровня развития технологии и задач, стоящих перед производством и может меняться со временем. К примеру, уран, ранее являвшийся отходом при получении радия, теперь является важнейшим стратегическим сырьем.
Доступность сырья для добычи определяется географией месторождения, глубиной залегания, разработанностью промышленных методов извлечения, наличием людских ресурсов для его эксплуатации.
Существенным фактором, определяющим возможность использования запасов сырья, является концентрация целевого элемента. Известно, что многие, распространенные в земной коре элементы, являются рассеянными, что затрудняет их использование для промышленного производства. Тем не менее, нередко эксплуатация бедных месторождений является рентабельной.
На долю России приходится мировых запасов, % масс.: газа – 45, ископаемых углей – 23, нефти – 6-8, древесины – 30, торфа и калийных солей – более 50, различного минерального сырья – около 20, в т.ч. железа и олова более – 27, никеля – 36, меди – 11, кобальта – 20, свинца – 12, цинка – 16, металлов платиновой группы – 40. По запасам золота Россия занимает третье место в мире. К этому следует добавить, что на территории России сосредоточено 20 % мировых запасов пресной воды.
Подготовка сырья к переработке предполагает доведение его качества и химического состава до определенных требований.
Если речь идет о подготовке твердого сырья, то она может включать классификацию, измельчение и сушку.
Подготовка жидкого сырья включает очистку его от газообразных и твердых примесей. Методы очистки жидкого сырья включают фильтрование, циклонирование, центрифугирование, отстаивание.
Газовое сырье очищают от жидких и твердых примесей теми же методами, что и жидкое сырье, а также электростатическим воздействием.
Одной из важнейших стадий подготовки твердого сырья является обогащение, т.е. отделение полезной составляющей сырья от балласта (пустой породы). Результатом процесса обогащения является получение концентрата полезного компонента и «хвостов» с преобладанием в них пустой породы. Эффективность процесса обогащения характеризуется следующими показателями.
1. Выход концентрата – отношение масс полученного концентрата тк и обогащаемого сырья тс:
= тк/ тс. (2.1)
2. Степень извлечения полезного компонента Хи – отношение масс полезного компонента в концентрате тк.к. и в обогащаемом сырье тк.с.:
Хи = тк.к/ тк.с. (2.2)
3. Степень обогащения сырья Хо – отношение массовых долей полезного компонента в концентрате ωк.к. и в обогащаемом сырье ωк.с.:
Хо = ω к.к/ ωк.с. (2.3)
Обогащение твердого сырья ведут физическими, химическими и физико-химическими методами.
К физическим методам относят:
– гравитационный, основанный на разной скорости оседания частиц различной плотности и размеров в потоке газа или жидкости, либо в поле центробежной силы;
– электромагнитный, основанный на различной магнитной проницаемости компонентов сырья;
– электростатический, основанный на различной электрической проводимости компонентов сырья;
– термический, основанный на разности плавкости компонентов сырья.
Химическое обогащение основано на взаимодействии химических реагентов с полезным продуктом в породе (руде) с последующим выделением образовавшихся соединений осаждением, испарением, плавлением и т.д.
Одним из наиболее распространенных методов физико-химического обогащения сырья является флотация. Этим методом извлекают из природного сырья почти все минералы. Флотация базируется на различии в смачиваемости компонентов твердого сырья. Процесс флотации – это гетерогенный процесс, в котором присутствуют три фазы: твердая (т), жидкая (ж) и газообразная (г). На границе раздела фаз работа адгезии WA определяется суммой величин поверхностных натяжений на границах радела фаз: σж-г + σт-г + σт-ж. Для ускорения флотации и повышения ее качества в систему флотации вводят добавки – флотореагенты. Устройства, в которых проводят флотацию, называют флотационными аппаратами. Их конструкции весьма разнообразны.