
- •Получение сернистого газа сжиганием серы, сероводорода и других видов сырья
- •Коксование каменных углей
- •Химические методы получения гидроксида натрия
- •Известковый метод
- •Ферритный метод
- •Электрохимические методы получения гидроксида натрия
- •Контактный аппарат для окисления оксида серы(IV) в кипящем слое: 1 – выравнивающие решетки; 2 – катализатор; 3 – газораспределительные решетки; 4 – теплообменные элементы
- •Получение азота
- •13. Аммиак. Синтез аммиака.
- •14. Азотная кислота. Абсорбция нитрозных газов при атмосферном давлении.
- •15. Получение чугуна
- •16.Абсорбция серного ангидрида. Получение могогидрата и олеума
- •17. Получение этилена, ацетилена.
- •Получение пиролизом
- •20. Ректификация нефти.
- •23.Каталитический крекинг.
- •22. Выплавка стали.
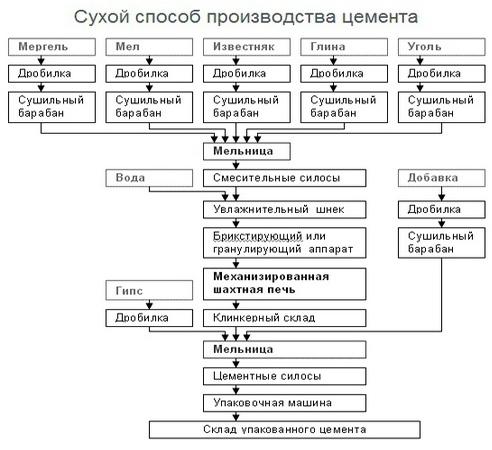
- •24.Получение цемента сухим способом.
- •Производство цемента сухим способом
- •25. Технология получения соды.
- •26. Получение водорода из водяного пара
- •27. Получение стекла
- •28. Получение карбамида
- •29. Получение капролактама. Капрон.
- •9. Топливо. Электроэнергия.
- •10. Уравнение теплопроводности.
- •11. Уравнение Эйлера для гидродинамических условий.
- •12. Насосы. Компрессоры.
- •13. Сушка. Виды сушилок.
- •15. Теплообменники.
- •22. Ректификация. Ректификационная колонна.
- •21. Закон сохранения массы для любого разреза аппарата.
- •20. Выпарки. Упаривание методом противотока
- •19. Выпарки. Упаривание методом прямотока.
- •18. Экстракция. Экстракторы.
- •17. Уравнение Бернулли.
- •16. Критерии Рейнольдса.
22. Выплавка стали.

24.Получение цемента сухим способом.
Производство цемента включат 2 этапа:
получение клинкера,
измельчение клинкера и введение добавок.
На получение клинкера приходится приблизительно 70% себестоимости стройматериала.
Начинается все с добычи сырьевых материалов. Как правило, добыча известняка осуществляется путем сноса части горы, после которого открывается слой желто-зеленого известняка. Глубина залегания известнякового слоя – приблизительно 10 м, толщина – в среднем 0,7 м. После того, как сырье доставлено на завод, производится обжиг в специальной печи при температуре +1450°С, в результате которого получают клинкер.На второй стадии производства цемента осуществляют дробление клинкера, гипсового камня, сушка добавок. Затем производится помол клинкера вместе с добавками и гипсом. Гипс добавляют в размере 5% от общей массы, добавки вводят в зависимости от типа смеси.
Однако, учитывая тот факт, что технические и физические характеристики сырьевого материала могут отличаться, для каждого типы сырья предусмотрен свой способ подготовки.
Производство цемента сухим способом
Данный способ по праву считается наиболее экономически выгодным. Особенность его в том, что на всех стадиях используются материалы только в сухом состоянии. Выбор схемы производства цемента определяется химическими и физическими характеристиками сырья. Наиболее востребованным признано изготовление материалов во вращающихся печах, в котором используются глина и известняк.
После того, как глина и известняк прошли измельчение в дробилке, их сушат до требуемого состояния (влажность - не более 1%). Просушка и измельчение производиться в сепараторной машине, после чего смесь отправляется в циклонные теплообменники, где находится не боле 30 секунд. Далее идет стадия, на которой производиться обжиг сырья с дальнейшим перемещением в холодильник. Затем клинкер направляется на склад, где происходит его перемалывание и фасовка. В завершение цемент перенаправляется из бункеров мельниц в специальные помещения для хранения. На этом производственном этапе лаборанты осуществляют контроль качества продукции и определяют марку цемента. Только после этого продукция направляется в упаковочные аппараты.
25. Технология получения соды.
Сода впервые была получена в 1793 г. Лебланком, однако пищевая, очищенная сода была изготовлена в 1861 г. Сольвэ. В конце XVIII и начале XIX в. для получения искусственной соды стали применять способ Леблана, сущность которого заключается в следующем: из поваренной соли действием на нее серной кислотой вначале получали сульфат натрия, затем сульфат натрия сплавляли при высокой температуре с углекислым кальцием и углем. Из полученного сплава соду выщелачивали водой. Раствор затем выпаривали. Изобретение бельгийским ученым Э. Сольвэ в середине XIX столетия аммиачного способа получения соды способствовало интенсивному ее внедрению в первую очередь в кондитерское дело. Основной способ искусственного получения соды в настоящее время во всех странах - аммиачный способ производства кальцинированной соды, являющейся материалом для получения остальных содовых продуктов. Сначала Франция и Германия использовали соду как технологическую добавку для разрыхления теста с целью увеличения его объема, улучшения качества. Сода делает тесто мягким, пышным, легко усвояемым. С конца XIX-начала XX века соду стали применять другие страны, в том числе Россия. Добывают соду сейчас промышленным аммиачным способом (способ Сольве). В насыщенный раствор хлорида натрия пропускают эквимолярные количества газообразных аммиака и диоксида углерода, то есть как бы вводят гидрокарбонат аммония NH4HCO3: NH3 + CO2 + H2O + NaCl → NaHCO3 + NH4Cl. Выпавший остаток малорастворимого (9,6 г на 100 г воды при 20° C) гидрокарбоната натрия отфильтровывают и кальцинируют (обезвоживают) нагреванием до 140 - 160° C, при этом он переходит в карбонат натрия: 2NaHCO3 →(t) Na2CO3 + CO2↑ + H2O Образовавшийся диоксид углерода и аммиак, выделенный из маточного раствора на первой стадии процесса по реакции: 2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3↑ + 2H2O возвращают в производственный цикл. Аммонизация раствора необходима для введения в него углекислого газа, малорастворимого в насыщенном растворе. Выпавший в виде кристаллов бикарбонат натрия отфильтровывают от раствора, содержащего хлористый аммоний и непрореагировавший NaCl, и прокаливают (кальцинируют). При этом происходит образование кальцинированной соды. Выделяющиеся при кальцинации газы, содержащие углекислоту СO2, используют для карбонизации. Таким образом, часть затраченной углекислоты регенерируется. Необходимую для процесса углекислоту получают обжигом известняка или мела. Обожженную известь СаО гасят водой. Гашеная известь Са(ОН)2 замешивается с водой. Образовавшееся известковое молоко используют для регенерации аммиака из раствора (фильтровой жидкости), полученного после отделения бикарбоната и содержащего хлористый аммоний. Для производства соды используют раствор поваренной соли (рассол) концентрации около 310 г/л, полученный в естественных условиях подземным выщелачиванием залежей поваренной соли. В естественном рассоле, помимо NaCl, обычно содержатся соли кальция и магния. При аммонизации и карбонизации рассола в результате взаимодействия этих примесей с NH3 и СО2 будут выпадать осадки, что приведет к загрязнению аппаратов, нарушению теплообмена и нормального хода процесса. Поэтому рассол предварительно очищают от примесей: осаждают их, добавив к рассолу строго определенное количество реактивов - суспензии соды в очищенном рассоле и известкового молока. Этот способ очистки называется содово-известковым. Выпавшие при этом осадки гидрата магния и карбоната кальция отделяют в отстойниках. Очищенный и осветленный рассол поваренной соли направляют в барботажную абсорбционную колонну. Верхняя часть колонны служит для промывки рассолом газа, отсасываемого вакуум-насосом из вакуум-фильтров, и газа из карбонизационных колонн. В этих газах содержится небольшое количество аммиака и углекислоты, которые целесообразно отмыть свежим рассолом и, таким образом, более полно использовать их в производстве. Нижняя часть колонны служит для насыщения рассола аммиаком, поступающим из дистилляционной колонны. Полученный аммиачно-соляной рассол далее направляют в барботажную карбонизационную колонну, где происходит основная реакция превращения исходного сырья в бикарбонат натрия. Необходимая для этой цели углекислота СO2 поступает из шахтной известково-обжигательной печи и печи кальцинации бикарбоната натрия и нагнетается снизу в колонну. Карбонизация аммиачно-соляного рассола является важнейшей стадией производства соды. Образование бикарбоната натрия при карбонизации происходит в результате протекания в карбонизационной колонне сложных химических процессов. В верхней части колонны идет образование углекислого аммония из аммиака, содержащегося в рассоле, и углекислоты, подаваемой в колонну. По мере прохождения рассола в колонне сверху вниз углекислый аммоний, реагируя с избытком углекислоты, поступающей снизу колонны, переходит в двууглекислый аммоний (бикарбонат аммония). Примерно в середине верхней неохлаждаемой части колонны начинается реакция обменного разложения, сопровождающаяся выпадением кристаллов бикарбоната натрия и образованием в растворе хлористого аммония. В средней части колонны, где идет образование кристаллов бикарбоната натрия за счет экзотермичности реакции, температура рассола несколько повышается (до 60 - 65° C), однако охлаждать его не надо, так как такая температура способствует формированию более крупных хорошо фильтрующихся кристаллов бикарбоната натрия. Внизу колонны охлаждение необходимо для уменьшения растворимости бикарбоната натрия и увеличения его выхода. В зависимости от температуры, содержания NaCl в рассоле, степени насыщения его аммиаком и углекислотой и других факторов выход бикарбоната составляет 65-75%. Практически невозможно полное превращение поваренной соли в осадок бикарбоната натрия. В этом заключается один из существенных недостатков производства соды аммиачным методом.
Способы производства бикарбоната натрия.
Бикарбонат натрия выступает промежуточным продуктом промышленного получения кальцинированной соды по методу Сольве, предусматривающему пропускание через насыщенный раствор хлорида натрия эквимолярных (т.е. содержащих равные количества молей) количеств газообразных аммиака и диоксида углерода, что имитирует ввод в систему гидрокарбоната аммония NH4HCO3: NH3 + H2O + CO2 + NaCl / NH4HCO3 → NaHCO3 + NH4Cl. В образующемся растворе наименее растворимой солью является бикарбонат натрия, который выпадает в виде кристаллического осадка. При этом важно отметить, что товарным видом данной продукции выступает очищенный двууглекислый натрий. Наиболее широко распространенным способом очистки солей от примесей в общем случае выступает их перекристаллизация из растворов, причем в качестве растворителя наиболее часто используется вода. В основе данного способа лежит свойство большинства солей увеличивать растворимость при повышении температуры. Согласно методу перекристаллизации, очищаемая соль растворяется в воде при высокой температуре, после чего раствор доводится до насыщенияч, а затем охлаждается, причем началу последнего из перечисленных процессов предшествует удаление нерастворенных примесей посредством фильтрации. В ходе же охлаждения раствора растворимость соли уменьшается, она выпадает в осадок и отфильтровывается. Вследствие предпринимаемых мер чистота соли повышается, поскольку все примеси, входящие в ее состав до осуществления процесса, растворяются в воде и переходят в фильтрат, представляющий собой маточную жидкость, возвращаемую на начальную стадию. По мере циркуляции маточной жидкости в ней накапливаются примеси, что в конечном счете негативно отражается на чистоте получаемой продукции и обуславливает необходимость периодического вывода из цикла части фильтрата. Однако в том случае, если соль, подобно бикарбонату натрия, плохо растворима в воде, очищать ее методом перекристаллизации представляется экономически невыгодным, так как в системе для получения единицы массы чистого продукта должно циркулировать большое количество маточной жидкости, требующей попеременного нагревания и охлаждения. В связи с этим обстоятельством в промышленных масштабах очищенную пищевую соду получают не методом перекристаллизации, но карбонизацией содового раствора путем пропускания диоксида углерода под давление в насыщенном растворе карбоната натрия при температуре около 75° С согласно реакции: Na2CO3(р.) + CO2(г.) + H2O(ж.) ↔ 2NaHCO3(тв.) + 52,4 кДж (+ 12,5 ккал). Практическое применение метода карбонизации позволяет значительно сократить объем жидкости, необходимой для получения единицы бикарбоната натрия, поскольку растворимость кальцинированной соды в несколько раз превышает соответствующий показатель гидрокарбоната натрия. Содовый раствор для карбонизации получается путем растворения в воде твердой технической соды, образующейся при кальцинации сырого бикарбоната (этот процесс носит название «сухого» способа) или же разложением двууглекислого натрия в водной среде при нагревании («мокрый» способ), которое называется декарбонизацией, согласно реакции: 2NaHCO3(р.) ↔ Na2CO3(р.) + CO2(г.) + H2O(пар) - 20,6 кДж (- 4,9 ккал). Выпадающая при насыщении содового раствора диоксидом углерода чистая пищевая сода отделяется, а маточная жидкость, содержащая смесь карбоната и бикарбоната натрия, а также растворенных примесей (например, NaCl), возвращается в начало процесса для получения исходного раствора. Вследствие многократной циркуляции маточной жидкости в ней накапливаются примеси, способные засорить очищенный продукт. В результате этого часть маточной жидкости выводится из цикла и направляется в общем случае на рассолоочистку с целью разбавления крепкого содового раствора.
Для производства очищенного бикарбоната натрия используются так называемые «сухой» и «мокрый» способы. В основе процесса обычная реакция карбонизации, т.е. насыщение раствора углекислым газом. Происходит перекристаллизация. Способы отличаются приготовлением раствора. При сухом способе берется готовая кальцинированная сода и растворяется водой, а при мокром используется технический бикарбонат. Колонное оборудование по принципу действия почти идентично тому, что задействовано при производстве кальцинированной соды, но выполнено из высококачественной нержавеющей стали. Чистота в цехе и чистота готовой продукции находятся под постоянным контролем органов государственного санитарно-эпидемиологического надзора.
