
04_Per_zakon
.pdf
Періодичний закон Д.І. Менделєєва
24.09.2013 |
1 |

Перші варіанти періодичної системи
Тріади Деберейнера (1829)
Йоганн Вольфганг Деберайнер
|
|
|
|
|
|
|
M |
|
|
M Ca M Ba |
|
40 137 |
88,5 |
Sr |
|
|
||||
|
2 |
|
2 |
|
||
|
|
|
|
|||
24.09.2013 |
2 |
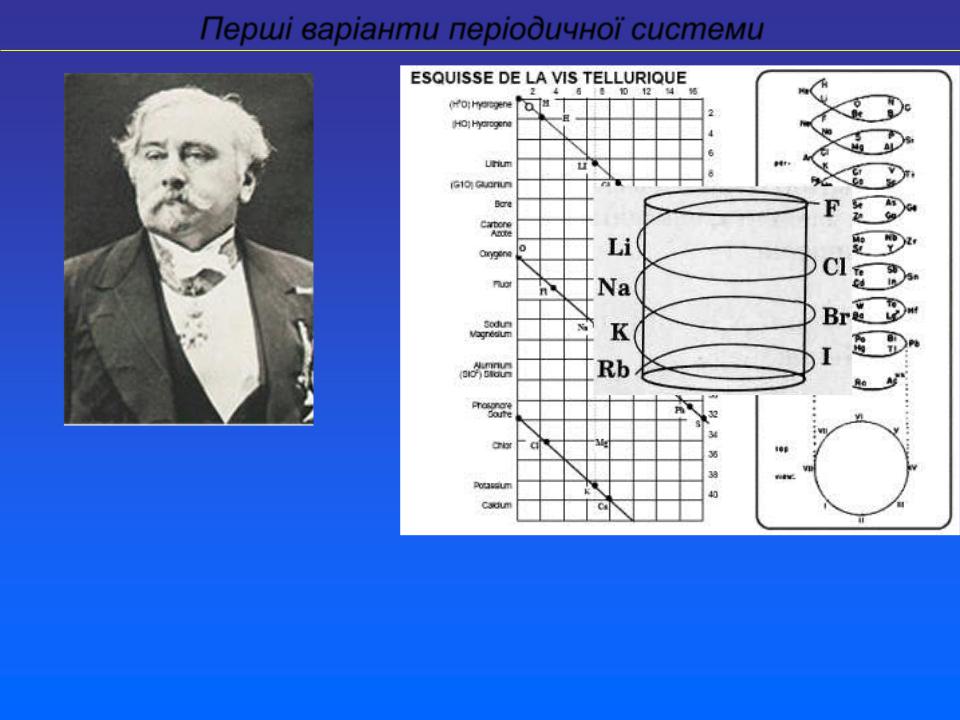
Перші варіанти періодичної системи
Александр Еміль Бегуйє де Шанкуртуа
Спіраль де Шанкуртуа (1862) – елементи розташовані за зростанням їх атомних мас і нанесені на циліндр по лінії, що виходила з його основи під кутом 45°
24.09.2013 |
3 |

Перші варіанти періодичної системи |
|
|
||||||
Таблиці Одлінга і Мейера (1864 р.): |
|
|
|
|
||||
28 елементів – 6 стовпців згідно їх валентностей |
||||||||
|
|
|
|
Валентність |
|
|
||
|
|
|
IV |
III |
II |
I |
I |
II |
|
|
I |
|
|
|
|
Li |
Ве |
|
|
II |
C |
N |
O |
F |
Na |
Mg |
|
Ряд |
III |
Si |
P |
S |
Cl |
K |
Ca |
|
|
|
|
|
|
|
|
|
|
|
IV |
|
As |
Se |
Br |
Rb |
Sr |
|
|
V |
Sn |
Sb |
Te |
I |
Cs |
Ba |
Лотар Юліус Мейєр |
|
VI |
Pb |
Bi |
|
|
Tl |
|
24.09.2013 |
|
|
|
|
|
|
|
4 |

Перші варіанти періодичної системи
Джон Александр Рейна Ньюлендс
Октави Ньюлендса (1865)
до |
ре |
мі |
фа |
соль |
ля |
сі |
|
|
|
|
|
|
|
H |
Li |
Ве |
B |
C |
N |
O |
|
|
|
|
|
|
|
F |
Na |
Mg |
Al |
Si |
P |
S |
|
|
|
|
|
|
|
Cl |
K |
Ca |
Ti |
Cr |
Mn |
Fe |
|
|
|
|
|
|
|
Co, Ni |
Cu |
V |
Zn |
In |
As |
Se |
|
|
|
|
|
|
|
•елементи – за зростанням атомних мас
•порядковий номер
•систематичне співвідношення між розташуванням і властивостями
24.09.2013 |
5 |

Відкриття Д.І. Менделєєва
«Властивості елементів, а тому і властивості утворюваних ними простих і складних тіл перебувають у періодичній залежності від їх атомних ваг (мас – з 1954 р.)»
1 березня 1871 р.
Розташував у порядку зростання атомних ваг (мас), але:
змінив атомні ваги 17 елементів
сформулював поняття про групи, малі та великі періоди (оцінив їх «місткість»)
24.09.2013 |
6 |

Відкриття Д.І. Менделєєва
Рукописний та перший друкований варіанти таблиці
24.09.2013 |
7 |
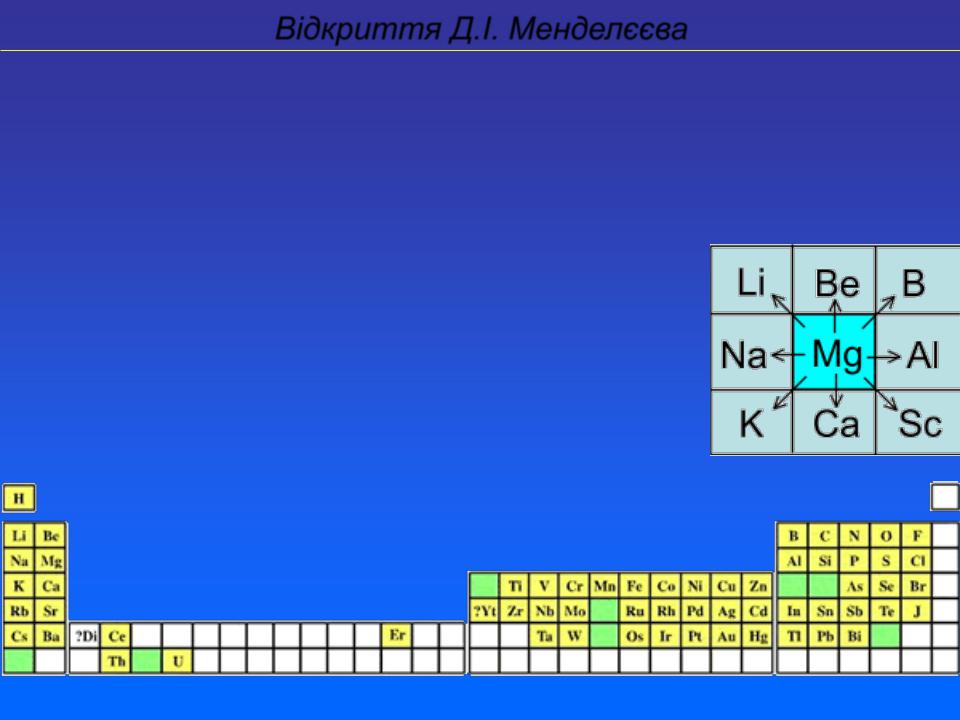
Відкриття Д.І. Менделєєва
Описав властивості ще невідкритих елементів. Передбачені елементи відкрили:
Екаалюміній - галій (Лекок де Буабодран, 1875),
Екабор - скандій (Нільсон, 1879)
Екасиліцій - германій (Вінклер, 1886)
1880 р. - Періодичний закон остаточно визнаний як одна з теоретичних основ хімії
24.09.2013 |
8 |

Закон Мозлі (1913)
корінь квадратний з частоти конкретної лінії однакових серій рентгенівського спектру випромінювання елементів прямо пропорційний їх атомному номеру:
1 |
a(Z b) або √ν = a(Z – b), |
|
|
||
|
де: λ – довжина хвилі; ν – частота випромінення;
Z – атомний номер елемента; a і b – константи.
Причина періодичної зміни властивостей – не атомні маси, а заряди ядер, які чисельно рівні атомним номерам.
Сучасне формулювання:
Властивості простих речовин, а також форми і властивості сполук елементів знаходяться в періодичній залежності від зарядів ядер атомів елементів
24.09.2013 |
9 |

Розвиток Періодичного закону в XX ст.
Д. І. Менделєєв, У. Рамзай - нульова група - інертні гази
Б. Браунер, 1902 р. - поміcтив РЗЕ в одну клітинку
Ф. Содді, 1911 р. – розмістив елементи з різними атомними масами (ізотопи) в одних клітинках
А. Ван ден Брук (1911) – атомний номер – основа класифікації хімічних елементів
Дж. Чедвік (1920) – підтвердив гіпотезу Ван ден Брука
Н. Бор (1921 – 1923) – теорія Періодичної системи
З. А. Щукарєв (1948) – «лантаноїди» і «актиноїди»
24.09.2013 |
10 |
