
Гидроксикоричные кислоты
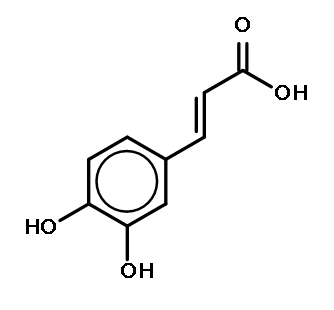
Кофейная кислота - обладает желчегонным и сильным антибактериальным действием.
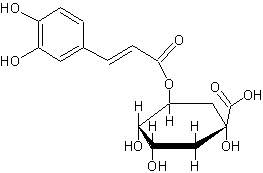
Хлорогеновая кислота – имеет:
антибактериальные, противовоспалительные и противовирусные свойства;
характеризуется противораковой (антимутагенной) активностью;
имеет антиоксидантное действие;
способствует укреплению мышц, костей;
благоприятствует нормальной деятельности печени;
способствует стабилизации беременности.
Скополетин
-
биологически очень активен и оказывает
психофармакологическое действие на
организм. Это выражается прежде всего
в снижении зависимости от алкоголя и
различных наркотических веществ, в т.ч.
табака. Поэтому лекарственные вытяжки
часто используют в лечении наркозависимости
и алкоголизма.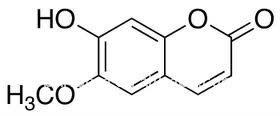
Стероиды
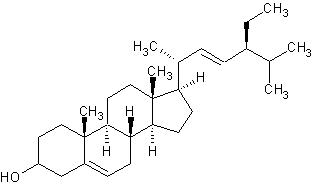
Бета-ситостерин - основной эффект, за счет которого он приобрел популярность - снижение уровнях вредного холестерина в крови, поэтому чаще всего ситостерин используется для лечения гиперхолестеринемии. Бета-ситостерол подавляет всасывание холестерина из пищеварительного тракта, благодаря схожести в структуре он конкурентным образом связывается с мицеллами, не давая холестерину быть усвоенным.
Одно небольшое исследование установило, что бета-ситостерин тормозит потерю волос у мужчин.
В Европе ситостерол применяется для лечения доброкачественной гипертрофии простаты, карциномы простаты, рака молочной железы, хотя положительный эффект лечения еще не доказан.
Кампестерол
-
является естественным солнцезащитным
фильтром, он обладает свойствами
абсорбции ультрафиолета; сдерживая
меланогенез, он профилактирует появление
нежелательной пигментации и старческих
пятен.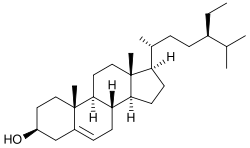
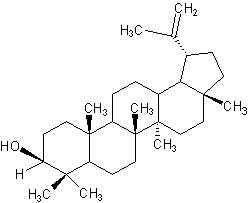
Лупеол – проявляет противораковую активность, уменьшает уровень метастазирования
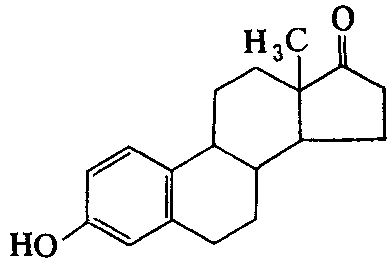
Фолликулин - естественный фолликулярный гормон (гормон яичников). Оказывает специфическое эстрогенное действие (подобное действию женских половых гормонов - эстрогенов.
Прочие
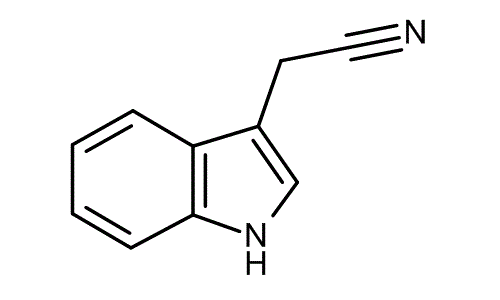
Индол-3-ацетонитрил
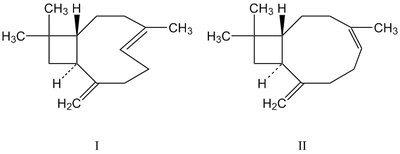
Кариофиллен
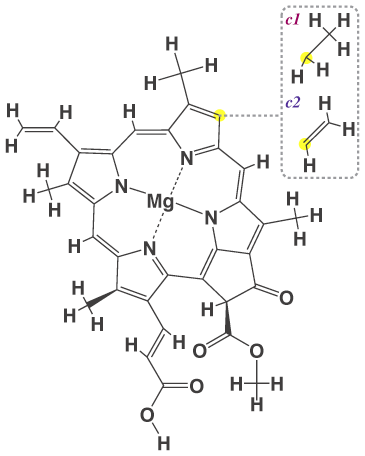
Хлорофилл
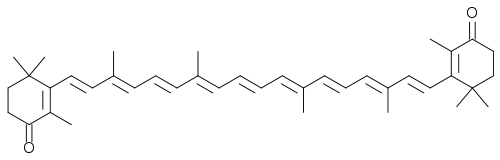
Ксантофилл

Гуминовые кислоты
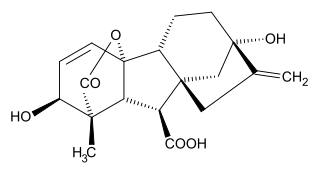
Гиббереллин
А так же минеральные соли: кальций, магний, калий, фосфор, цинк, железо, кобальт, марганец. [7] [11]
Количественное определение гликозидов
Образцы для исследований брали на испытательном участке университета, в селах Патара Поти Хобско-го района, Анаклиа Зугдидского района, Грмагеле Ланчхутского района, Ахалсопели Сенакского района (Западная Грузия).
С
целью инактивации ферментов растительные
образцы фиксировали водяным паром в
течение 1 мин, затем сушили при комнатной
температуре и измельчали. Исследование
сладких дитерпеноидных гликозидов
листьев стевии проводили по схеме,
представленной на рисунке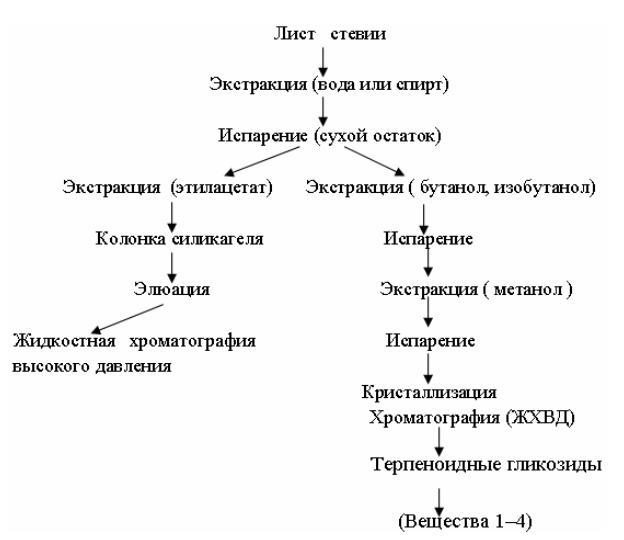
Листья стевии(5 г) измельчали, обрабатывали в аппарате Сокслета хлороформом(300 мл) в течение 2 ч, далее метанолом(300 мл) в течение 5 ч, затем водой(30 мл). Полученный экстракт фильтровали и концентрировали в условиях вакуума. Хлороформные и водяные экстракты не содержат сладких терпеноидных гликозидов.
Метанольные экстракты перекристаллизировали трижды, растворяли в метаноле(10 мл), фильт-ровали через мембранные фильтры(0,45 мкр). Высокоэффективную тонкослойную хроматографию произ-водили на тонком слое силикагеля(Меrс), система растворителей: хлороформ– метанол– вода(30 : 20 : 4).
Хроматограму проявляли10% серной кислотой. При хроматографировании применяли растворите-ли: 1) хлороформ– метанол– вода(30 : 20 : 4); 2) этилацетат– изопропанол– н-бутанол– вода(20 : 12 : 7 : 6).
Исследование терпеноидных соединений осуществляли методом жидкостной хроматографии высокогодавления. Хроматографирование проводили на хроматографеBeckman (USA), детектор Millipore-Wаters 210 нм, хроматографические колонкиBordapac C18; Bordapac NH2. Системы растворителей: 1) метанол– вода(65 : 35); 2) ацетонитрил– вода(85 : 15); 3) ацетонитрил– вода(40 : 60).
После проявления пластинки нагревали до110 °С иденситометрировали при390 нм. В таблице1 приве-дены значения Rf этих соединений(окраска экстракта после обработкиH2SO4 темная). Идентификация сладких дитерпеноидных гликозидов стала возможной на основе сопоставления литературных данных споказателями аутентичных соединений(стевиозид и ребаудиозид А).

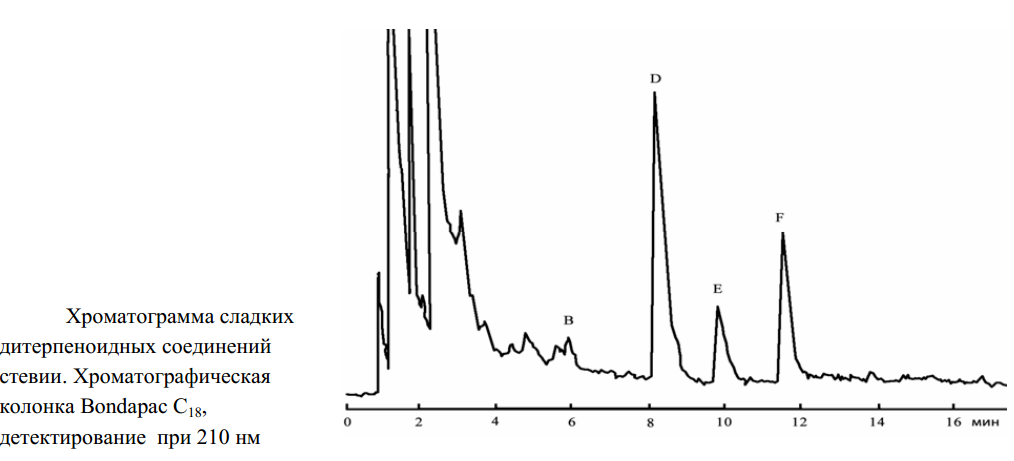
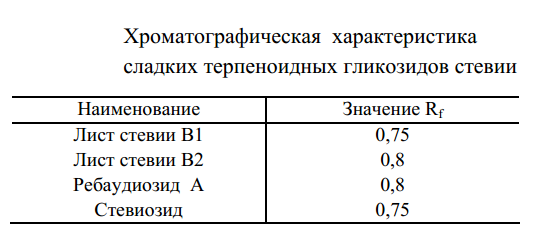
Для стевиозида значение Rf равно 0,75, а для ребаудиозида– 0,80. Опрыскивание серной кислотой, естественно, вызывает образование темных пятен на хроматограмме. Сладкие дитерпеноидные гликозиды в УФ-свете имеют максимум поглощения при210 нм.
Жидкостная хроматография высокого давления позволяет провести анализ в течение20–30 мин, при этом разделяются все основные дитерпеноидные гликозиды.
Посадка саженцев стевии производится в апреле. На1 га сажают 50–70 тыс. саженцев.
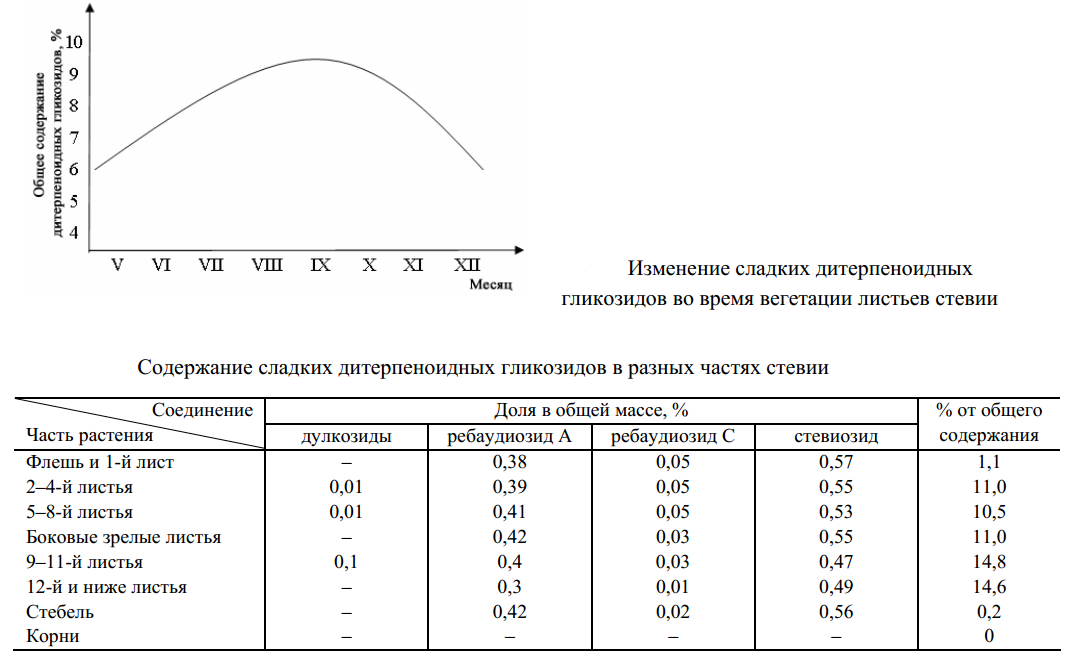
Определение оптимального периода уборки урожая крайне важно, чтобы урожай и содержание в растениях сладких дитерпеноидных гликозидов были максимальными. Зафиксировано содержание сладких дитерпеноидных гликозидов на всех этапах роста и развития стевии.
Количество этих соединений возрастает до начала цветения, а затем чуть снижается, поэтому для уборки урожая оптимальным можно считатьпериод бутонизации.
В стевии сладкие дитерпеноидные соединения распределены неравномерно. Основная их часть рассредоточена в зрелых листьях, которые во время бутонизации растения составляют35% от общей массы. Зрелые листья накапливают основную часть сладких веществ, в 9–12-м листьях насчитывается более70% терпеноидов от их общего содержания. В стеблях концентрация сладких гликозидов низкая(0,1%), поэтому перерабатывать их дальнейшем нет смысла(общая доля стебля– 40%).
Выводы
Нами установлено, что в листьях нового для влажных субтропиков растения стевия(Stevia rebaudiana Bertoni) содержится до 11%сладких дитерпеноидных соединений. Сладкие дитерпеноиды в разных частях растения накапливаются по-разному. Максимальное содержание этих соединений обнаружено в зрелых листьях. [8] [9] [15]
