
гинекология 5 курс экзамен / а / Диагностика и лечение гипоксии плода во время родов
.docxДиагностика и лечение гипоксии плода во время родов.
Под гипоксией плода подразумеваются патологические состояния, развившиеся под влиянием кислородной недостаточности во время беременности и в родах. В структуре перинатальной смертности гипоксия плода и новорожденного занимает одно из первых мест. Частота гипоксии плода составляет 4—6%, а в структуре перинатальной заболеваемости — 21—45%.
Классификация. Гипоксия плода возникает в результате нарушения доставки кислорода к тканям и (или) его использования. В соответствии с этим можно различать следующие виды гипоксии:
-
гипоксическая гипоксия, когда насыщение гемоглобина кислородом ниже нормального уровня;
-
циркуляторная гипоксия, когда кислород не поступает к тканям в достаточном количестве, несмотря на нормальное его напряжение в артериальной крови;
-
гемическая (анемическая) гипоксия при значительном уменьшении эритроцитов (например, гемолитическая болезнь плода) или низком содержании гемоглобина в эритроцитах, а также при снижении способности гемоглобина связывать кислород;
-
тканевая гипоксия при нарушениях клеточного гомеостаза, когда клетки не в состоянии в полной мере использовать кислород.
При развитии тяжелого кислородного голодания у плода наблюдается смешанный тип гипоксии, характеризующийся одновременным нарушением функции нескольких систем, обеспечивающих снабжение тканей кислородом.
Этиология и патогенез. Различают острую и хроническую гипоксию плода. Причинами хронической гипоксии плода являются следующие: 1) заболевания матери, ведущие к развитию у нее гипоксии (декомпенсированные пороки сердца, сахарный диабет, анемия, бронхолегочная патология, интоксикации, в том числе инфекционные) и неблагоприятные условия труда (профессиональная вредность); 2) осложнения беременности (и связанное с ними нарушение развития плаценты) и расстройство маточно-плацентарного кровообращения (поздний гестоз, перенашивание, многоводие); 3) заболевания плода (тяжелые формы гемолитической болезни, генерализованной внутриутробной инфекции, пороки развития).
Острая гипоксия плода возникает в результате: 1) неадекватной перфузии крови к плоду из материнской части плаценты; 2) отслойки плаценты; 3) прекращения тока крови по пуповине при ее пережатии; 4) истощения компенсаторно-приспособительных реакций плода и его неспособности переносить изменения оксигенации, связанные с сократительной деятельностью матки даже в условиях нормального родового акта. Подобное состояние возникает в связи с нарушением развития плода (гипотрофия, анемия) или в результате медикаментозных воздействий (обезболивание родов).
Плод более резистентен к гипоксии, чем взрослый. Факторами, обеспечивающими адаптацию плода к гипоксии, являются:
-
увеличенное сродство к кислороду фетального гемоглобина;
-
повышенная способность тканей поглощать кислород из крови;
-
высокая тканевая резистентность к ацидозу.
Патогенез внутриутробной гипоксии плода можно представить следующим образом. Нарушение трансплацентарной диффузии кислорода и транспорта кислорода от матери к плоду ведет к гипоксемии плода, в результате чего активируются его компенсаторно-приспособительные механизмы. Последовательно происходят следующие процессы:
-
увеличение интенсивности маточно-плацентарного кровотока;
-
возрастание продукции катехоламинов, ренина, вазопрессина, глюкокортикоидов;
-
повышение сосудистого тонуса и за счет этого — сокращение значительной части сосудистого русла; депонирование крови в печени облегчает системное кровообращение плода;
-
перераспределение крови с преимущественным снабжением мозга, сердца, надпочечников и уменьшением кровотока в легких, почках, желудочно-кишечном тракте и теле плода;
-
увеличение сердечного выброса;
-
возрастание систолического артериального давления и центрального венозного давления.
При длительно сохраняющейся гипоксии плода или при дополнительном резком уменьшении поступления кислорода наступает следующий этап реакции плода, характеризующийся максимальным вовлечением биохимических функциональных резервов и появлением первых признаков истощения компенсаторно-приспособительных реакций. Наблюдается усиление анаэробного гликолиза, мобилизация гликогена из депо (печень, сердце, почки) и активация фосфолипаз. Вслед за усилением отдачи кислорода уменьшается его потребление тканями плода, что способствует развитию гипоксии тканей. Характерной чертой данного этапа является появление ацидоза крови. В условиях прогрессирующей гипоксии наблюдается отхождение мекония в околоплодные воды. Появляется брадикардия плода, вследствие которой увеличивается продолжительность диастолы, что способствует улучшению наполнения левого желудочка и поддержанию силы сердечных сокращений. Это позволяет временно сохранить нормальными сердечный выброс и систолическое артериальное давление. В этих условиях мозговой кровоток еще достаточен для функции органа, хотя возникает перераспределение крови в мозге с преимущественным снабжением подкорковых отделов.
На последнем этапе адаптации к гипоксии происходит истощение компенсаторно-приспособительных реакций, что ведет к значительному снижению напряжения кислорода и возрастанию РС02> развитию и прогрессированию метаболического ацидоза. В условиях метаболического ацидоза наступает падение сосудистого тонуса, повышается проницаемость сосудистой стенки. Вначале возникает внутриклеточный отек, затем отек тканей — за счет выхода жидкости из сосудистого пространства. Нарушается синтез простагландинов, что способствует изменению сосудистого тонуса и усилению агрегации тромбоцитов, нарушению микроциркуляции и ишемии ткани мозга. Продолжает повышаться центральное венозное давление, падает системное артериальное давление, уменьшается сердечный выброс, возникает гипоперфузия мозга, что ведет к еще более глубоким нарушениям метаболизма в нервной ткани. Истощение энергетических ресурсов изменяет функциональную активность АТФаз. В результате увеличивается выход из клетки калия и повышается внутриклеточное содержание натрия, что способствует деполяризации клеточных мембран. Увеличение кальциевых каналов и повышение внутриклеточного кальция вызывает активацию фосфолипазы А2, что способствует усилению перекисного окисления липидов, увеличению продукции свободных радикалов кислорода и эндоперекисей, вызывающих повреждение клеточных мембран и усугубляющих расстройство микроциркуляции, особенно в мозге. Там появляются участки ишемии с последующим некрозом, что ведет к необратимым изменениям нервной ткани и смерти плода.
Диагностика. При диагностике гипоксии плода необходима комплексная оценка результатов различных методов исследования.
Одним из наиболее простых и распространенных методов контроля за функциональным состоянием плода во время беременности и в родах является регистрация его сердечной деятельности. Для диагностики нарушений жизнедеятельности плода определяют частоту, ритм, вариабельность сердцебиения во время функциональных проб, к которым относят нестрессовый (НОТ), степ-тест и контрактильный стрессовый (КСТ) тесты. Оценку частоты сердечных сокращений (ЧСС) необходимо проводить с учетом срока беременности (брадикардия в I, тахикардия во II и нормокардия в III триместрах). Урежение ЧСС до 80 уд/мин и менее указывает на тяжелую гипоксию плода, а стойкость этого симптома является плохим прогностическим признаком.
Достаточно ранние и четкие критерии гипоксии плода можно получить при анализе ЭКГ и ФКГ плода: деформация комплекса ОК5, его увеличение свыше 0,07 с, увеличение интервала Р0.до 0,12 с и появление шумов на ФКГ.
Для суждения о характере ЧСС необходимо использовать длительное мониторное наблюдение, выявляющее нормальные колебания ЧСС от 120 до 160 уд/мин. Низкий вариационный размах ЧСС в течение не менее часа наблюдения (монотонный сердечный ритм) свидетельствует о высоком риске для плода. Анализ сердечного ритма и его реактивности у плода в последнем триместре беременности должны проводиться с учетом его функционального состояния (активное или спокойное). Поскольку фаза спокойного сна может продолжаться до 30— 40 мин, продолжительность регистрации сердечного ритма должна быть не менее 60 мин.
Учащение сердцебиений плода на 15—35 ударов в ответ на шевеление (положительный «миокардиальный рефлекс» или реактивный НСТ-тест) характеризует нормальное его состояние. НСТ-тест свидетельствует о гипоксии плода при наличии брадикардии, которая определяется как снижение ЧСС на 40 уд/мин по сравнению с базальной ЧСС (90 уд/мин), зарегистрированной в течение минуты.
В тех случаях, когда учащение сердцебиения плода выражено слабо или отсутствует (нереактивный НСТ-тест), производится проба с функциональной нагрузкой: беременная в течение 3—4 мин поднимается и спускается по двум ступенькам. До и после нагрузки регистрируют сердечную деятельность плода. При этом происходит уменьшение объема кровотока в матке, но ЧСС остается в физиологических границах 120—160 уд/мин. При гипоксии плода либо возникает монотонность ритма ЧСС без физиологических ее колебаний, либо появляется тахикардия, либо развивается стойкая брадикардия.
Окситоциновый тест позволяет создать модель, близкую по воздействию на плод родовой деятельности. Под влиянием окситоцина уменьшается кровоток в межворсинчатом пространстве, что проявляется, в свою очередь, реакцией
ЧСС плода. При гипоксии внутриутробного плода ЧСС либо возрастает (более 160 уд/мин), либо (при выраженной гипоксии) снижается (менее 120 уд/мин). Наиболее неблагоприятно появление монотонности ритма (10—50% тахограммы). При своей распространенности окситоциновый тест имеет ряд противопоказаний: угроза прерывания беременности, рубец на матке, предлежание плаценты, тяжелые формы позднего гестоза.
Проводятся пробы с задержкой дыхания на вдохе и выдохе. В норме задержка дыхания сопровождается изменением ЧСС в среднем на ±7 уд/мин. Задержка дыхания на вдохе вызывает урежение, а на выдохе — учащение ЧСС плода. Особенно показательна проба «на выдохе». При гипоксии плода наблюдается парадоксальная реакция или отсутствие изменений ЧСС.
При холодовом тесте (термическая проба) происходит уменьшение ЧСС в пределах 10 уд/мин, при гипоксии изменения ритма отсутствуют или реакция бывает извращенной.
При всех перечисленных тестах наиболее показательны длительность и скорость изменений ритма, амплитуда учащения или замедления ритма сердечных сокращений плода. Весьма информативным следует считать окситоциновый тест.
В настоящее время разработан способ определения функционального состояния плода, основанный на изменении ЭКГ и ФКГ при непосредственном воздействии на плод звуком [Айламазян Э. К., 1984]. В качестве звукового раздражителя служит звуковой сигнал частотой 3 кГц, длительностью 5 с, интенсивностью 95—100 дБ. При физиологически протекающей беременности воздействие звуковым раздражителем на плод вызывает изменение ЧСС в пределах 15—20 уд/мин. Отсутствие изменений ЧСС или увеличение (не более чем на 1—8 уд/мин) свидетельствует о гипоксии плода. Звуковой тест, являющийся в настоящее время единственной функциональной пробой, неопосредованной через организм матери, реализуется через слуховой анализатор плода и может быть использован как для оценки интегративной функции слухового анализатора и ЦНС плода в целом, так и для оценки зрелости компенсаторно-приспособительных механизмов и слухового порога плода, коррелирующего с насыщением крови кислородом.
В
настоящее время установлено, что
значительное снижение двигательной
активности плода является угрожающим
признаком. Большую информативность
несут ощущения самой беременной шевелений
плода, поскольку совпадение ее
субъективных ощущений с данными
объективного исследования наблюдается
в 82—87% случаев. Беременная в течение 30
мин подсчитывает движения плода (5 или
более движений плода — показатель
хорошего состояния плода).
Достоверность оценки состояния плода повышается при комплексном анализе различных характеристик.
В 1980 г. Р. Маппищ и соавт. предложили оценивать биофизический профиль плода на основании 5 переменных величин (табл. 22) и рекомендовать лечение (табл. 23).
В последние годы в связи с разработкой и внедрением ультразвуковой диагностической аппаратуры появилась возможность неинвазивного измерения скорости кровотока в сосудах плода, пуповины, маточной артерии и на основании полученных данных выявлять ранние признаки нарушения кровообращения в системе мать—плацента—плод. Первое исследование рекомендуется проводить уже на 16—20-й неделе беременности, так как в этот период можно вы- явить нарушение в системе кровообращения плода еще до того, как возникли изменения фетометрических показателей. Допплерография позволяет выявить критическое состояние плода раньше, чем оно может быть установлено на основании КТГ плода. Допплерометрия помогает установить качественные изменения кровообращения плода. С помощью кордоцентеза (пункция пуповины), анализируя полученные пробы крови, можно получить количественные данные рН крови, гликемии, Рсо , Р0 . Однако применение этого метода, кроме наличия аппаратуры, требует высокой квалификации врача, поэтому пока используется в крупных акушерских стационарах.
Применение наиболее информативных биофизических методов контроля за состоянием плода не исключает параллельную оценку биохимических маркеров фетоплацентарной системы.
Определение
уровня активности окситоциназы (ОЦ)
сыворотки крови дает возможность
своевременно выявить плацентарную
недостаточность и провести ее коррекцию,
а также выбрать время для досрочного
прерывания беременности. Прогностически
неблагоприятным является отсутствие
роста активности ОЦ по мере прогрессирования
срока беременности, повышение ее по
сравнению с уровнем у здоровых женщин,
а также резкое понижение активности ОЦ
сыворотки крови.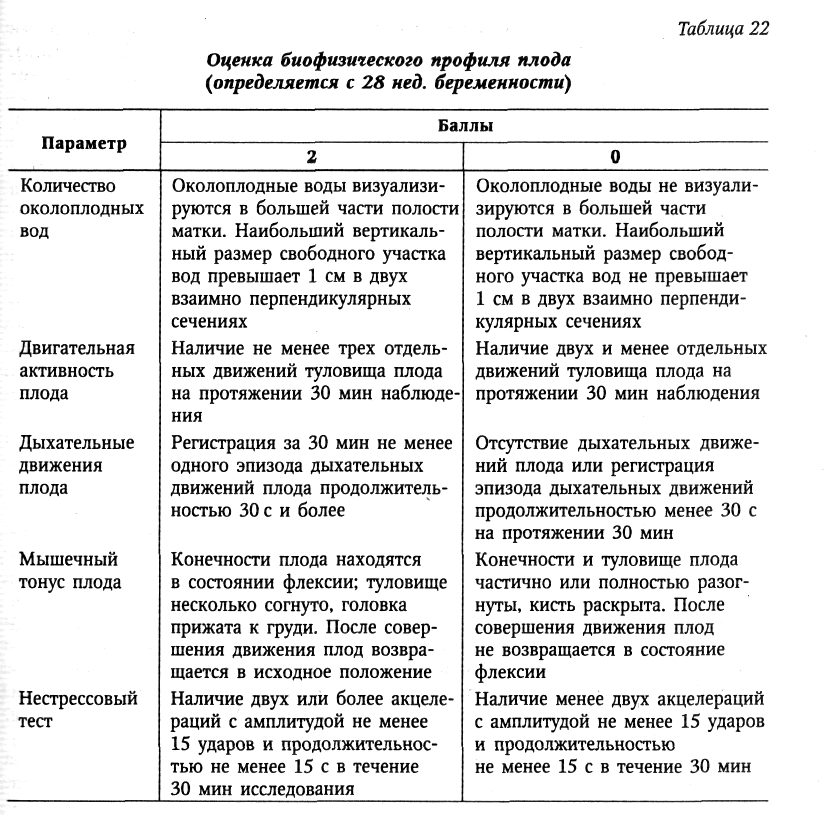
Внедрение в практику радиоизотопных методов диагностики позволило определять содержание плацентарного лактогена в сыворотке крови беременной. Концентрация его зависит от массы плаценты и срока беременности (в норме — 10 мгк/мл в 36 нед., с некоторым снижением к моменту родов). При плацентарной недостаточности уровень лактогена снижается в 2 раза, а при гипоксии плода — в 3 раза.
К современным методам оценки состояния плода относится и ультразвуковая диагностика, позволяющая определить величину бипариетального размера головки плода, толщину и площадь плаценты.
Указанные методы диагностики гипоксии плода применимы во время беременности и в I периоде родов, но наибольшее значение приобретают электро- и фонокардиография плода. Наиболее информативным является изменение ЧСС в ответ на схватку. Тахикардия (выше 180 уд/мин) и брадикардия (ниже 100 уд/мин) должны расцениваться как симптом тяжелой гипоксии.
В то же время только постоянное мониторное наблюдение или прямая электрокардиография позволяют четко выявить ранние симптомы начинающейся асфиксии плода. На фоне периодически изменяющейся базальной ЧСС плода выделяют 3 типа реакции сердечного ритма плода на шевеление или на схватку.
-
Раннее снижение ЧСС плода, синхронное со схватками, выражается замедлением ритма сердцебиения, возникает одновременно с началом схватки. В конце схватки восстанавливается первоначальная основная ЧСС. Этот чисто рефлекторный процесс является следствием повышения внутричерепного давления у плода во время схватки. Повышение давления оказывает возбуждающее действие на центр блуждающего нерва плода, что и приводит к временному замедлению ЧСС, не связанному с нарушением газообмена.
-
Позднее замедление ЧСС плода, возникающее после начала схватки и заканчивающееся с восстановлением базальной ЧСС через 20—40 с после завершения схватки. Эти изменения ритма сердечных сокращений плода связаны с нарушением маточно-плацентарного кровообращения. На развитие стаза в межворсинчатом пространстве, гипоксии, гиперкапнии требуется время, так же как и на восстановление первоначального уровня газообмена, что и проявляется изменением ЧСС плода.
3. Существует изменчивая форма снижения частоты; ее связывают с патологией пуповины.
Признаком гипоксии плода является позднее замедление ЧСС плода. Ценность этого признака состоит в возможности получения ранней информации о состоянии плода, когда ЧСС в паузе между схватками нормальна. Дополнением к электрокардиографии в родах в группах высокого риска является обнаружение мекония в околоплодных водах при головном предлежании плода, а также определение КОС крови плода, полученной из предлежащей головки. Повторное подтверждение ацидоза (рН <7,2) является показанием к немедленному родоразрешению.
Профилактика и лечение. Профилактика гипоксии плода заключается в выявлении и лечении осложнений беременности (поздние гестозы, резус-конфликт, перенашивание), эксграгенитальной патологии. В то же время имеется целый комплекс мероприятий, непосредственно направленных на улучшение плацентарно-маточного кровообращения, снятие метаболического ацидоза у плода.
Одним из компонентов лечения гипоксии плода остается кислородотерапия. Кислород необходимо вдыхать по 10—15 мин в количестве 10—12 л/мин с такими же интервалами. Длительное (более 30 мин) вдыхание чистого кислорода может привести к гипероксидации и к окислению сурфактанта, что снижает поверхностное натяжение альвеол и полноценное расправление легких. Чрезмерное насыщение крови плода кислородом приводит к снижению кровотока через артериальный проток, уменьшению сопротивления легочных сосудов плода, сужению сосудов пуповины.
С целью активации окислительно-восстановительных процессов, улучшения маточно-плацентарного кровообращения беременной или роженице внутривенно вводят глюкозу: либо 20—40 мл в виде 40% раствора струйно, либо 200—300 мл в виде 10% или 5% раствора капельно с добавлением 2—4 мл 1% раствора сигетина и соответствующих количеств инсулина или 3 мл 5% раствора унитиола и 3 мл 5% раствора аскорбиновой кислоты.
К средствам, улучшающим маточно-плацентарный кровоток, относятся токолитики (β-адреномиметики) — гинипрал, партусистен, беротек, алупент, а также эуфиллин, курантил, трентал.
С целью стимуляции созревания сурфактантной системы легких и профилактики дыхательной недостаточности новорожденных при лечении гипоксии плода у женщин с угрозой прерывания беременности до 36-недельного срока и при подготовке к досрочному родоразрешению необходимо использовать синтетический глюкокортикоид дексаметазон 4 раза в день в течение 3 сут. Последний прием "должен быть не позднее чем за 24 ч до родоразрешения. Разовая доза — 1 мг, суточная — 4 мг, курсовая — 12 мг. При затянувшихся преждевременных родах дексаметазон назначается по 1 мг через 6 ч. Последний прием дексаметазона должен быть проведен не менее чем за 6 ч до родоразрешения.
Для ускорения созревания легких плода используют также этимизол либо в виде ежедневных внутривенных инъекций — 1 мл 1,5% раствора в 1ОО мл изотонического раствора натрия хлорида или глюкозы, либо по 1/4 таблетки (0,025 г) 2 раза в день. За 3—4 ч до родоразрешения при выявлении гипоксии плода можно ввести внутривенно капельно 2 мл 1,5% этимизола в 200 мл 5% раствора глюкозы, тем самым уменьшить вероятность развития дыхательной недостаточности у новорожденных. Назначение дексаметазона и этимизола
особенно важно при проведении преждевременных родов, осложнившихся гипоксией плода.
Основными сурфактантами, участвующими в становлении функции внешнего дыхания, являются лецитин и сфингомиелин, о зрелости легких внутриутробного плода можно судить по коэффициенту лецитин/сфингомиелин (Л/С) после определения этих липидов в околоплодных водах. Соотношение 2:1 считается показанием к проведению профилактики синдрома дыхательной недостаточности.
При хронической гипоксии и гипотрофии плода дети рождаются с дефицитом массы за счет потери липидов, что предопределяет потребность в последних. Неблагоприятное соотношение между массой тела и его поверхностью вызывает необходимость в больших затратах энергии, основным источником которой у новорожденных также являются липиды. Увеличенный расход липидов способствует развитию гликемии. На этом основано использование экзогенных фосфолипидов (в виде эссенциале). Эссенциале способствует улучшению плацентарно-маточного кровообращения, транспортной функции плаценты и более быстрому становлению обменных процессов у плода, что выражается увеличением его массы. Схема применения эссенциале при хронической гипоксии и гипотрофии плода в III триместре беременности: 10 дней по 10 мл препарата (в ампулах) внутривенно в 200 мл 5% раствора глюкозы с одновременным применением его внутрь по 5 капсул ежедневно до родоразрешения. После родов показано продолжение лечения новорожденного: по 1—2 мл раствора эссенциале внутривенно в 5—10 мл 5% раствора глюкозы в течение 7 дней. Применение в общем комплексе эссенциале позволяет значительно повысить эффективность лечения хронической гипоксии на фоне отставания плода в развитии.
