- •Введение
- •Измерение физических величин и вычисление погрешностей
- •Определение погрешностей при прямых измерениях
- •Определение погрешностей при косвенных измерениях
- •Графическое изображение результатов работы
- •Оформление отчета по работе
- •Часть 1
- •Измерения и обработка результатов
- •Лабораторная работа №2 определение момента инерции махового колеса и силы трения в опоре
- •Краткая теория
- •Порядок выполнения работы.
- •Контрольные вопросы
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа № 4 опытная проверка уравнения бернулли
- •Краткая теория
- •Описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Порядок выполнения работы
- •Контрольные вопросы
- •Краткая теория
- •Описание лабораторной установки.
- •Порядок выполнения работы
- •Контрольные вопросы
- •Литература
- •Лабораторная работа №7 определение коэффициента внутреннего трения газа, средней длины свободного пробега и эффективного диаметра его молекул
- •Теоретическое введение. При движении слоев газа параллельно друг другу с различными по величине скоростями между ними возникают силы внутреннего трения (закон Ньютона)
- •Теория метода
- •Порядок выполнения работы.
- •Контрольные вопросы.
- •Литература
- •Лабораторная работа № 8 определение отношения удельных теплоемкостей газа методом адиабатического расширения.
- •Порядок выполнения работы
- •Контрольные вопросы
- •Порядок выполнения работы
- •Контрольные вопросы
Порядок выполнения работы
Открыть кран Д, при закрытом кране С накачать воздух в баллон так, чтобы разность уровней жидкости в манометре составила 30-40 мм.
Закрыть кран Д и выждать 2-3 минуты, пока благодаря теплообмену температура в баллоне не станет равной комнатной, и уровни в коленах манометра перестанут изменяться.
Отсчитать разность уровней Н жидкости в коленах манометра.
Открыть кран С и в тот момент, когда уровни жидкости обоих коленах манометра сравняются, быстро закрыть кран С.
Выждать 2-3 минуты пока газ, охлажденный про адиабатическом расширении, нагреется до комнатной температуры
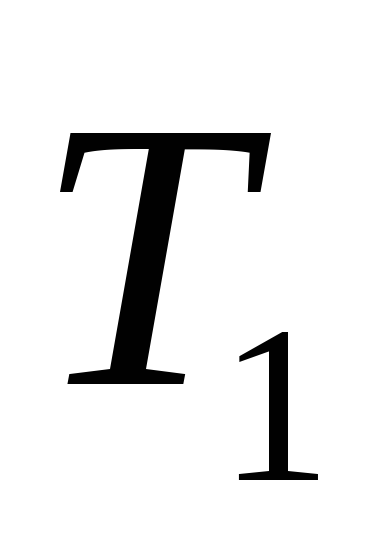 и отсчитать разность уровней h
жидкости в коленах манометра.
и отсчитать разность уровней h
жидкости в коленах манометра.По формуле (8) вычислить значение
 .
.Опыт повторить 5-7 раз, меняя величину Н.
Все полученные опытом (и вычислением) результаты измерений занести в таблицу отчета.
Таблица
-
№ опыта
H, мм
h, мм

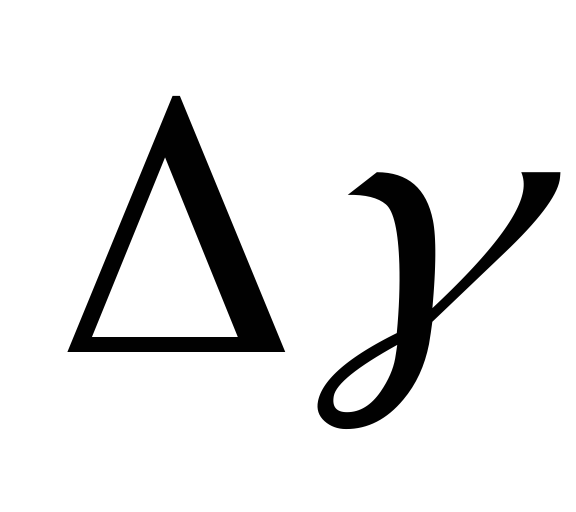

E, %
Контрольные вопросы
Что называется удельной теплоемкостью?
Запишите и сформулируйте I начало термодинамики
Почему
 ?
?Какой процесс называется адиабатическим? Запишите уравнение Пуассона.
Почему температура газа при адиабатном расширении уменьшается?
 P
P
 1(P
1(P![]() ,V
,V![]() ,T
,T![]() )
)
 3(P
3(P![]() ,V
,V![]() ,T
,T![]() )
)
 2(P,V
2(P,V![]() ,T
,T![]() )
)
V
Рис. 2
Литература
Шубин А.С. Курс общей физики.
Савельев И.В. Курс физики, т.1
Детлаф А.А., Яворский Б.М. Курс физики, т.1.
ЛАБОРАТОРНАЯ РАБОТА № 9
ОПРЕДЕЛЕНИЕ ПРИРАЩЕНИЯ ЭНТРОПИИ ПРИ
НАГРЕВАНИИ И ПЛАВЛЕНИИ ОЛОВА.
Приборы и принадлежности:
тигель с оловом, смонтированный в микроэлектропечи;
термопара;
сосуд с маслом;
милливольтметр;
градуировочный график термопары;
автотрансформатор и амперметр.
Цель работы: определение приращения энтропии при фазовом переходе первого рода на примере плавления олова.
Теория метода и описание установки
В
середине прошлого века было сделано
существенное открытие, касающееся
обратимых термодинамических процессов.
Оказалось, что наряду с внутренней
энергией у тела имеется еще одна
замечательная функция состояния –
энтропия.
Если тело или система при бесконечно
малом переходе из одного состояния в
другое при температуре Т получает тепло
dQ,
то отношение
![]() является полным дифференциалом некоторой
функции S.
Эта функция и есть энтропия,
определяющаяся одним из двух эквивалентных
равенств:
является полным дифференциалом некоторой
функции S.
Эта функция и есть энтропия,
определяющаяся одним из двух эквивалентных
равенств:
![]() ,
,
![]() (1)
(1)
Утверждение
о существовании функции, дифференциал
которой есть
![]() ,
носит название принципа существования
энтропии и является одним из важнейших
законов природы.
,
носит название принципа существования
энтропии и является одним из важнейших
законов природы.
Энтропия изолированной системы при любых происходящих в ней процессах не может убывать:
![]()
Это утверждение носит название закона возрастания энтропии или второго начала термодинамики.
Энтропию в кинетической теории или статистической механике отождествляют со степенью хаотичности движения в системе. Энтропия системы мала, когда движение в системе упорядоченно или когда распределение частиц в ней по скоростям маловероятно. В физических процессах упорядоченные системы стремятся стать неупорядоченными. Энтропия является количественной мерой степени молекулярного беспорядка в системе.
В
данной работе нужно найти изменение
энтропии
![]() при нагревании и плавлении олова.
при нагревании и плавлении олова.
![]() ,
(2)
,
(2)
где
![]() - приращение энтропии при нагревании
олова от комнатной температуры
- приращение энтропии при нагревании
олова от комнатной температуры![]() до температуры плавления
до температуры плавления![]() ;
;
![]() -
приращение энтропии при плавлении
олова.
-
приращение энтропии при плавлении
олова.
Согласно формуле (1):
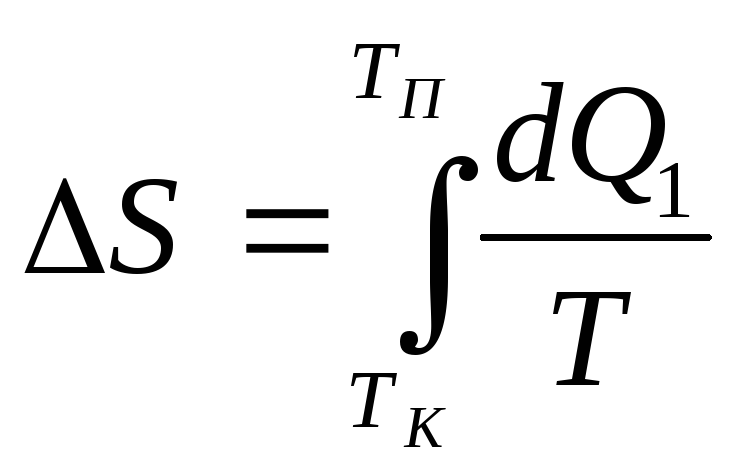 +
+
![]() =
= +
+![]() =
=![]() +
+![]() ,
(3)
,
(3)
где
dQ![]() и dQ
и dQ![]() - бесконечно малые количества теплоты,
полученные при нагревании и плавлении;
- бесконечно малые количества теплоты,
полученные при нагревании и плавлении;
![]() -
комнатная температура;
-
комнатная температура;
![]() - температура плавления;
- температура плавления;
с - удельная теплоемкость олова;
![]() -
удельная теплота плавления олова;
-
удельная теплота плавления олова;
m - масса олова.
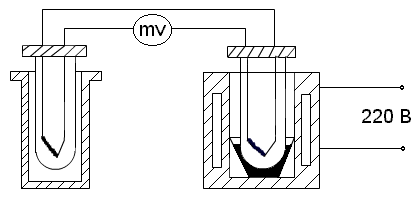
Рабочая схема установки показана на рисунке. Температура олова измеряется при помощи термопары, один спай которой погружают в тигель с оловом, а другой спай – в сосуд с маслом, в котором практически сохраняется комнатная температура. Термо - э.д.с., возникающая в цепи термопары при наличии разности температур в спаях, измеряется милливольтметром.