
прописанные экзаменационные билеты / 59
.docБилет №59
-
Изменение частоты и ритма дыхания. Дыхание Чейн-Стокса, Биота, Куссмауля. Патогенез. Диагностическое значение.
Поражение головного мозга нередко ведет к нарушениям ритма дыхания. Особенности возникающего при этом патологического дыхательного ритма могут способствовать топической диагностике, а иногда и определению характера основного патологического процесса в мозге.
Дыхание Куссмауля (большое дыхание) — патологическое дыхание, характеризующееся равномерными редкими регулярными дыхательными циклами: глубоким шумным вдохом и усиленным выдохом. Наблюдается обычно при метаболическом ацидозе вследствие неконтролируемого течения сахарного диабета или хронической почечной недостаточности у больных в тяжелом состоянии в связи с дисфункцией гипоталамического отдела мозга, в частности при диабетической коме. Этот тип дыхания описал немецкий врач A. Kussmaul (1822—1902).
Дыхание Чейна-Стокса — периодическое дыхание, при котором чередуются фазы гипервентиляции (гиперпноэ) и апноэ. Дыхательные движения после очередного 10—20-секундного апноэ имеют нарастающую, а после достижения максимального размаха — уменьшающуюся амплитуду, при этом фаза гипервентиляции обычно длительнее фазы апноэ. При дыхании Чейна—Стокса чувствительность дыхательного центра к содержанию С02 всегда повышена, средний вентиляционный ответ на С02 примерно в 3 раза выше нормы, минутный объем дыхания в целом всегда повышен, постоянно отмечаются гипервентиляция и газовый алкалоз. Дыхание Чейна—Стокса обычно обусловлено нарушением нейрогенного контроля за актом дыхания в связи с интракра-ниальной патологией. Причиной его могут быть и гипоксемия, замедление кровотока и застойные явления в легких при сердечной патологии. F. Plum и соавт. (1961) доказали первичное нейрогенное происхождение дыхания Чейна—Стокса. Кратковременно дыхание Чейна—Стокса может наблюдаться и у здоровых, но непреодолимость периодичности дыхания всегда является следствием серьезной мозговой патологии, ведущей к снижению регулирующего влияния переднего мозга на процесс дыхания. Дыхание Чейна—Стокса возможно при двустороннем поражении глубинных отделов больших полушарий, при псевдобульбарном синдроме, в частности при двусторонних инфарктах мозга, при патологии в диэнцефальной области, в стволе мозга выше уровня верхней части моста, может быть следствием ишемических или травматических повреждений этих структур, нарушений метаболизма, гипоксии мозга в связи с сердечной недостаточностью, уремией и др. При супратенториальных опухолях внезапное развитие дыхания Чейна—Стокса может быть одним из признаков начинающегося транстенториального вклинения. Периодическое дыхание, напоминающее дыхание Чейна—Стокса, но с укороченными циклами может быть следствием выраженной внутричерепной гипертензии, приближающейся к уровню перфузионного артериального давления в мозге, при опухолях и других объемных патологических процессах в задней черепной ямке, а также при кровоизлияниях в мозжечок. Периодическое дыхание с гипервентиляцией, чередующейся с апноэ, может быть и следствием поражения понтомедуллярного отдела ствола мозга. Этот тип дыхания описали шотландские врачи: в 1818 г. J. Cheyne (1777-1836) и несколько позже - W. Stokes (1804-1878).
Биотовское дыхание — форма периодического дыхания, характеризующегося чередованием учащенных равномерных ритмических дыхательных движений с длительными (до 30 с и более) паузами (апноэ).
Наблюдается при органических поражениях мозга, расстройствах кровообращения, тяжелых интоксикациях, шоке и других патологических состояниях, сопровождающихся глубокой гипоксией продолговатого мозга, в частности расположенного в нем дыхательного центра. Эту форму дыхания описал французский врач С. Biot (род. в 1878 г.) при тяжелой форме менингита.
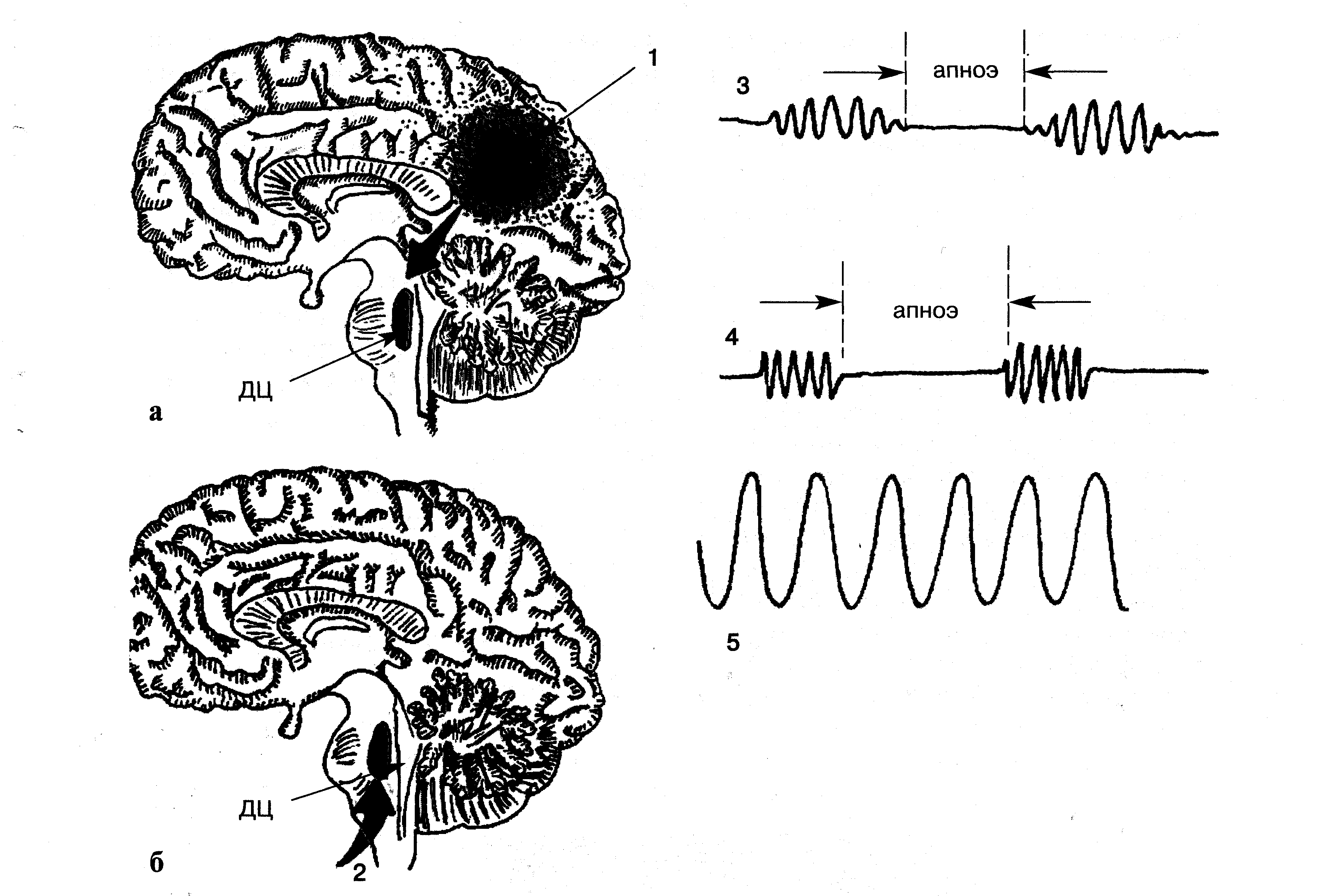
3 – дыхание Чейна-Стокса; 4 – дыхание Биота; 5 – дыхание Куссмауля.
-
Нефротический синдром: определение, патогенез, причины, клиническая и диагностика.
Нефротический синдром – это клинико-лабораторный симптомокомплекс, для которого характерны тяжелая протеинурия (более 3,0-3,5 г/сутки или 50 мг на 1 кг массы тела в сутки), гипопротеинемия (менее 60 г/л), гипоальбуминурия (менее 30 г/л), отеки, гиперлипидемия (гиперхолестеринемия и гипертриглицеридемия), холестеринурия.
Нефротический синдром (НС) развивается при вовлечении в патологический процесс клубочковых структур.
Наиболее частые заболевания, сопровождающиеся НС:
-
хронический гломерулонефрит
-
диабетическая нефропатия
-
отравление нефротоксическими ядами и лекарственными веществами
-
амилоидоз почек
-
нефропатия беременных
-
осложнения системных заболеваний соединительной ткани
Ведущим звеном патогенеза НС является повреждение гломерулярного фильтра, что обусловливает потерю белка с мочой. Первоначально через поврежденный фильтр теряется белок с самой малой молекулярной массой – альбумин (селективная протеинурия). Потеря белка вызывает снижение его содержания в крови (гипопротеинемия) и снижение онкотического давления плазмы, что способствует транссудации воды в ткани, появление отеков. Уменьшение объема циркулирующей крови (ОЦК), стимулирует повышение выработки антидиуретического гормона и активности ренин-ангиотензиновой и альдостероной систем. Механизм гормональной активации направлен на повышение реабсорбции воды для поддержания ОЦК. Так как гломерулярный фильтр остается поврежденным, это лишь усугубляет дальнейший выход жидкости в ткани с увеличением степени отеков. Снижение онкотического давления крови стимулирует в печени синтез белков и липидов, последнее приводит к гиперлипидемии, и как следствие холестеринурии.
К основным лабораторным признакам НС (протеинурия, гипоальбуминемия, гиперлипидемия, холестеринурия) также относят:
-
ОАК: гипохромная анемия за счет потери с мочой трансферрина, усиленной экскреции с мочой эритропоэтинов, плохого всасывания железа в ЖКТ; увеличение СОЭ до 50-60 мм\ч. Лейкоцитарная формула не претерпевает особых изменений.
-
В биохимическом анализе крови снижается содержание кальция, железа, кобальта, цинка, за счет нарушения метаболизма витамина D и фосфорно-кальциевого обмена;
-
Коагулограмм: гиперагрегация тромбоцитов, снижение антикоагулянтных свойств крови.
-
ОАМ: реакция чаще щелочная вследствие электролитных сдвигов. Относительная плотность мочи до присоединения ХПН обычно высокая. При гломерулонефрите встречается эритроцитурия. Возможна лейкоцитурия, которая опосредована протеинурией и не имеет связи с инфекционной природой.
-
Пароксизмальные тахикардии (желудочковые и наджелудочковые): критерии ЭКГ.
Пароксизмальные тахикардии – приступы учащенного сердцебиения правильного ритма с частотой от 140 до 220 в минуту. Источником является гетеротопный очаг возбуждения в предсердиях либо желудочках. Клинически проявляется приступом сердцебиения с ЧСС более 140 в минуту, гемодинамическими расстройствами (слабость, головокружение, одышка в покое, гипотония, возможен коллапс, либо аритмогенный шок). Приступ проходит либо внезапно, спонтанно, либо под воздействием вагусных проб (Вальсальвы, массаж каротидного синуса). На ЭКГ при наджелудочковой тахикардии – правильный ритм, деформированный зубец Р, узкий комплекс QRS (до 0,1 сек). При желудочковой – правильный ритм, отсутствие зубца Р, комплекс QRS шире 0,1 сек, с дискордантными зубцами.
