- •Специфика органической химии
- •Теория гибридизации
- •Типы гибридных орбиталей
- •Первое валентное состояние атома углерода Гибридизация sp3
- •Мезомерный эффект (эффект сопряжения) [±m]
- •Понятие сопряжения
- •Эффекты сопряжения
- •Правило Морковникова
- •Донорно-акцепторные связи. Семиполярные связи
- •Водородная связь
- •Названия ненасыщенных и ароматических углеводородов
- •Номенклатура гетероциклических соединений
- •Номенклатура июпак для производных различных классов органических соединений
- •Изомерия органических соединений
- •Структурная изомерия
- •Изомерия положения
- •Геометрическая изомерия (зеркальная, цис- транс- изомерия)
- •Оптическая изомерия
- •Устройство поляриметра
- •Диастереомеры
- •Номенклатура стереоизомеров
- •Номенклатура Кана, Ингольда, Прелога (кип)
- •Номенклатура стереоизомеров Потапова в.М., Терентьева а.П. И сотрудников
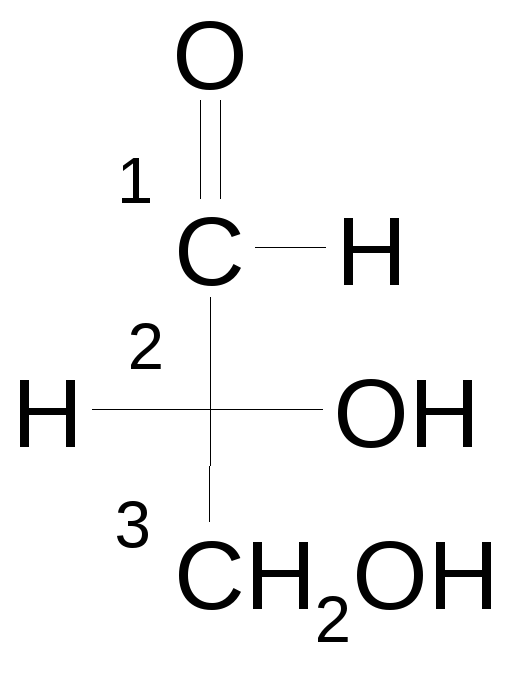
- •2(Ρ),3-диоксипропаналь
- •3(Ρ),4-дихлорпентен-4-аль
- •Классификация органических реакций и реагентов
- •По способу разрыва (образования) химических связей.
- •Классификация реакций по типу превращений в органических веществах
- •Свободные радикалы
- •Понятие о граничных структурах
- •Алканы (парафины)
- •Физические свойства
- •Промышленная переработка алканов (нефти)
- •Некоторые лабораторные способы получения алканов
- •Нитрование алканов
- •Строение малых циклов (циклопропан, циклобутан)
- •Некоторые закономерности реакции отщепления
- •Дегидратация спиртов (отщепление воды)
- •Дегалогенирование дигалогенпроизводных
- •Восстановление алкинов (ацетиленов)
- •Расщепление четвертичных аммонийных солей по Гофману
- •Присоединение галогенов
- •Строение диенов
- •Химические свойства диенов
- •Реакции присоединения
- •Механизм реакции [ae] для сопряженных диенов
- •Некоторые аспекты применения сопряженных диенов
- •Алкины (ацетилены)
- •Способы получения ацетилена
- •Некоторые способы получения гомологов ацетилена
- •Общая характеристика реакционной способности ацетиленов
- •Физические свойства ацетилена
- •Химические свойства
- •Реакции присоединения
- •Реакции нуклеофильного присоединения к ацетиленам
- •Некоторые свойства виниловых эфиров
- •Ароматические углеводороды
- •Признаки ароматичности
- •Направление реакций ароматических соединений
- •II стадия:
- •Мнемоническое правилосмещения электронной плотности под действием заместителя в ядре
- •Нуклеофильное замещение в ароматических системах (snAr)
- •Механизм реакции snAr
- •Галогенпроизводные углеводородов
- •Методы получения галогенпроизводных
- •Замещение водорода на галоген в условиях радикальных процессов (прямое галогенирование алканов)
- •Галогенирование непредельных углеводородов
- •Получение галогенпроизводных из непредельных углеводородов
- •Общая характеристика реакционной способности галогенпроизводных
- •Важнейшие реакции галогенпроизводных
- •Образование металлорганических соединений
- •Содержание
Номенклатура Кана, Ингольда, Прелога (кип)
Стереоизомер располагают в тетраэдре таким образом, чтобы младший заместитель находился в наиболее удаленной от наблюдателя вершине.
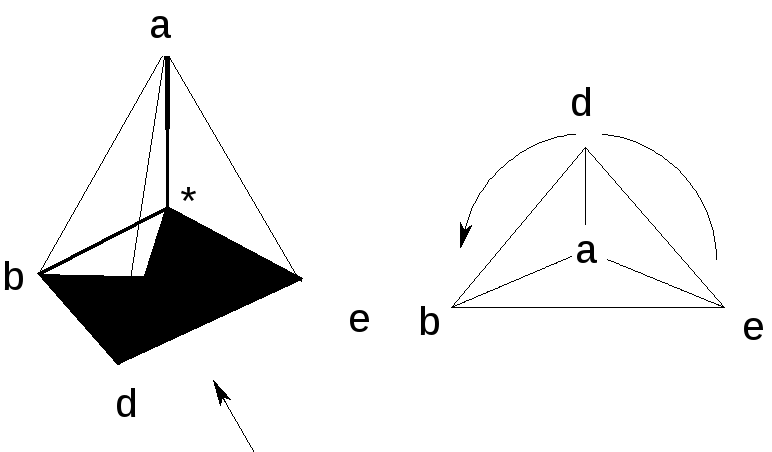
Для оставшихся трех заместителей (d,b,e) рассматривают изменение (в порядке уменьшения) их старшинства. При уменьшении старшинства по часовой стрелке, конфигурация асимметрического центра обозначается буквойR, противS. Если в приведенном примере старшинство убывает в рядуe>d>b>a, то изомер будет иметьSконфигурацию асимметрического центра.
При использовании проекционных формул Фишера для отнесения конфигурации по RS-номенклатуре меньший заместитель располагают внизу, а старшийслева от асимметрического центра.
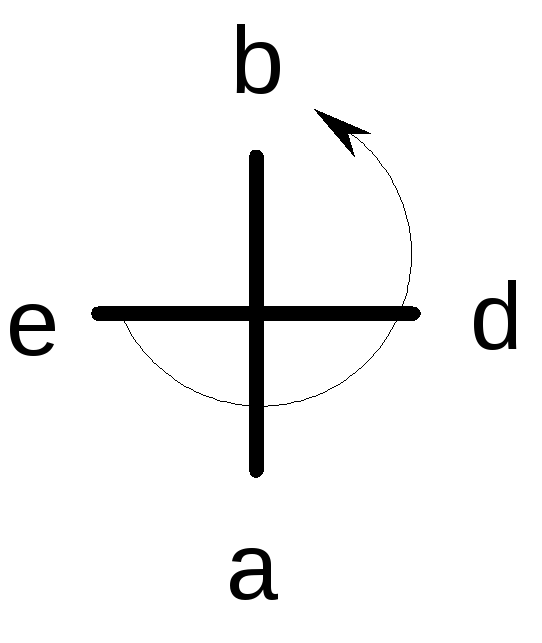
Старшинство заместителейопределяют по предложенной авторами системе, в основе которой лежит периодическая таблица Менделеева (по порядковому номеруэлемента).
В том случае, если элементы связаны двойной или тройной связью, то соответствующий атомный номер удваивается или утраивается.
Примечание:
В геометрической изомерии эта система используется для определения Z, E изомеров.
Пример 1:
Определим абсолютную конфигурацию D-глицеринового альдегида по номенклатуре КИП.
Примечание: заместители, расположенные в проекциях Фишера по горизонтали, направлены кнаблюдателю, по вертикалиотнаблюдателя.
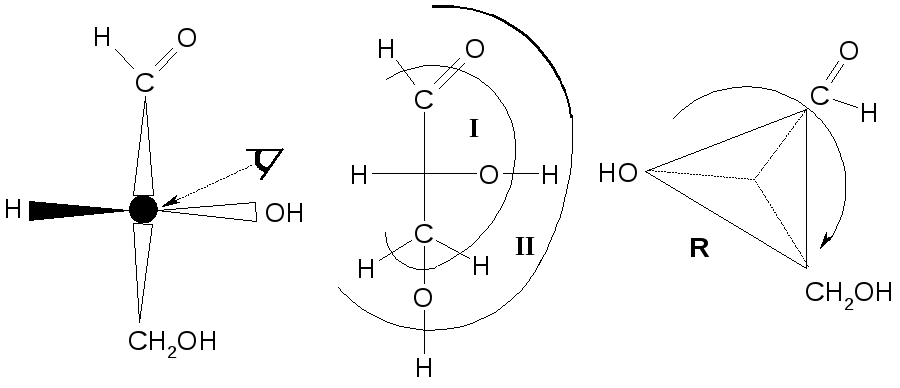
I слой:OH>XиY>H. ГдеX=COH,Y=CH2OH.
II слой:X=82+1=17;Y=6+1+1=8. Таким образом,COH>CH2OH.
Направление уменьшения старшинства заместителей – по часовой стрелке, поэтому, D-глицериновый альдегид имеетR-конфигурацию асимметрического центра.
Пример 2:
Определим конфигурацию хирального центра для (+)-D-яблочной кислоты (двухосновная кислота)
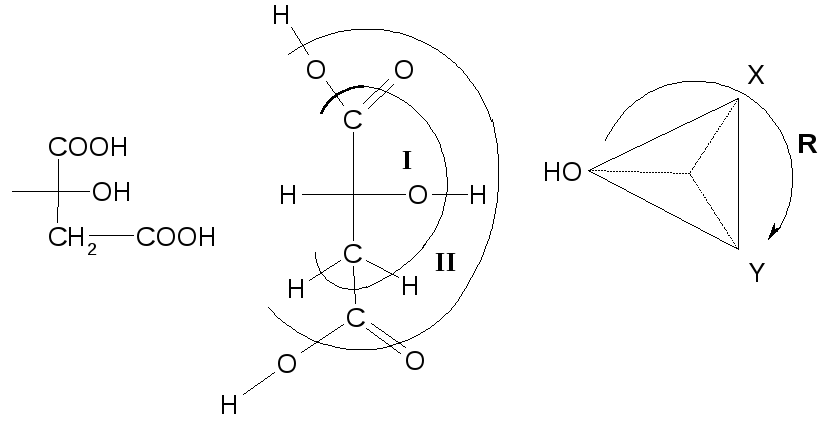
I слой: OH>X и Y>H. Где X=COOH, Y=CH2COOH.
II слой: X=82+8=24;Y=6+1+1=8. Таким образом,OH>X>Y>H.
Следовательно, асимметрический центр (+)-D-яблочной кислоты имеетR-конфигурацию.
Недостатки номенклатуры КИП:
Если автор ошибся в названии соединения по номенклатуре ИЮПАК, то читатель определяет конфигурацию хирального центра антипода.
При замене группы R, например, наBrконфигурация асимметрического центра не меняется, аабсолютнаяконфигурация (по номенклатуре КИП) измениться, так какBrиRимеют разные порядковые номера.
Значительные расхождения с номенклатурой ИЮПАК.
Номенклатура стереоизомеров Потапова в.М., Терентьева а.П. И сотрудников
Молекулу располагают таким образом, чтобы младший заместитель при асимметрическом центре был удален от наблюдателя, тогда при уменьшении старшинства остальных заместителей по часовой стрелке, конфигурацию асимметрического центра обозначают σ, против часовой стрелки ρ (σ,ρ-номенклатура).
Старшинство заместителей определяют с использованием номенклатуры ИЮПАК!
Начало цепи младше, чем конец цепи (т.е. чем старше номер, тем старше заместитель).
В проекционных формулах Фишера углеродную цепь располагают таким образом, чтобы нумерация цепи: шла сверху вниз.
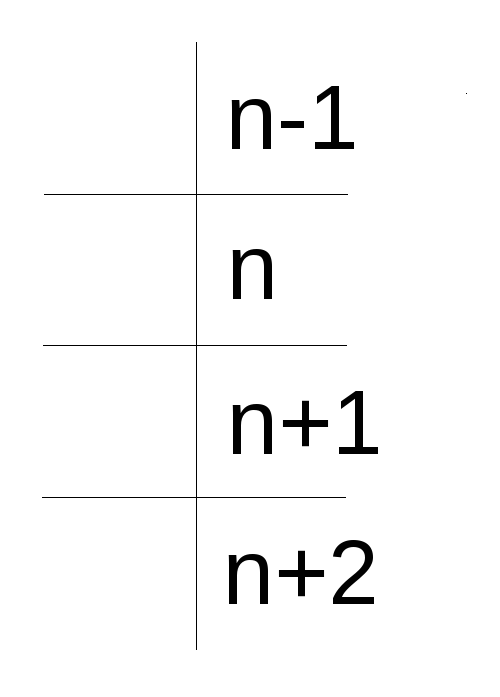
Для того, чтобы определить конфигурацию асимметрического центра, достаточно при обходе цепи сверху фиксировать положение заместителя. Если заместитель находится справа от основной цепи, то конфигурацию обозначают через ρ, если слева то через σ. Например, определим конфигурацию 2-бром-2-метилбутановой кислоты следующего строения:
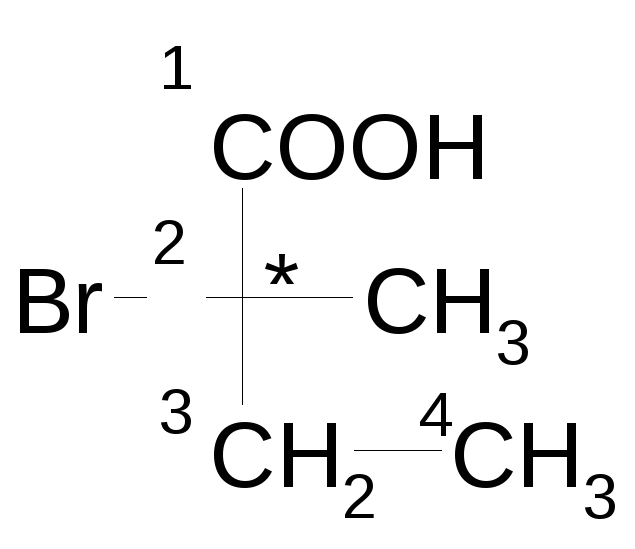
Обходим цепь слева: 2-(σ)-бром-2-метилбутановая кислота; справа - 2-бром-2-(ρ)-метилбутановая кислота. Оба названия правильны. С другой стороны, рассмотрим хиральный центр обычным способом:
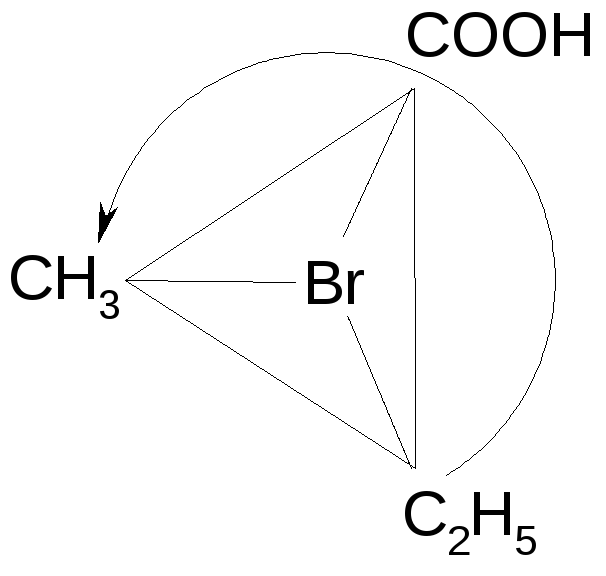
Углеводородные заместители превалируют над другими, кроме функциональных групп, то естьBr –младший заместитель. Таким образом определяем конфигурацию соединения как 2-бром-2-(ρ)-метилбутановая кислота.
При наличии в молекуле двух асимметрических центров пользуются правилом старшинства по порядковым номерам. Например:
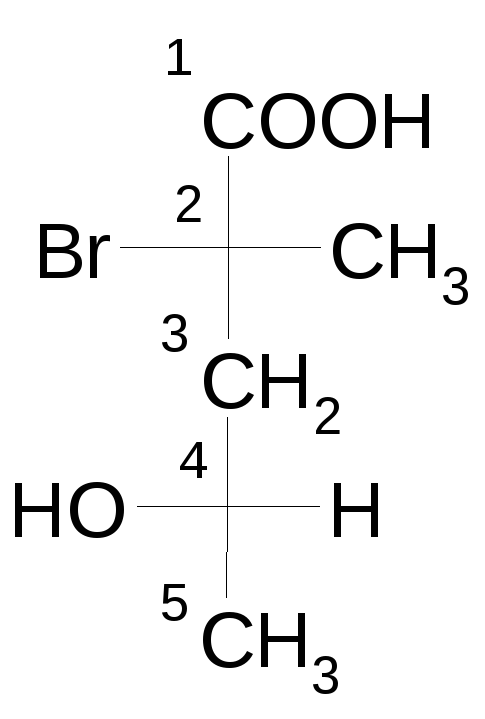
2-(σ)-бром-4-(σ)-гидрокси-2-метилпентановая кислота
Если цепь состоит из одного асимметрического атома углерода, заместители располагают таким образом, чтобы самый старший заместитель находился внизу, а атом водорода, если он есть, располагают слева или справа.
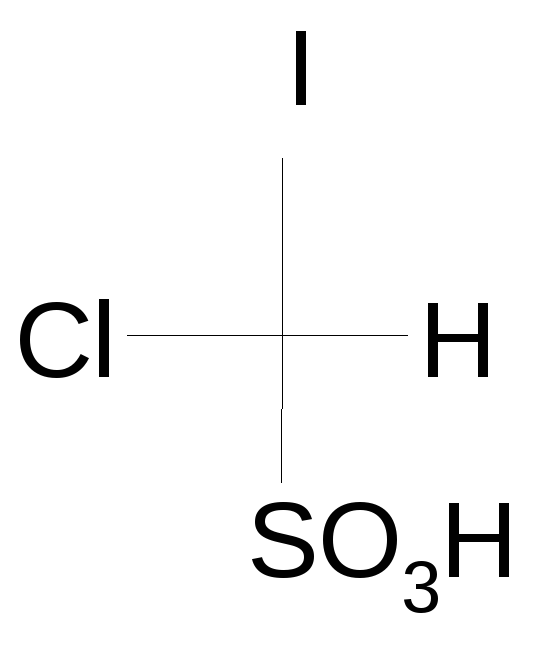
(σ)-хлориодметансульфокислота
Если цепь состоит из двух атомов углерода, то за начало цепи выбирается асимметрический центр.
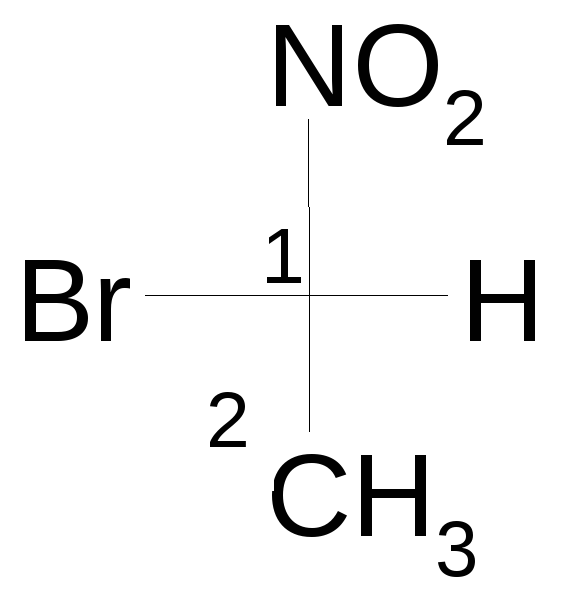
1-(σ)-бром-1-нитроэтан
Преимущества номенклатуры Потапова В.М. и др.:
1. Используется та же система определения старшинства, как и в номенклатуре ИЮПАК.
2. Если автор ошибся в нумерации цепи, то читатель по данному названию сможетопределить формулу вещества и конфигурацию асимметрических центров.
Определим конфигурацию асимметрического центра D-глицеринового альдегида: