
- •Специфика органической химии
- •Теория гибридизации
- •Типы гибридных орбиталей
- •Первое валентное состояние атома углерода Гибридизация sp3
- •Мезомерный эффект (эффект сопряжения) [±m]
- •Понятие сопряжения
- •Эффекты сопряжения
- •Правило Морковникова
- •Донорно-акцепторные связи. Семиполярные связи
- •Водородная связь
- •Названия ненасыщенных и ароматических углеводородов
- •Номенклатура гетероциклических соединений
- •Номенклатура июпак для производных различных классов органических соединений
- •Изомерия органических соединений
- •Структурная изомерия
- •Изомерия положения
- •Геометрическая изомерия (зеркальная, цис- транс- изомерия)
- •Оптическая изомерия
- •Устройство поляриметра
- •Диастереомеры
- •Номенклатура стереоизомеров
- •Номенклатура Кана, Ингольда, Прелога (кип)
- •Номенклатура стереоизомеров Потапова в.М., Терентьева а.П. И сотрудников
- •2(Ρ),3-диоксипропаналь
- •3(Ρ),4-дихлорпентен-4-аль
- •Классификация органических реакций и реагентов
- •По способу разрыва (образования) химических связей.
- •Классификация реакций по типу превращений в органических веществах
- •Свободные радикалы
- •Понятие о граничных структурах
- •Алканы (парафины)
- •Физические свойства
- •Промышленная переработка алканов (нефти)
- •Некоторые лабораторные способы получения алканов
- •Нитрование алканов
- •Строение малых циклов (циклопропан, циклобутан)
- •Некоторые закономерности реакции отщепления
- •Дегидратация спиртов (отщепление воды)
- •Дегалогенирование дигалогенпроизводных
- •Восстановление алкинов (ацетиленов)
- •Расщепление четвертичных аммонийных солей по Гофману
- •Присоединение галогенов
- •Строение диенов
- •Химические свойства диенов
- •Реакции присоединения
- •Механизм реакции [ae] для сопряженных диенов
- •Некоторые аспекты применения сопряженных диенов
- •Алкины (ацетилены)
- •Способы получения ацетилена
- •Некоторые способы получения гомологов ацетилена
- •Общая характеристика реакционной способности ацетиленов
- •Физические свойства ацетилена
- •Химические свойства
- •Реакции присоединения
- •Реакции нуклеофильного присоединения к ацетиленам
- •Некоторые свойства виниловых эфиров
- •Ароматические углеводороды
- •Признаки ароматичности
- •Направление реакций ароматических соединений
- •II стадия:
- •Мнемоническое правилосмещения электронной плотности под действием заместителя в ядре
- •Нуклеофильное замещение в ароматических системах (snAr)
- •Механизм реакции snAr
- •Галогенпроизводные углеводородов
- •Методы получения галогенпроизводных
- •Замещение водорода на галоген в условиях радикальных процессов (прямое галогенирование алканов)
- •Галогенирование непредельных углеводородов
- •Получение галогенпроизводных из непредельных углеводородов
- •Общая характеристика реакционной способности галогенпроизводных
- •Важнейшие реакции галогенпроизводных
- •Образование металлорганических соединений
- •Содержание
Нитрование алканов
Парофазное нитрование.
Проводят при температурах до 400 С и давлении. В продуктах реакции присутствуют соединения с меньшим количеством атомов углерода (деструкция):
![]()
Жидкофазное нитрование.
Проводят при t=125С и давленииP=14 атм (реакция Коновалова). В этих условиях образуются нитропроизводные с тем же числом атомов углерода. Реакция протекает селективно, с преимущественным образованием третичных нитропроизводных.
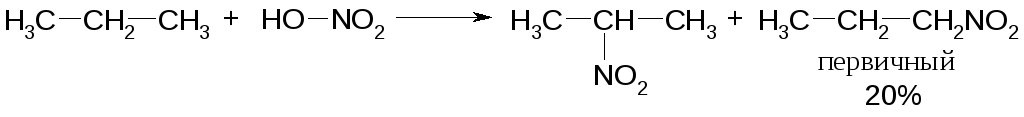
Сульфирование алканов
Проводится с целью получения моющих средств и детергентов.
![]()
Длина цепочки R=C8C14
Реакция носит радикальный характер.
Окисление алканов
Представляет собой сложный процесс в результате которого образуются спирты, альдегиды, кетоны, карбоновые кислоты. В каталитических процессах окисление воздухом или кислородом в основном образуются карбоновые кислоты. Промежуточными продуктами в реакции являются свободные радикалы и пироксисоединения:
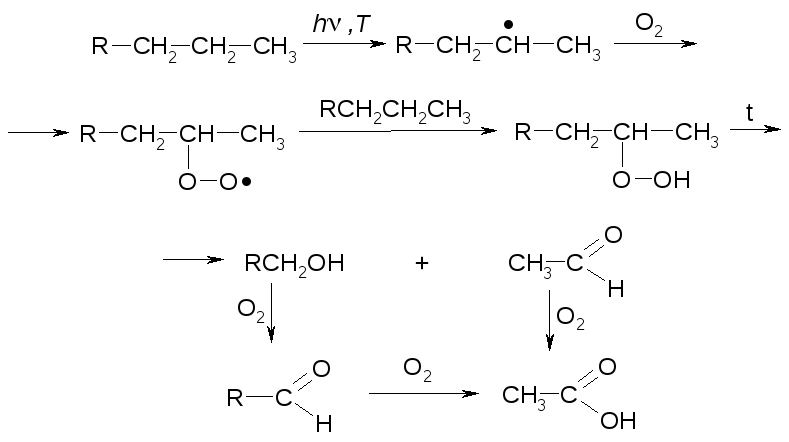
Циклоалканы
В небольших количествах содержатся в нефти.
Основные способы получения
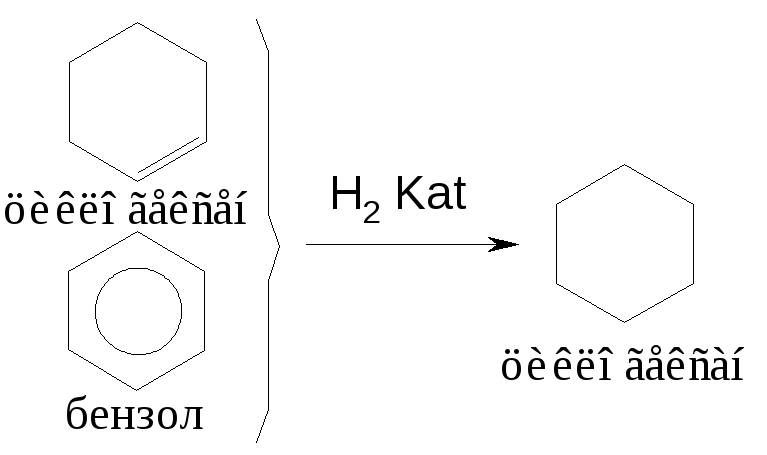
Гидрирование непредельных циклических и ароматических углеводородов
Катализаторы гидрирования:
NiReникель Ренея. Используют для гидрирования при повышенных температурах (до 120С) и избыточном давлении (до 250 атм).
Катализаторы на основе благородных металлов палладий, платинаработают при нормальных условиях.
Реакции расширения цикла (внедрения)
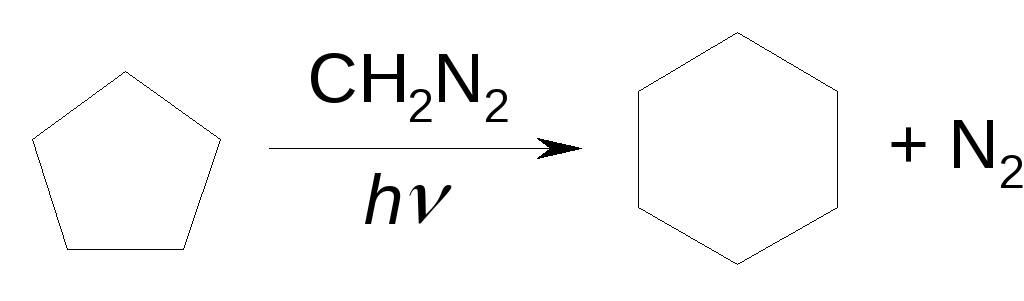
Дорогостоящий способ с применением диазаметана широко применяется в лабораторной практике.
Реакции циклизации
Реакция Вюрца-Густавсона
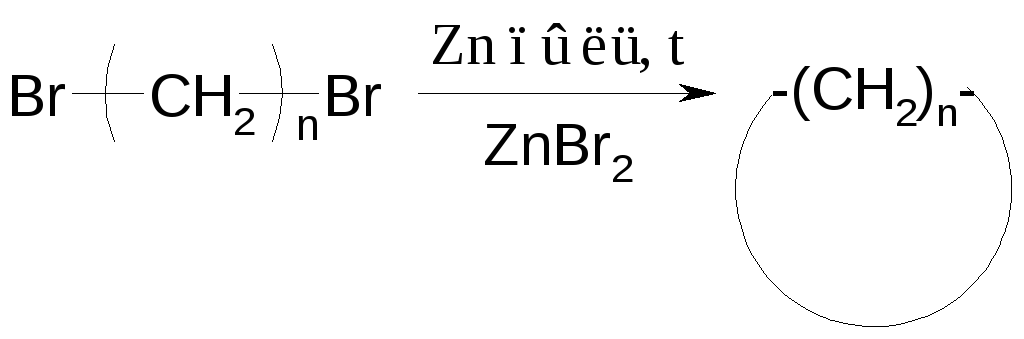
Реакция Дикмана
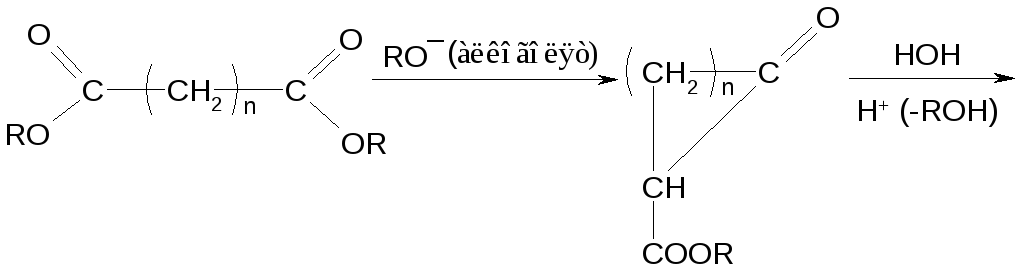
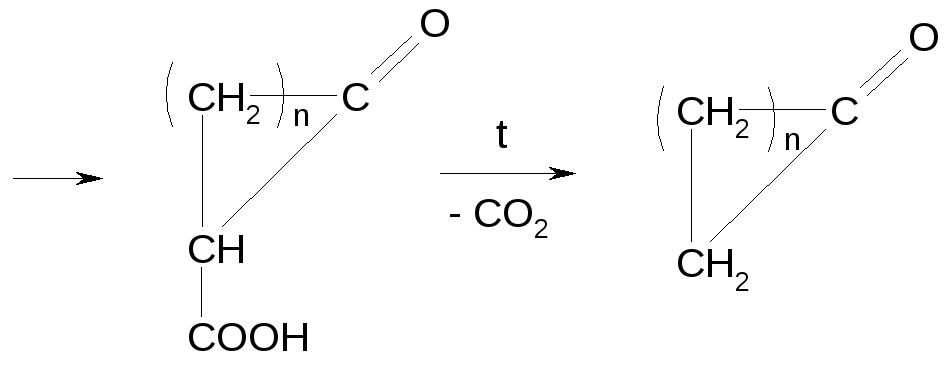
Восстановление циклического кетона амальгамами приводит к циклоалканам.
Строение циклических углеводородов
Согласно теории напряжений циклов Байерасчиталось, что циклы являются плоскими, поэтому наиболее устойчивым считался циклопентан (у которого плоский валентный угол 108).
Предсказание Байера оказалось не совсем точным, т.к. циклы существуют в конформациях, с валентным углом близким к 10928’.
Самый устойчивый циклогексан. Конформации циклогексана:
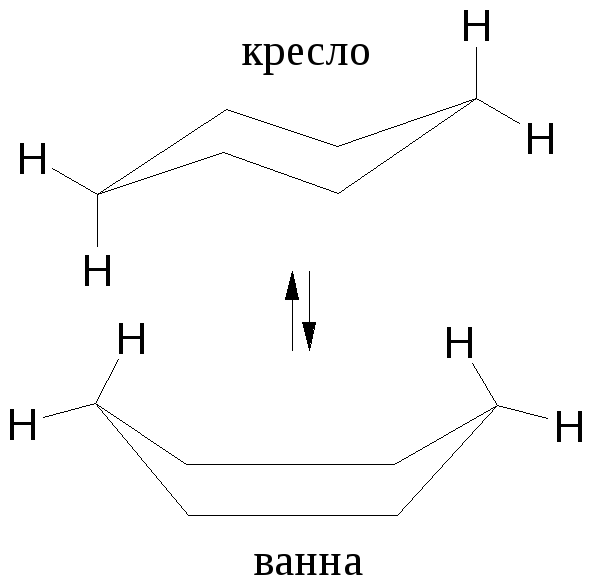
Конформация «кресла» более устойчива, поскольку в нем отсутствует взаимодействие атомов водорода при С1С4.
Циклопентан находится в конформациях скошенного типа «гош»:
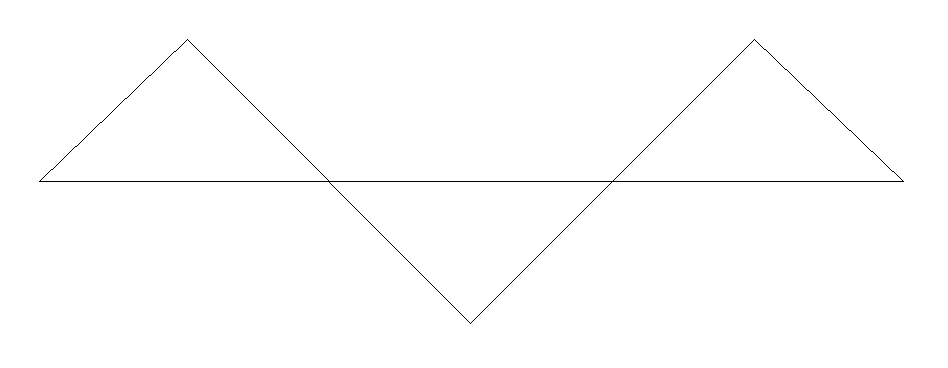
или «конверт»:
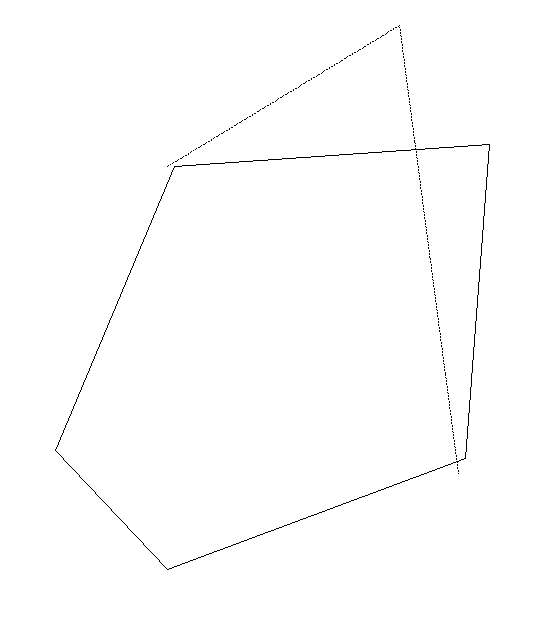
Строение малых циклов (циклопропан, циклобутан)
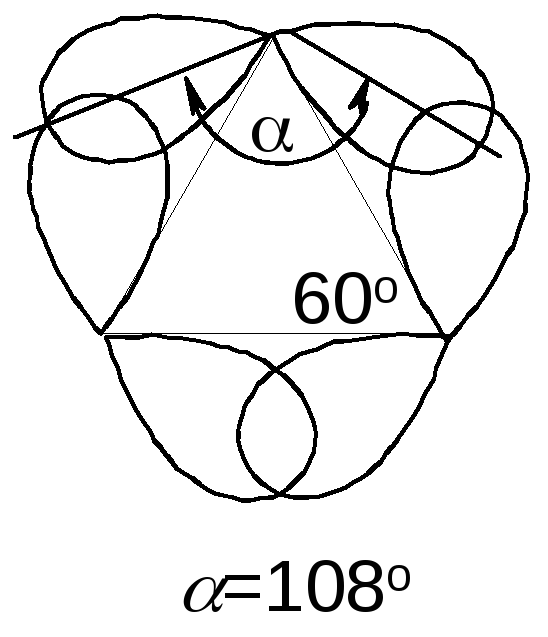
Связи в малых циклах отличаются от
простых σ-связей;
п
σ
Гидрирование:
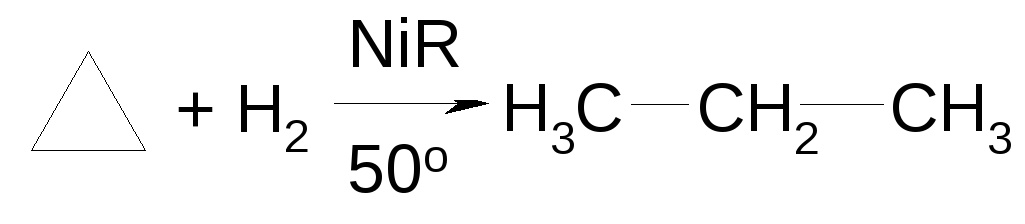
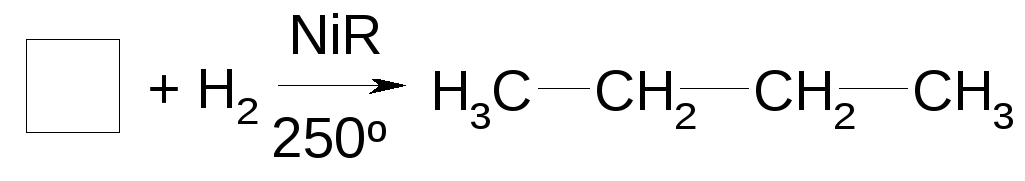
По тому же принципу проходят реакции бромироваия и гидрогалогенирования.
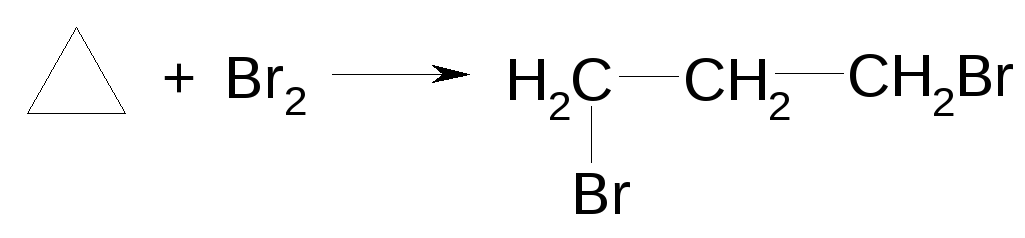
![]()
Для циклобутана подобные реакции не идут.
Основные реакции средних циклов (циклопентан, циклогексан)
Химические реакции средних циклов в основном схожи с реакциями алканов.
Дегидрирование на катализаторах

Галогенирование
Реакция протекает по схеме, аналогичной алканам
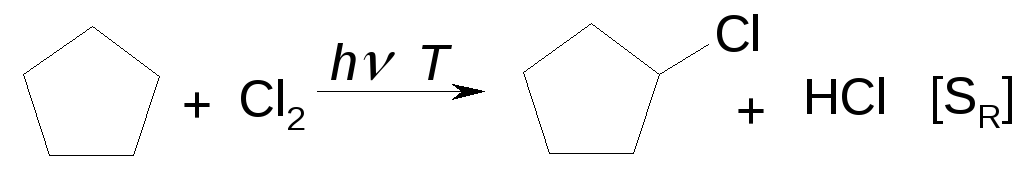
[SR] – радикальное замещение
Реакции с диазометаном
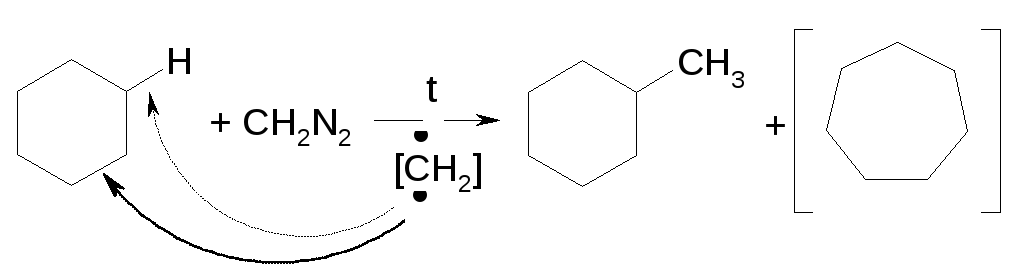
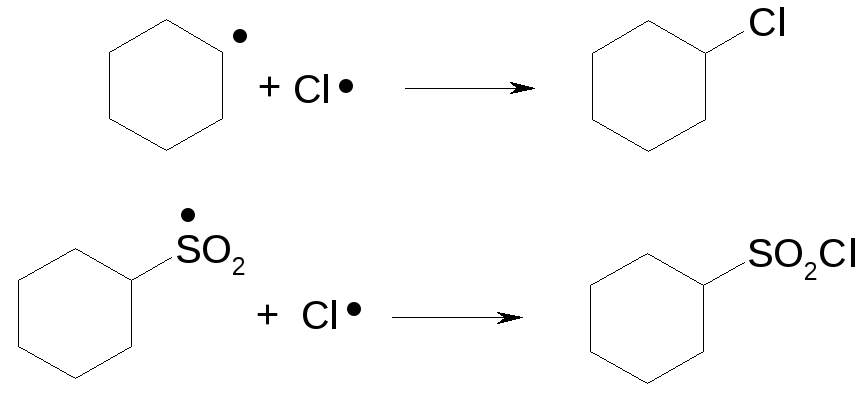
Реакции сульфохлорирования
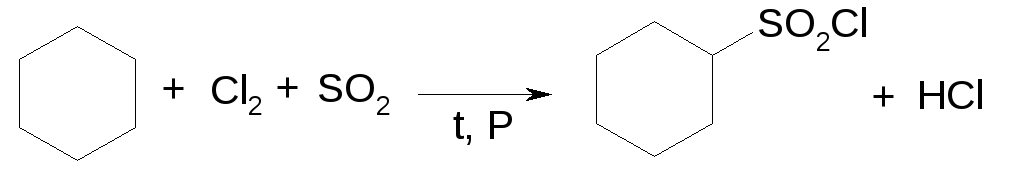
Механизм:
Инициация
![]()
Рост и развитие цепи
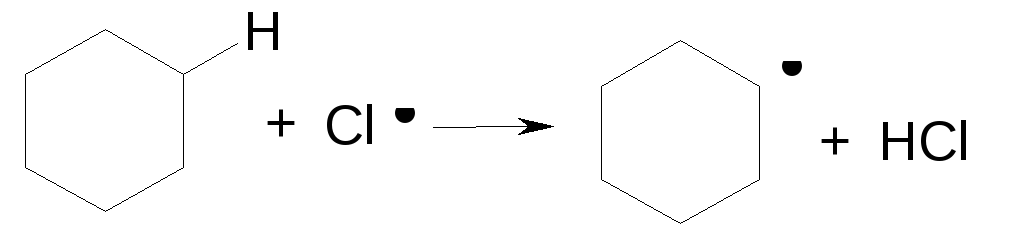
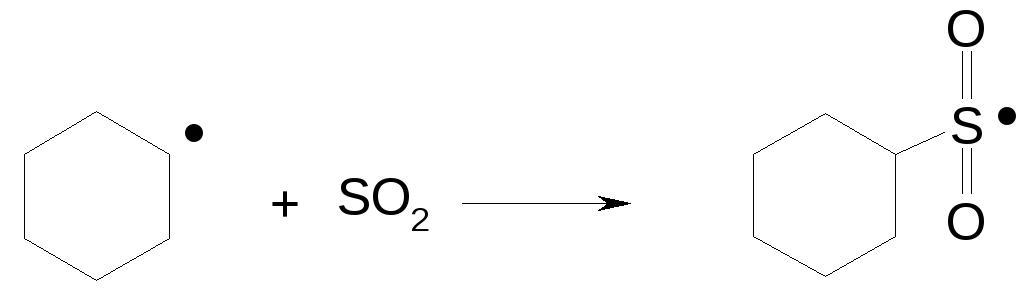
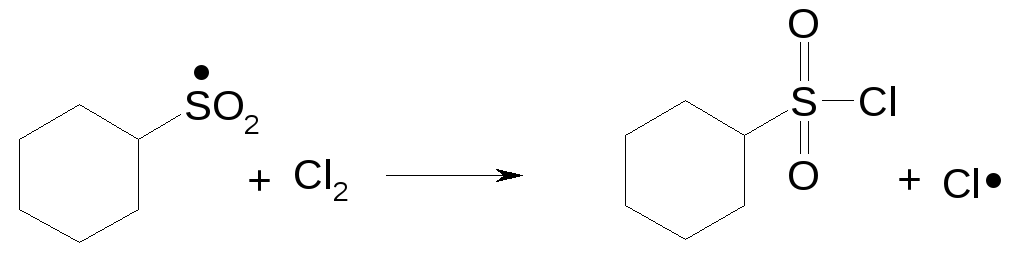
Обрыв цепи рекомбинация радикалов
Алкены (этилены)
Строение алкенов
![]() ,
R и R’
алкильные заместители.
,
R и R’
алкильные заместители.
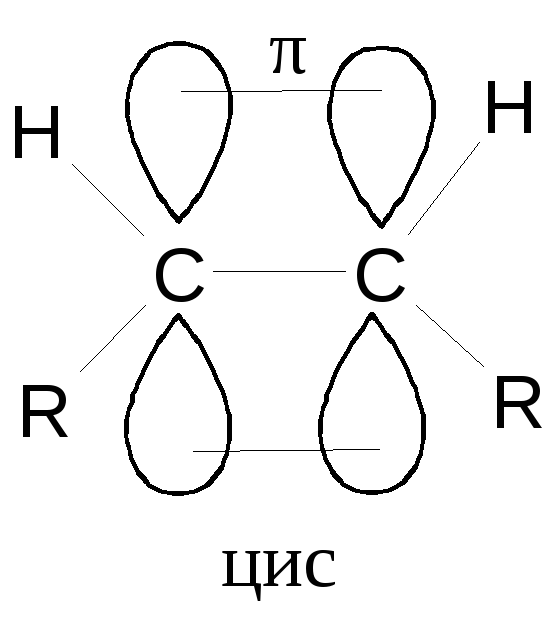
Атомы углерода при двойной связи находятся в состоянии sp2-гибридизации.
Двойная связь короче одинарной и составляет 0,134 нм. Вращение вокруг двойной связи невозможно, поэтому существуют цис- и транс- изомеры. Переход цис в транс и обратно возможен только при условии разрыва кратной связи (конфигурационные изомеры).
Получение алкенов
В природе алкены в небольших количествах встречаются в нефти, природных газах и каменноугольных смолах. Алкены играют значительную роль в живой природе. Например, они являются составной частью ферамонов, непредельных жирных кислот.
Важнейшая реакция получения алкенов в промышленности это крекинг и дегидрирование.
Крекинг:
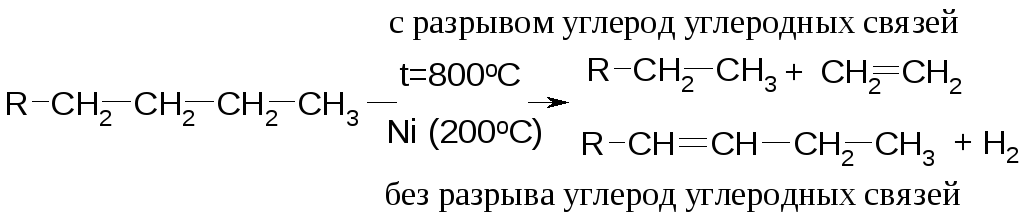
Большое промышленное значение имеет дегидратация спиртов, которая протекает по правилу Зайцева:
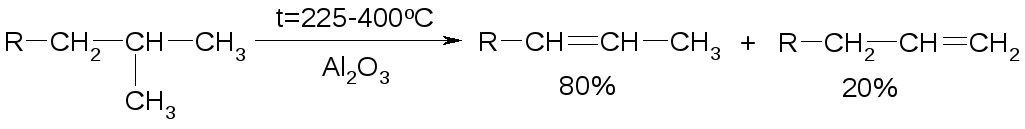
Лабораторные методы получения алкенов
Дегидрогалогенирование галогенпроизводных (по правилу Зайцева)
Отщепление от наиболее замещенного атома водорода.
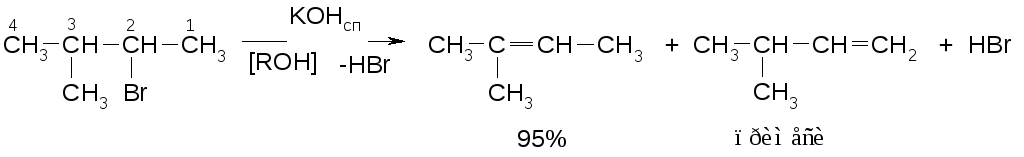
Правило Зайцева:отщеплениеН-галогенот алкилгалогенидов протекает таким образом, что водород уходит от наименее гидрированного атома углерода.
Исследованиями установлено, что реакции дегидрогалогенирования протекают стереоселективно, т.е. с образованием преимущественно одного из двух возможных продуктов.
Возможно протекание реакции по мономолекулярному и бимолекулярному механизмам отщепления.
Мономолекулярные реакции наблюдается в тех случаях, когда кинетика (скорость) процесса зависит от концентрации одного из взаимодействующих веществ, а бимолекулярные реакции когда кинетика процесса зависит от концентрации двух взаимодействующих веществ:
v1=K1[RHal]мономолекулярные
v2=K2[RHal] [ROK]бимолекулярные
Механизм Е2 реакции элиминирования (Е2 бимолекулярный механизм).
Реакция протекает лишь при транс- расположении отщепляющихся атомов (регеоселективность)
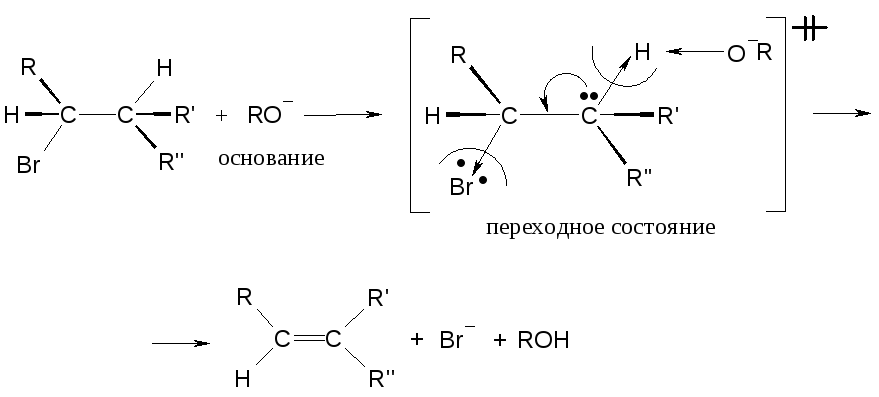
При невозможности транс расположения HиHalреакция может вообще не протекать, или протекать, но с очень низким выходом.
Рассмотрим на фиксированных структурах:
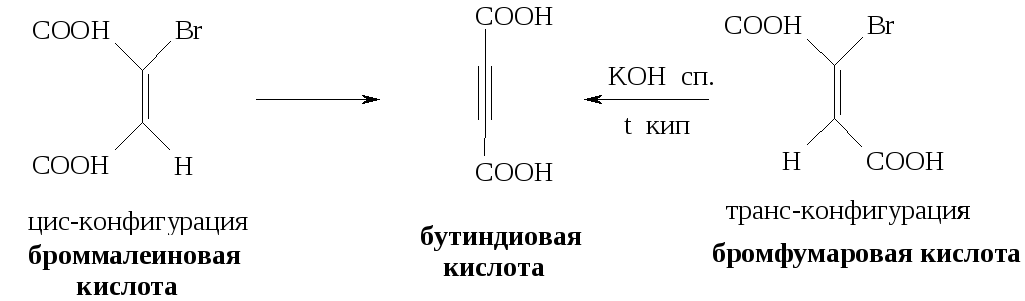
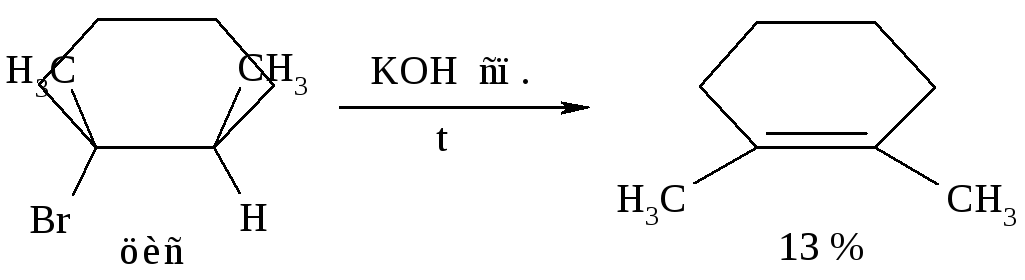
Механизм реакции E1 (мономолекулярной)
Реакция протекает в две стадии:
Лимитирующая стадия
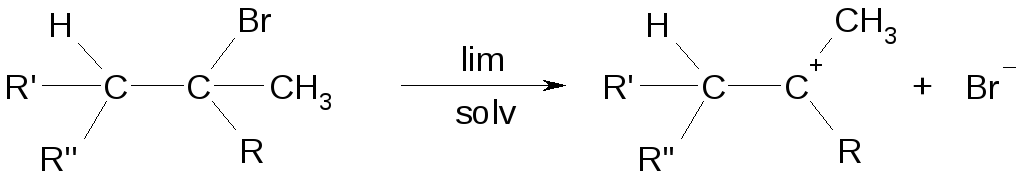
диссоциация по ионному механизму.
Быстрая, выброс протона от соседнего атома углерода
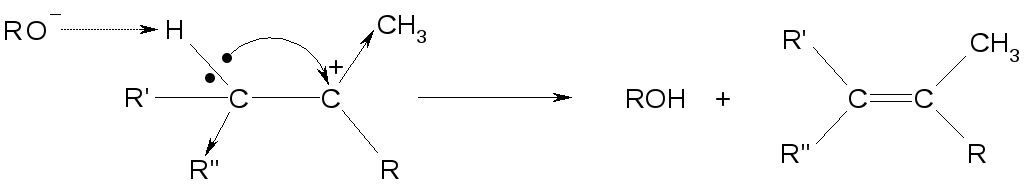
Для чего нужно транс-расположение HиHal?
Для того, чтобы основание RO¯не испытывало пространственных взаимодействий с богатым электронами атомом галогена.
Транс-расположение более важно при прохождении реакции по механизму E2.
