
- •Тема 4. Фазовые равновесия
- •4.1. Основные понятия и определения
- •4.2. Правило фаз Гиббса
- •4.3. Понятие о физико-химическом анализе. Термический анализ
- •4.4. Однокомпонентные гетерогенные системы. Уравнение Клапейрона – Клаузиуса
- •4.5. Фазовые диаграммы однокомпонентных гетерогенных систем
- •4.5.1. Фазовая диаграмма воды
- •4.5.2. Полиморфизм
- •4.5.3. Фазовая диаграмма серы
4.4. Однокомпонентные гетерогенные системы. Уравнение Клапейрона – Клаузиуса
Однокомпонентная гетерогенная система состоит из индивидуального вещества, которое может существовать в различных агрегатных состояниях или полиморфных модификациях.
Рассмотрим равновесный процесс перехода вещества из фазы 1 в фазу 2. В условиях равновесия молярная энергия Гиббса вещества в первой и второй фазах равны:
G1=G2(4.5)
Изменение температуры и давления вызовет изменение энергии Гиббса в каждой фазе [см. (2.53)]:
dG1=S1dT+V1dP(4.6)
dG2=S2dT+V2dP, (4.7)
где V1,V2– молярные объёмы, аS1, S2– молярные энтропии веществав соответствующих фазах. При равновесии между фазами dG1 = dG2.
Следовательно,
(S2–S1)dT= (V2 -V1)dP, (4.8)
откуда
![]() . (4.9)
. (4.9)
Изменение энтропии при температуре фазового перехода
![]() , (4.10)
, (4.10)
где ΔНФ.П.молярная теплота фазового перехода.
При подстановке (4.10) в уравнение (4.9) получим уравнение
Клапейрона - Клаузиуса:
![]() (4.11)
(4.11)
Уравнение Клапейрона – Клаузиуса характеризует зависимость температуры фазового перехода от внешнего давления в однокомпонентной системе. В данной форме уравнение применимо к любому двухфазному равновесному переходу.
Для процесса плавления dТ/dР – изменение температуры плавления при изменении давления на единицу. Поскольку плавление всегда сопровождается поглощением тепла, то знак производной dТ/dР зависит от знака ΔV= Vж – Vтв, то есть изменения объёма при плавлении (следует помнить, что при определении изменения объёма всегда вычитают из конечного значения параметра – начальное). Чаще всего, Vж > Vтв, поэтому с увеличением давления температура плавления вещества повышается. Реже наблюдается обратная закономерность: ΔV < 0, и с ростом давления температура плавления понижается. Таких веществ не много. Это, например, вода ( при давлениях ниже 2200 атм), висмут, галлий, чугун и некоторые другие.
Для процесса испарения жидкости уравнению Клапейрона - Клаузиуса можно придать другой вид. Часто можно пренебречь объемом жидкой фазы по сравнению с объемом пара и считать V=Vп. Например, при 273,15 К для водыVп= 22400 см3, аVж= 18 см3. Если насыщенный пар подчиняется уравнению состояния идеальных газов, то Vп= RT/P (для 1 моля идеального газа) и из (4.11) получим
![]()
или
![]() (4.12)
(4.12)
Уравнение (4.12) тоже называется уравнением Клапейрона-Клаузиуса.
Здесь следует снова обратить внимание на то, что под знаком логарифма оказывается величина, имеющая размерность. Не приводя здесь преобразований этой величины в безразмерную, отметим только, что для соблюдения правил применения математического аппарата к вычислениям физических параметров, будем считать, что под знаком логарифма и в этом случае, как и в предыдущем разделе курса, например см. (2.77) и далее мы подставим относительное давление, то есть давление, отнесённое к Р0 – стандартному давлению. Если давление выражено в атмосферах, то Р0 = 1 атм.
Для равновесия «кристаллы ↔ пар», зависимость давления насыщенного пара вещества, равновесного с кристаллами, от температуры выражается аналогичным уравнением. Тогда вместо Нисп. следует записать Нвозг. –молярная теплота возгонки, Т – температура возгонки (или сублимации).
Проинтегрируем уравнение (4.12) в пределах от состояния 1 до состояния 2, считая Нисп. величиной постоянной (не зависящей от температуры):
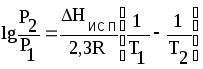 (4.13)
(4.13)
Или неопределенный интеграл:
![]() (4.14)
(4.14)
Физический смысл постоянной интегрирования
В:
![]() ,
гдеSисп.изменение энтропии
при образовании 1 моля пара.
,
гдеSисп.изменение энтропии
при образовании 1 моля пара.
Зависимость
![]() линейна, угловой коэффициент ее составляетНисп./2,3R.
Для фазовых превращений конденсированных
фаз (например, вода ↔ лед) или полиморфных
превращений (например,Sромб
↔Sмонокл.)
температурный коэффициент dP/dT характеризует
возникающее давление при изменении
температуры на 1 градус.
линейна, угловой коэффициент ее составляетНисп./2,3R.
Для фазовых превращений конденсированных
фаз (например, вода ↔ лед) или полиморфных
превращений (например,Sромб
↔Sмонокл.)
температурный коэффициент dP/dT характеризует
возникающее давление при изменении
температуры на 1 градус.
Уравнения Клапейрона-Клаузиуса широко используются при расчете фазовых равновесий.
Пример. На вершине горы атмосферное давление Р = 634 мм рт. ст. При какой температуре закипит вода в этих условиях? Известно, что теплота испарения водыНисп.= 40587 Дж/моль, и при Р1= 760 мм рт. ст. температура кипения воды Т1=373 К. Подставив эти данные в уравнение (4.13), рассчитаем Т2. При заданных условиях вода закипит при Т=368 К, или при 95С.
