
- •Классификация и роль углеводов в организме.
- •Моносахариды могут связываться друг с другом.
- •Углеводы – это не только источники энергии.
- •Переваривание углеводов начинается в ротовой полости.
- •В клетки разных органов глюкоза проникает различными механизмами.
- •Фруктоза и галактоза превращаются в глюкозу.
- •Обмен галактозы.
- •Глюкоза запасается в клетках в форме гликогена.
- •Гликогенолиз – процесс распада углеводов.
- •Гликогенфосфорилаза
- •Неактивная Активная
- •Восстановительный путь обмена глюкозы.
- •Дихотомический путь окисления глюкозы – основной путь получения энергии в клетке.
- •Анаэробное дыхание – гликолиз.
- •Триозофосфат-
- •В анаэробных условиях конечным акцептором водорода может быть ацетальдегид.
- •В аэробных условиях пвк окончательно окисляется Цепь реакций аэробного распада глюкозы можно расчленить на 3 основных этапа:
- •Окислительное декарбоксилирование пирувата
- •Регуляция активности пируватдегидрогеназы.
- •Цикл Кребса – центральный путь обмена веществ.
- •3 Реакция – дегидрирование и прямое декарбоксилирование изолимонной кислоты.
- •4 Реакция – окислительное декарбоксилирование α-кетоглутаровой кислоты.
- •5 Реакция – субстратное фосфорилирование.
- •6 Реакция – дегидрирование янтарной кислоты сукцинатдегидрогеназой.
- •7 Реакция – образование яблочной кислоты ферментом фумаразой.
- •8 Реакция – образование оксалацетата.
- •Функции цикла трикарбоновых кислот многообразны
- •Скорость реакция цикла Кребса определяется энергетическими потребностями клетки.
- •1. Пентозофосфатный путь окисления глюкозы обслуживает восстановительные синтезы в клетке.
- •2 Глутатион-sh МетНb витамин с
- •2.Глюконеогенез – механизм синтеза глюкозы.
- •Гликолиз и глюконеогенез – взаимосвязанные процессы.
- •Глюкуроновый путь обмена глюкозы
- •Фруктоза и галактоза превращаются в глюкозу.
- •Обмен галактозы.
- •Гликогеновые болезни.
- •Регуляция углеводного обмена.
- •1. Регуляция углеводного обмена.
- •2.Сахарный диабет тип I.
- •3.Гиперинсулинизм
- •4. Фруктоза и галактоза превращаются в глюкозу
- •Обмен галактозы.
- •Гликогеновые болезни.
Скорость реакция цикла Кребса определяется энергетическими потребностями клетки.
Скорость реакций цикла Кребса коррелирует с интенсивностью процесса тканевого дыхания и связанного с ним окислительного фосфорилирования. В свою очередь, функцио(дыхательного контроля): чем меньше это соотношение, тем интенсивнее идёт тканевое дыхание и эффективнее генерируется электро-химический потенциал, т. е. увеличивается выработка АТФ. Ускорение тканевого дыхания приводит к более быстрому потреблению субстратов цикла Кребса, которые одновременно являются также субстратами тканевого дыхания.
Непосредственно регулируется активность дегидрогеназ цикла Кребса, которая зависит от величины отношения НАДН∙Н+/ НАД+: при недостатке НАД+ их активность снижается, поскольку именно окисленная форма кофермента является акцептором водородов для субстратов лимоннокислого цикла. Помимо этого, существует аллостерический механизм регуляции: для изоцитрадегидрогеназы аллостерическими ингибиторами являются АТФ и НАДН∙Н+, активатором – АДФ. Сукцинатдегидрогеназа угнетается избытком субстрата.
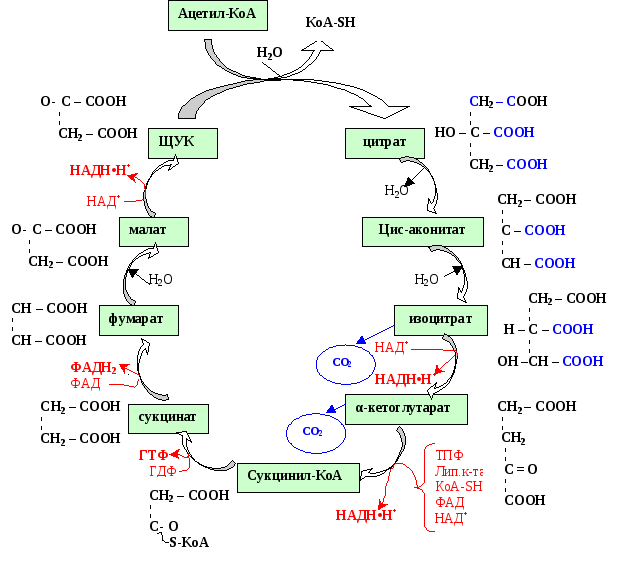
Рис.. Цикл трикарбоновых кислот (цикл Кребса)
Заключение
Должность и ф.и.о. автора лекции Дата
ЛЕКЦИЯ
По биологической химии
для студентов_____2-го_____ курса ___лечебного___________________факультета
Тема:___Углеводы 3. Тканевой обмен __углеводов_. Регуляция уровня глюкозы в крови__________
Время__90 мин___________________
Учебная цель:
Сформировать представления о путях метаболизма глюкозы, молекулярных и физиологических механизмах регуляции уровня глюкозы в крови.
ЛИТЕРАТУРА
1.Биохимия человека:, Р.Марри, Д.Греннер, П.Мейес, В.Родуэлл.- М.книга ,2004.- т.1.т.2
,с..
2.Основы биохимии:А.Уайт, Ф.Хендлер,Э.Смит, Р.Хилл, И.Леман.-М. книга,
1981,т. 2, 541-608,.с.641-646
3.Наглядная биохимия: Кольман., Рем К.-Г-М. книга 2004г.
4.. Биохимические основы ...под. ред. член- корр. РАН Е.С. Северина
М.Медицина,2000.-с.156-158.
МАТЕРИАЛЬНОЕ ОБЕСПЕЧЕНИЕ
1.Мультимедийная презентация
РАСЧЕТ УЧЕБНОГО ВРЕМЕНИ
|
№п/п |
Перечень учебных вопросов |
Количество выделяемого времени в минутах |
|
1. |
Пути обмена глюкозо-6 фосфата. Пентозный цикл |
30 мин |
|
2. |
Глюконеогенез. |
30 мин |
|
3. |
Биосинтез ГАГ. Регуляция уровня глюкозы в крови |
30 мин
|
Всего 90 минут
1. Пентозофосфатный путь окисления глюкозы обслуживает восстановительные синтезы в клетке.
Как видно из названия, в этом пути образуются столь необходимые клетке пентозофосфаты. Поскольку образование пентоз сопровождается окислением и отщеплением первого углеродного атома глюкозы, то этот путь называется также апотомическим(apex– вершина).
Пентозофосфатный путь можно разделить 2 части: окислительную и неокислительную. В окислительной части, включающей 3 реакции, образуются НАДФН∙Н+ирибулозо-5-фосфат. В неокислительной части рибулозо-5-фосфат превращается в различные моносахаридыс 3, 4, 5, 6, 7 и 8-ью атомами углерода; конечными продуктами являются фруктозо-6-фосфат и 3-ФГА.
Окислительная часть.
Первая реакция– дегидрирование глюкозо-6-фосфатаглюкозо-6-фосфатдегидрогеназой с образованием δ-лактона 6-фосфоглюконовой кислоты иНАДФН∙Н+ (НАДФ+ – кофермент глюкозо-6-фосфатдегидрогеназы).

Вторая реакция – гидролиз 6-фосфоглюконолактонаглюконолактонгидролазой. Продукт реакции – 6-фосфоглюконат.
глюконолактонгидролаза

 6-фосфоглюконолактон
6-фосфоглюконат
6-фосфоглюконолактон
6-фосфоглюконат
Н2О
Третья реакция– дегидрирование и декарбоксилирование 6-фосфоглюко-нолактона ферментом6-фосфоглюконатдегидрогеназой, коферментом которого являетсяНАДФ+ . В ходе реакции восстанавливается кофермент и отщепляется 1С глюкозы с образованием рибулозо-5-фосфата.
СООН
│
 Н–С–ОН
СН2ОН
Н–С–ОН
СН2ОН
│ СО2 │
Н–С–ОНС=О
│ │
Н–С–ОН 6-фосфоглюконатдегидрогеназаН–С–ОН
│ (декарбоксилирующая) │
Н–С–ОН Н–С–ОН
│ │
СН2ОРО3Н2СН2ОРО3Н2
6-фосфоглюконат Рибулозо-5-фосфат
Неокислительная часть.
В отличие от первой, окислительной, все реакции этой части пентозофосфатного пути обратимы.
Рибулозо-5-фосфат может изомеризоваться (фермент – кетоизомераза) в рибозу-5-фосфат и эпимеризоваться (фермент –епимераза) в ксилулозо-5-фосфат. Далее следуют 2 типа реакций: транскетолазная и трансальдолазная.
Транскетолаза(кофермент – тиаминпирофосфат) отщепляет 2С-фрагмент и переносит его на другие сахара (см. схему).Трансальдолазаспособна переносить 3С-фрагменты.
В реакцию вначале вступают рибозо-5-фосфат и ксилулозо-5-фосфат. Это – транскетолазная реакция: переносится 2С-фрагмент от ксилулозо-5-фос-фата на рибозо-5-фосфат.
 Рибозо-5-фосфат
Ксилулозо-5-фосфат
Рибозо-5-фосфат
Ксилулозо-5-фосфат
Транскетолаза (ТПФ)
Седогептулозо-7-фосфат 3-ФГА
Затем два образовавшиеся соединения реагируют друг с другом в трансальдолазной реакции; при этом в результате переноса 3С-фрагмента от седогептулозо-7-фосфата на 3-ФГА (3-фосфоглицериновый альдегид) образуются эритрозо-4-фосфат и фруктозо-6-фосфат.
С едогептулозо-7-фосфат
3-ФГА
едогептулозо-7-фосфат
3-ФГА
Трансальдолаза
Эритрозо-4-фосфат Фруктозо-6-фосфат
Однако реакция может идти и по другому пути (рис.6.17). В этом случае в трансальдолазной реакции образуется октулозо-1,8-дифосфат.

Рис.. Пентозофосфатный (апотомический) путь обмена глюкозы
Эритрозо-4-фосфат и фруктозо-6-фосфат могут вступать в транскетолазную реакцию, в результате которой образуются фруктозо-6-фосфат и 3-ФГА:
Э ритрозо-4-фосфат
Фруктозо-6-фосфат
ритрозо-4-фосфат
Фруктозо-6-фосфат
Транскетолаза (ТПФ)
Фруктозо-6-фосфат 3-ФГА
Общее уравнение окислительной и неокислительной частей пентозофосфатного пути можно представить в следующем виде:
6 Глюкозо-6-ф-т + 7Н2О + 12 НАДФ+
5 Глюкозо-5-ф-т + 6СО2 +
12 НАДФН∙Н+ + Рн
Глюкозо-6-ф-т + 7Н2О + 12 НАДФ+
5 Глюкозо-5-ф-т + 6СО2 +
12 НАДФН∙Н+ + Рн
Значение пентозофосфатного пути окисления глюкозы
Ферменты пентозофосфатного пути локализуются в цитоплазме. В тканях, синтезирующих стероиды или жирные кислоты (для чего необходим НАДФН∙Н+), окислительная часть пути протекает весьма интенсивно. К таким тканям относятся: надпочечники, печень, жировая ткань, лактирующая молочная железа. Эритроциты нуждаются в коферменте НАДФН∙Н+для восстановления глутатиона (трипептид). Совместно с витамином С восстановленный глутатион играет основную роль в предупреждении образования метгемоглобина: глутатион-SHявляется активной частью глутатионпероксидазы, устраняющей токсическое влияние пероксида водорода и других перекисей, окисляющих железо гемоглобина и нарушающих его кислородтранспортную функцию.

глутатион –S-S-глутатион
НАДФН∙ Н+ Н2О
Глутатионредуктаза Глутатионпероксидаза
НАДФ+ Н2О2
