
- •Лекция 13
- •План
- •13.1. Введение. Биологическая роль
- •Биологическая роль углеводов
- •13.2 Классификация, стереоизомерия углеводов
- •Классификация углеводов В зависимости от
- •Классификация углеводов ПО ЧИСЛУ АТОМОВ УГЛЕРОДА
- •Простейшие представители моносахаридов
- •Стереоизомерия моносахаридов
- •Многообразие форм молекул моносахаридов предполагает различные способы их изображения
- •Британский химик W.N.Haworth (лауреат Нобелевской премии в 1937)
- •Пяти- и шестичленные цепи имеют клешневидную конфигурацию и вследствие этого возможно сближение в
- •В циклической форме возникает дополнительный центр хиральности, т.е. асимметрическим становится карбонильный атом углерода.
- •У α-аномера конфигурация аномерного центра совпадает с конфигурацией концевого, наиболее удаленного асимметрического атома
- •Относительная конфигурация моносахаридов, т.е. принадлежность к D-и L-стереохимическим рядам определяется путем сравнения конфигурации
- •ОТНОСИТЕЛЬНАЯ КОНФИГУРАЦИЯ ГЛЮКОЗЫ
- •Эпимеры – диастереомеры, различающиеся конфигурацией только одного хирального атома
- •Эпимеры глюкозы
- •Эпимеры глюкозы
- •13.3. Пентозы. Гексозы
- •Рибоза входит в состав нуклеиновых кислот, а в виде восстановленного спирта входит в
- •Дезоксирибоза входит в состав нуклеиновых кислот
- •Арабиноза широко распространена в гемицеллюлозах и пектиновых веществах. Ксилоза – древесный сахар. Восстановленный
- •Гексозы
- •Глюкоза (виноградный сахар) содержится во всех фруктах, ягодах, меде
- •Фруктоза – плодовый сахар, встречается обычно вместе с глюкозой. В свободном виде находится
- •Гексозы
- •Гексозы
- •Гексозы
- •Манноза образует сложные природные углеводы – маннаны, входит в состав гликопротеидов. Встречается в
- •13.4. Цикло-оксо таутомерия
- •HOCH2
- •Процесс растворения моносахаридов в воде сопровождается своеобразным оптическим эффектом, который получил название мутаротация
- •Явление мутаротации связано с таутомерными превращениями глюкозы
- •Для пиранозной формы наиболее предпочтительна конформация кресла. Конформационное строение D-глюкопиранозы проливает свет на
- •Конформации глюкозы
- •Благодаря строению (экваториальное расположение всех заместителей) β- глюкоза термодинамически устойчива, именно это и
- •13.5. Химические свойства моносахаридов
- •Для моносахаридов характерны как реакции, свойственные спиртам, так и альдегидам
- •1.Образование простых эфиров
- •2.Образование сложных эфиров
- •Из сложноэфирных производных наибольшее значение имеют эфиры фосфорной кислоты (фосфаты), они содержатся во
- •Фосфаты глюкозы
- •II.Реакции, обусловленные альдегидной группой
- •При восстановлении ксилозы образуется ксилит, галактозы
- •2. Реакции окисления а) Реакции окисления в щелочной
- •б) Реакции окисления в щелочной среде реактивом Фелинга (реактивом Бенедикта)
- •Углеводы, дающие положительные реакции окисления в щелочной среде, называются восстанавливающими
- •В) ОКИСЛЕНИЕ В КИСЛОЙ И НЕЙТРАЛЬНОЙ СРЕДЕ
- •Мягкие окислители окисляют только альдегидную группу, не затрагивая первичную спиртовую
- •ПОЛУЧЕНИЕ О-ГЛИКОЗИДОВ
- •О-гликозиды легко гидролизуются в кислой
- •Аминопроизводные углеводов, аминосахара, входят в состав мукополисахаридов в организме человека и животных. Важнейшие
- •Производные углеводов (аминосахара)
- •Производные углеводов (аминосахара)
- •COOH
- •Взаимные превращения альдоз и кетоз в щелочной среде
- •Благодарим за внимание !
Гексозы
Галактоза в свободном виде не встречается, входит в состав дисахаридов
H |
|
|
O |
|
|
|
H |
|
|
|
|
|
OH |
||||
H |
C |
|
|
|
H |
C |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
OH |
|
|
|
|
|
|
|
OH |
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||||||
HO |
|
|
H |
|
|
|
HO |
|
|
|
|
H O |
|||||
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|||||||||||||
HO |
|
|
H |
|
|
|
HO |
|
|
|
|
H |
|
|
|||
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|||||||||
H |
|
|
OH |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
CH2OH |
|
|
|
|
|
|
CH2OH |
||||||||
|
|
|
|
|
|
|
|||||||||||
D-галактоза
Фишера Колли-Толленса
CH2OH
HO O
OH
OH
OH
D -ГАЛАКТОПИРАНОЗА
HO |
|
|
CH2OH |
OH |
|||
|
|||||||
|
|
|
O |
||||
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|||
|
|
|
|
||||
OH
D -ГАЛАКТОПИРАНОЗА
Хеуорса

Гексозы
H |
|
|
O |
|
|
|
H |
|
|
|
|
OH |
||||
HO |
C |
|
|
|
|
C |
|
|
|
|
||||||
|
|
|
|
|
||||||||||||
|
|
H |
|
|
|
HO |
|
|
|
H |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|||||||||
HO |
|
|
H |
|
|
|
HO |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
H O |
||||||||
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
||||||||||||
H |
|
|
OH |
|
|
|
H |
|
|
|
OH |
|
|
|||
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|||||||||
H |
|
|
OH |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
||||||||
|
CH OH |
|
|
|
|
|||||||||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
D-манноза
CH2OH
O
OH OH
OH  OH
OH
D -МАННОПИРАНОЗА
CH2OH
O OH
OH OH
OH
D -МАННОПИРАНОЗА

Манноза образует сложные природные углеводы – маннаны, входит в состав гликопротеидов. Встречается в растениях, в составе слизей, гемицеллюлоз, содержится в ячмене, корках апельсина

13.4. Цикло-оксо таутомерия
В кристаллическом состоянии все моносахариды находятся в циклической форме в виде α- или β-аномеров. При растворении моносахаридов в воде наблюдается так
называемая цикло-оксо таутомерия (кольчато-цепная таутомерия), т.е.
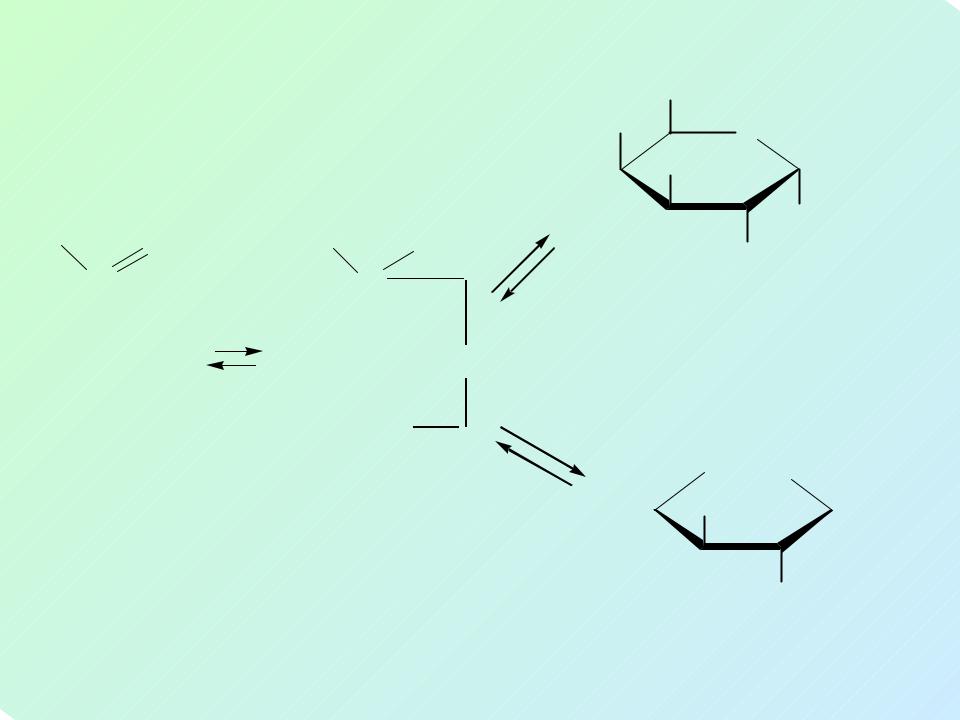
устанавливается равновесие между циклическими таутомерами моносахаридов, различающихся по размеру цикла (фуранозный, пиранозный), α- и β-формами и открытой формой
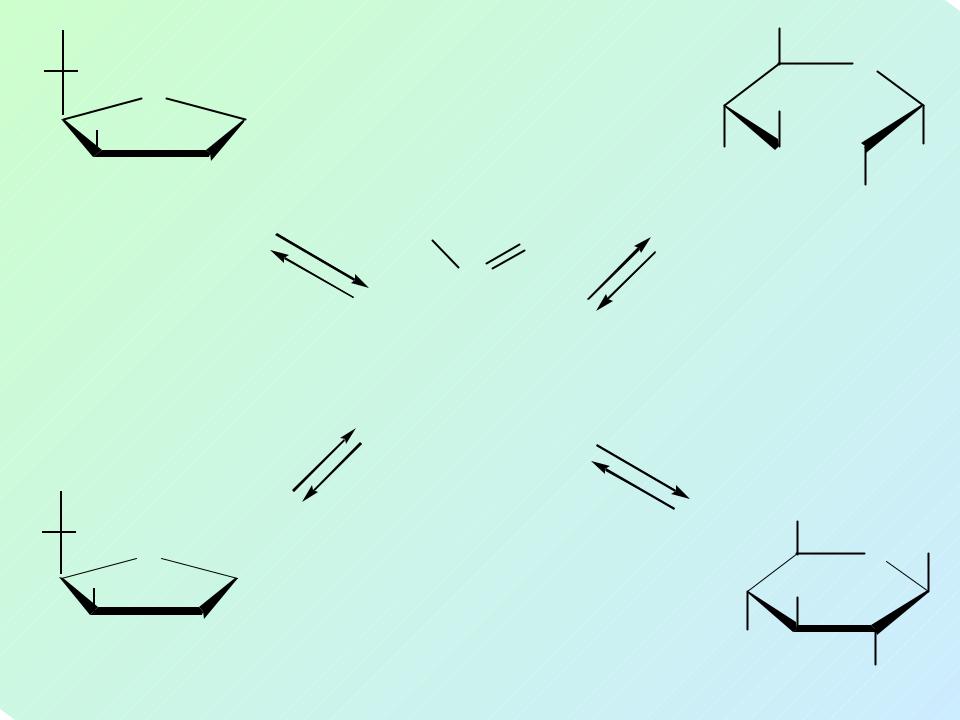
HOCH2
HO |
|
|
|
H |
O |
Таутомерные формы |
||||||||||||||||||
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
глюкозы |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
||||
D -ГЛЮКОФУРАНОЗА |
|
H |
|
|
|
O |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
HOCH2 |
|
|
|
|
|
|
|
|
|
H |
|
|
|
OH |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
HO |
|
|
H |
O |
|
OH |
|
0,02% |
|
|||||||||||||||
|
|
|
|
|
||||||||||||||||||||
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
64% |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|||||||
CH2OH
O
OH
OH  OH OH
OH OH
D -ГЛЮКОПИРАНОЗА
36%
CH2OH
O OH
OH
OH
OH
D -ГЛЮКОФУРАНОЗА |
D -ГЛЮКОПИРАНОЗА |

Процесс растворения моносахаридов в воде сопровождается своеобразным оптическим эффектом, который получил название мутаротация – изменение удельного вращения до некоторой определенной величины при растворении моносахарида в воде

Явление мутаротации связано с таутомерными превращениями глюкозы
В смеси таутомеров глюкозы преобладают пиранозные формы, однако, хотя откры- тая форма и составляет только ≈ 0,02 % в смеси, тем не менее для глюкозы характерны все реакции на альдегидную группу, т.к. по мере расходования одной формы, она вновь образуется, потому что таутомеры легко переходят один в другой

Для пиранозной формы наиболее предпочтительна конформация кресла. Конформационное строение D-глюкопиранозы проливает свет на уникальность β- D-глюкопиранозы: единственный моносахарид с полным экваториальным расположением заместителей
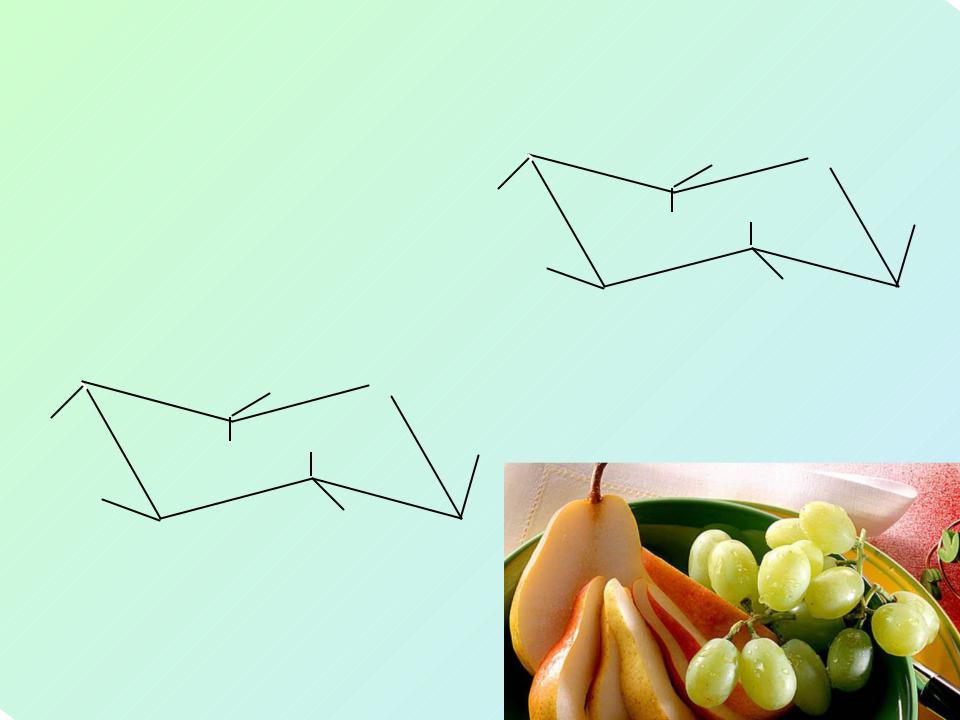
Конформации глюкозы
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH O |
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
H |
|
H |
||||
|
|
|
|
|
|
|
|
|
HO |
|
H |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
||
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
CH2OH O |
|
|
|
H |
|
|
OH |
||||
HO |
|
|
|
|
|
|
|
|
D-ГЛЮКОПИРАНОЗА |
||||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
H |
|
OH |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
HO |
|
H |
|
|
|
|
|
|
|
|
||||||
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|||||
|
|
|
H |
|
|
|
|
|
|
|
|
|
|||||
|
D-ГЛЮКОПИРАНОЗА |
|
|
|
|
|
|
|
|
|
|
||||||

Благодаря строению (экваториальное расположение всех заместителей) β- глюкоза термодинамически устойчива, именно это и является причиной распространенности β-глюкозы в природе
