- •Міністерство освіти і науки україни
- •Термохімія.
- •Напрям перебігу хімічних процесів.
- •Експериментальна частина.
- •Лабораторна робота "Визначення теплового ефекту реакції нейтралізації" Хід роботи
- •Розрахунки
- •Лабораторна робота «Визначення молярної теплоти розчинення солі» Хід роботи
- •Обробка експериментальних даних
- •Питання для самоконтролю
- •Задачі і вправи для самостійної роботи
- •Рекомендована література
Експериментальна частина.
Лабораторна робота "Визначення теплового ефекту реакції нейтралізації" Хід роботи
|
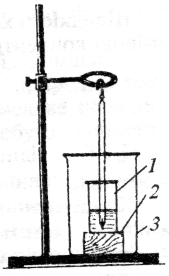
Роботу виконують у спрощеному калориметрі (рис. 1), який складається із зовнішнього стакана З місткістю 500 мл і внутрішнього 1 місткістю 250 мл. Внутрішній стакан ставлять на корок 2 для зменшення теплообміну із навколишнім середовищем, а зовнішній закривають азбестовою кришкою, крізь отвір якої пропускають у внутрішній стакан термометр на 50 °С з ціною поділки 0,1 °С. |
Рис.1. Спрощений калориметр |
У внутрішній хімічний стакан 1, маса якого відома, відміряють мірним циліндром 50 мл вказаної викладачем кислоти, концентрація якої відома. Термометром вимірюють температуру розчину і записують в табл.1. Відміряють мірним циліндром 50 мл розчину лугу NaOH, виливають в стакан з кислотою, перемішують і виміряють зміну температури. Результати заносять в табл.1. Аналогічно виконують дослід з іншою кислотою. Виконують розрахунки і записують рівняння відповідних реакцій.
Розрахунки
Кількість теплоти, яка виділилась при нейтралізації кислоти в першому та другому дослідах, розрахувати за формулою:
![]() ,
,
де: mст – маса стакана ;
сск – питома теплоємність скла (0,795 Дж/гград) ;
своди – питома теплоємність води (4,2 Дж/гград) ;
mрозчин – маса розчину, г ;
mрозчин
= (mкислоти+
mлугу);
![]() ;
;
- густини розчинів кислоти та лугу відповідно (за довідником);
V – об'єми розчинів кислоти та лугу відповідно, мл.
Тепловий ефект реакції нейтралізації розраховують на 1 моль води, яка утворилась внаслідок реакції, за формулою:
![]()
У відповідності зрівнянням реакції кількість води, яка утворилась (H2O), дорівнює кількості кислоти(кислоти)або кількості лугу(лугу), тобто
![]() ,
,
де: С(кислоти) – молярна концентрація кислоти, моль/л;
V(кислоти) – об'єм розчину кислоти, л.
Таблиця 1
|
Показники |
Дослід 1 –нейтралізація сильної кислоти лугом |
Дослід 2 –нейтралізація слабкої кислоти лугом |
|
Рівняння реакції
|
|
|
|
Температура: |
|
|
|
-до
початку реакції,
|
|
|
|
-після
реакції,
|
|
|
|
-зміна
температури,
|
|
|
|
Тепловий ефект: |
|
|
|
Hх.р.практ. |
|
|
|
Hх.р.теорет. |
|
|
|
Похибка досліду, % |
|
|
Теоретичне значення теплового ефекту для першого та другого дослідів розраховують, використовуючи наслідок із закону Гесса:
![]()
Значення теплот утворення речовин наведені в табл.2 (або в довіднику).
Таблиця 2
Стандартні теплоти утворення деяких речовин
|
Речовина |
|
|
Катіон водню, Н+ |
0 |
|
Гідроксид-іон, ОН- |
-230,02 |
|
Вода, Н2О |
-285,83 |
|
Ацетат-іон, СН3СОО- |
-483,64 |
|
Оцтова кислота, СН3СООН |
-484,09 |
Порівнюють теоретичні значення теплових ефектів нейтралізації з практично одержаними результатами та розраховують похибку досліду в першому та другому дослідах за формулою:
![]() %
%
За результатами експерименту та розрахунків роблять висновки.