
06.Карб.кисл
.pdf
Если вместо глицерина использовать многоатомный спирт пентаэритрит
CH2OH HOH2C C CH2OH
,то получится не глифталевая, а пентафталевая смола. Специальные добавки превратят ее в пентафталевую эмаль.
Взаимодействие с аммиаком. При нагревании фталевого ангидрида с аммиаком образуется имид фталевой кислоты (фталимид), широко применяемый в органическом синтезе. Реакция протекает через стадии образования моно- и нестойкого диамида фталевой кислоты:
O |
|
C |
O |
|
C |
NH |
OH |
NH3 |
|
|
|
|||
O |
3 |
|
|
|
|
|
NH2 |
- H2O |
|
C O |
|
C |
||
|
O |
|
||
фталевый ангидрид |
|
моноамид фталевой кислоты |
|
|
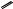 O
O
 C
C NH2
NH2
|
NH2 |
|
|
|
C |
|
- NH3 |
||
O |
|
|
|
|
диамид фталевой кислоты
O

 C
C 
. N H .
 C
C O
O
фталимид
Сравнение кислотно – основных свойств аммиака и его производых (аминов, амидов и имидов).
Аммиак, будучи сильным основанием, легко вступает в реакции с кислотами, образуя соли аммония:
.. |
[NH4]+Cl- |
NH3 + HCl |
Первичные, вторичные и третичные амины также являются
основаниями и под действием кислот превращаются в соли:
.. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|||||||
R |
|
|
|
NH2 |
+ HCl |
|
|
|
|
R |
|
|
|
NH3 |
|
|
|
Cl |
|||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
первичный амин |
|
|
хлорид алкиламмония |
||||||||||||||||||||||||||
R .. |
|
|
|
|
|
|
R |
|
|
|
|
|
+ |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
NH2 |
|
|
Cl |
|||||||||||||||||||
|
|
|
|
|
NH |
+ HCl |
|
|
|
|
R |
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
вторичный амин |
|
|
хлорид диалкиламмония |
||||||||||||||||||||||||||
R .. |
|
|
|
|
|
|
R |
|
|
+ |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
R |
|
N |
+ HCl |
|
|
|
|
|
R |
|
|
NH |
|
Cl |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
R |
|
|
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
третичный амин |
|
|
хлорид триалкиламмония |
||||||||||||||||||||||||||
183
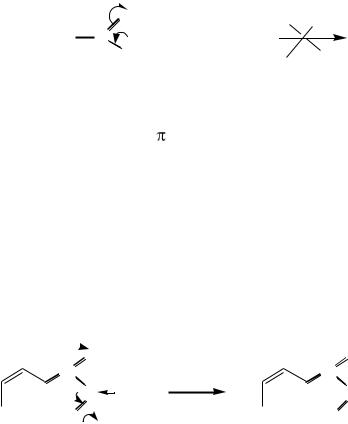
Амиды карбоновых кислот не проявляют основных свойств, с
кислотами не реагируют:
O
R C .. + HCl
.. + HCl
NH2
амид карбоновой кислоты
Причиной этого является тот факт, что свободная электронная пара азота в амиде вступает в сопряжение с -электронами карбонильной группы, что приводит к стягиванию электронов с азота и затруднению присоединения протона, т.е. азот в амидах теряет свои основные свойства.
Имиды (циклические вторичные амиды) не только лишены основных свойств, но даже приобретают кислотные свойства, поскольку две карбонильные группы мощно стягивают на себя электронную плотность и с атома азота, и с атома водорода, делая последний подвижным. В частности, фталимид, являясь слабой кислотой, реагирует с водными растворами щелочей, образуя N-металлические производные:
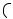 O C
O C


 :N H
:N H 
 C
C O
O
NaOH
- H2O
O
C

 N Na
N Na 
 C
C O
O
184
