
06.Карб.кисл
.pdf
CH3 |
|
|
|
|
|
|
C |
O |
+ |
PCl5 |
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
C |
O |
+ HCl |
+ POCl3 |
|||
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
3 CH3 |
|
|
|
|
|
C |
O |
+ |
PCl3 |
|
|
|
|
|
|
3 CH3 |
|
|
|
|
|
|
C |
O |
+ H3PO3 |
||||||
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
+ SO2 |
CH3 |
|
|
|
|
C |
OH + SOCl2 |
|
|
|
|
|
|
CH3 |
|
|
|
|
|
C |
Cl + |
HCl |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|||||||||||||||||||||||||||||||
CH3 |
|
|
|
C |
O |
+ SO2Cl2 |
|
|
|
|
|
|
CH3 |
|
|
|
|
C |
O |
+ |
HCl |
|
|
+ SO3 |
|||||||
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
этановая кислота |
ацетилхлорид |
|
(хлорангидрид этановой кислоты) |
||
|
Свойства галогенангидридов карбоновых кислот.
Галогенангидриды карбоновых кислот – очень реакционноспособные соединения.
Гидролиз галогенангидридов карбоновых кислот:
CH3 |
|
CH2 |
|
C |
O |
+ |
Н2О |
|
CH3 |
|
CH2 |
|
C |
O |
+ HCl |
|
|
Cl |
|
|
|
OH |
|||||||||
|
|
|
|||||||||||||
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пропионилхлорид |
пропановая кислота |
|
|
(хлорангидрид пропановой кислоты) |
|
Взаимодействие галогенангидридов карбоновых кислот со спиртами,
алкоголятами и фенолятами с образованием сложных эфиров:
СН3 |
|
|
C |
O |
+ |
С2Н5ОН |
|
|
|
|
|
|
СН3 |
|
|
|
C |
O |
+ |
HCl |
|||||
|
|
Cl |
|
|
|
|
|
|
|
|
|
OС2Н5 |
|||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
ацетилхлорид |
|
этанол |
|
|
|
|
|
этиловый эфир уксусной кислоты |
|
||||||||||||||||
|
|
|
|
|
|
|
O |
+ С2Н5О- Na+ |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
||
СН3 |
|
|
|
C |
Cl |
|
|
|
|
|
|
СН3 |
|
|
C OС2Н5 |
+ |
NaCl |
||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||
ацетилхлорид |
|
этилат натрия |
|
|
|
|
|
этиловый эфир уксусной кислоты |
|
||||||||||||||||
СН3 |
|
|
|
C |
O |
|
С6Н5О- Na+ |
|
|
|
|
|
|
СН3 |
|
|
C |
O |
+ |
|
|||||
|
|
|
Cl |
+ |
|
|
|
|
|
|
|
|
OС6Н5 |
NaCl |
|||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
ацетилхлорид |
|
фенолят натрия |
|
|
|
|
|
фениловый эфир уксусной кислоты |
|
||||||||||||||||
Взаимодействие галогенангидридов карбоновых кислот с аммиаком с |
|||||||||||||||||||||||||
образованием амидов: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
R |
|
C |
O |
+ NH4Cl |
||||||
|
|
R |
|
C |
Cl |
+ 2 NH3 |
|
|
|
|
|
|
|
NH2 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
амид кислоты
Галогенангидриды карбоновых кислот – ацилирущие агенты.
Ацилирование ароматических углеводородов по Фриделю – Крафтсу описано в разделе «Одноядерные арены».
Образование ангидридов кислот. При нагревании в присутствии водоотнимающих средств карбоновые кислоты подвергаются межмолекулярной дегидратации с образованием ангидридов:
153

|
|
O |
|
|
|
|
|
|
O |
|
|
|
Р2О5 |
СН3 |
|
|
|
C |
|
|
|
2 СН3 |
C |
ОН |
|
|
|
O |
+ 2НРО3 |
|||
|
СН3 |
|
|
C |
||||||
|
|
|
|
|
|
O |
|
|||
|
|
|
|
|
|
|
|
|
|
|
уксусная кислота |
|
уксусный ангидрид |
|
|||||||
Ангидриды кислот получаются также при взаимодействие галогенангидридов с солями карбоновых кислот:
|
|
|
|
|
|
|
O |
|
|
|
|
O |
R |
|
C |
O |
+ R |
|
C |
|
R |
|
C O + NaCl |
||
|
|
|
|
|||||||||
|
|
|
|
|
|
|||||||
|
Cl |
|
ONa |
|
R |
|
||||||
|
|
|
|
|
|
|
|
C |
|
|||
|
|
|
|
|
|
|
|
|
|
O |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
ангидрид кислоты
Свойства ангидридов карбоновых кислот.
Гидролиз ангидридов карбоновых кислот. При лѐгком нагревании с водой ангидриды образуют соответствующие карбоновые кислоты:
|
|
|
|
|
O |
|
|
|
|
|
O |
СН3 |
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
O |
+ |
Н2О |
|
2 СН3 |
C |
ОН |
||
|
|
|
C |
|
|||||||
СН3 |
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||
|
|
O |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
уксусный ангидрид |
|
|
|
уксусная кислота |
|||||||
Взаимодействие ангидридов карбоновых кислот со спиртами:
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
O |
СН3 |
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
O |
+ |
С2Н5ОН |
|
СН3 |
C |
ОС2Н5 |
+ |
СН3 |
|
C |
ОН |
||
|
|
|
|
|
||||||||||||
|
|
|
|
C |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
СН3 |
|
O |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
уксусный ангидрид |
|
|
|
этилацетат |
|
уксусная кислота |
||||||||||
Взаимодействие ангидридов карбоновых кислот с аммиаком. При этом образуется смесь кислоты и еѐ амида:
|
|
|
|
O |
|
|
|
|
O |
|
|
|
O |
СН3 |
|
|
C |
|
|
|
|
|
|
|
|
||
|
|
O |
+ NH3 |
|
СН3 |
C |
NН2 |
+ |
СН3 |
C |
ОН |
||
|
|
|
C |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||
СН3 |
O |
|
|
|
|
|
|
|
|||||
|
|
ацетамид |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
||||
уксусный ангидрид |
|
|
(амид уксусной кислоты) |
|
уксусная кислота |
||||||||
Ангидриды карбоновых кислот – ацилирущие агенты. Ацилирование с помощью ангидридов сопровождается выделением молекулы карбоновой кислоты.
Образование сложных эфиров (реакция этерификации). Карбоновые кислоты при нагревании в присутствии кислотного катализатора реагируют со спиртами, образуя сложные эфиры (см. раздел «Алканолы»):
|
|
|
O |
|
|
|
|
H2SO4 |
O |
|
|
|
||||
R |
|
C |
OH |
+ R' |
|
OH |
|
|
|
R |
|
C |
O |
|
R' |
+ H2O |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Скорость реакции этерификации зависит от строения кислот и спиртов. Линейные кислоты легче вступают в реакцию, чем разветвлѐнные.
154
Как указано выше, сложные эфиры могут быть также получены при
взаимодействии солей карбоновых кислот с галогеналканами, из галогенангидридов и ангидридов карбоновых кислот. Кроме того, к
образованию сложных эфиров приводит сложноэфирная конденсация альдегидов по Тищенко (см. раздел «Альдегиды и кетоны»):
O O
R C H + H
H + H C R
C R
(C2H5O)3Al
O
R C O CH2 R
Свойства сложных эфиров карбоновых кислот.
Гидролиз сложных эфиров. Сложные эфиры подвергаются гидролизу в кислой или щелочной средах. Кислотный гидролиз представляет собой последовательность обратимых превращений, противоположных реакции этерификации:
|
|
|
O |
|
|
|
|
H2SO4 |
O |
|
|
|
||||
R |
|
C |
O |
|
R' |
+ H2O |
|
|
|
R |
|
C |
OH |
+ R' |
|
OH |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
В отличие от кислотного щелочной гидролиз сложных эфиров – процесс необратимый. При щелочном гидролизе щѐлочь выступает не в роли катализатора, а в роли реагента:
O
R C O R' + NaOH
O R' + NaOH
H2O
O
R C O- Na+ + R' OH
O- Na+ + R' OH
Щелочной гидролиз сложных эфиров часто называют омылением. Это название связано с тем, что при щелочном гидролизе жиров, представляющих собой сложные эфиры глицерина и высокомолекулярных карбоновых кислот, образуются мыла.
Взаимодействие сложных эфиров со спиртами (реакция переэтерификации). Под действием спиртов в молекуле сложного эфира может происходить замена одного спиртового остатка на другой. Реакция обратима и катализируется кислотами или щелочами:
|
|
O |
|
|
|
|
|
O |
|
|||
|
|
|
H+или OН |
|
|
|
||||||
СН3 |
C |
OСН3 |
+ С2Н5ОН |
|
|
|
|
|
СН3 |
C |
ОС2Н5 |
+ СН3OH |
|
|
|||||||||||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
||
метилацетат |
этанол |
|
|
|
|
|
этилацетат |
метанол |
||||
Практическое значение переэтерификация имеет в том случае, когда в состав исходного сложного эфира входит остаток низкокипящего спирта. Отгоняя более летучий спирт, смещают равновесие реакции вправо.
Образование амидов карбоновых кислот. При взаимодействии карбоновых кислот с аммиаком образуются аммониевые соли кислот, которые при нагревании в сухом виде отщепляют воду и превращаются в амиды карбоновых кислот:
|
|
|
O |
|
|
R |
|
O |
|
|
200 оС |
R |
|
|
O |
|
R |
|
C |
OH |
+ NH3 |
|
|
C |
- |
+ |
|
|
|
C |
+ H2O |
||
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
O NH4 |
|
|
|
|
|
|
NH2 |
||
|
|
|
|
|
|
аммониевая соль |
|
|
|
|
амид |
|
||||
|
|
|
|
|
|
карбоновой кислоты |
|
|
|
карбоновой кислоты |
||||||
155

Из-за жѐстких условий протекания реакции этот метод образования амидов редко используется в препаративных целях. Чаще амиды получают при действии аммиака на сложные эфиры, галогенангидриды и ангидриды карбоновых кислот (см. выше).
Свойства амидов карбоновых кислот.
Гидролиз амидов карбоновых кислот. При кипячении с водными растворами минеральных кислот или щелочей амиды подвергаются гидролизу с образованием карбоновых кислот или их солей:
|
|
|
|
|
HCl |
|
R |
|
|
C |
O |
|
+ NH4Cl |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
O |
H2O |
|
|
|
|
OH |
||||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
||||
R |
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
NaOH |
|
R |
|
|
C |
O |
- + + NH4OH |
|||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
O |
||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
Na |
|
|
Амиды кислот образуются как промежуточные продукты при гидролизе нитрилов.
Дегидратация амидов карбоновых кислот. При нагревании с оксидом фосфора (V) амиды отщепляют воду с образованием нитрилов карбоновых кислот:
|
|
|
O |
Р2O5 |
|
|
|
|
|
|
|
R |
|
C |
|
R |
|
C |
|
|
N |
+ H2O |
|
|
NH2 |
|
|
|
|
||||||
|
t |
|
|
|
|||||||
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
||
амид карбоновой кислоты |
|
нитрил карбоновой кислоты |
|||||||||
Расщепление амидов карбоновых кислот по Гофману. При взаимодействии с гипобромитом натрия NaOBr амиды подвергаются расщеплению с образованием первичных аминов, содержащих на один атом углерода меньше, чем в исходном амиде:
|
|
|
|
O |
NaOBr |
|
|
|
|
CH3 |
|
CH2 |
C |
|
CH3 |
|
CH2 |
NH2 + NaBr + CO2 |
|
|
NH2 |
|
|
||||||
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
амид пропановой кислоты |
|
|
|
этиламин |
|||||
Восстановление амидов карбоновых кислот. При действии алюмогидрида лития LiAlH4 амиды восстанавливаются до аминов:
CH3 |
C |
O |
|
H |
|
CH3 |
CH2 |
NH2 + H2O |
|
|
|
||||||||
|
|
|
|||||||
NH2 |
|
|
|
||||||
LiAlH4 |
|||||||||
|
|
|
|
|
|||||
ацетамид |
|
|
|
|
этиламин |
||||
Замещение водорода у α-углеродного атома карбоновых кислот на галоген. Под действиием электроноакцепторной карбоксильной группы атомы водорода у α-углеродного атома приобретают подвижность, поэтому при обработке карбоновых кислот хлором или бромом в присутствии фосфора (или галогенидами фосфора) атомы водорода у α-углеродного атома замещаются на галоген. Реакция протекает через стадию образования галогенангидридов α- галогенкарбоновых кислот и известна как реакция Гелля – Фольгарда – Зелинского:
156
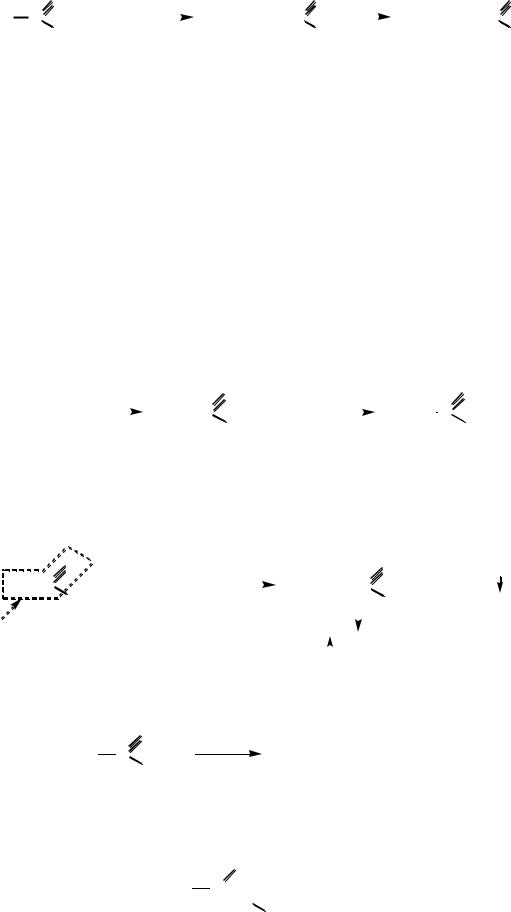
|
|
|
|
O |
|
|
P |
|
|
|
|
|
|
O |
|
CH3 |
|
CH2 |
C |
|
+ |
Br2 |
CH3 |
|
|
CH |
|
C |
|
||
|
OH |
|
|
|
|
|
Br |
||||||||
|
- Н2О |
|
|
||||||||||||
|
|
|
|
||||||||||||
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
Br |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
H2O |
|
|
|
|
|
|
O |
|
CH3 |
|
|
CH |
|
C |
|
||
|
|
|
|
|
OH |
|||
- HBr |
|
|
||||||
|
|
|
||||||
|
|
|
|
Br |
|
|
||
пропановая кислота |
бромангидрид |
2-бромпропановая |
|
2-бромпропановой кислоты |
кислота |
Окисление и восстановление карбоновых кислот. Монокарбоновые кислоты, за исключением муравьиной, довольно устойчивы к действию окислителей.
При восстановлении монокарбоновые кислоты образуют, в зависимости от условий, альдегиды или первичные спирты.
6.2.4. ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ НАСЫЩЕННЫХ МОНОКАРБОНОВЫХ КИСЛОТ
Му р а в ь и н а я к и с л о т а (метановая кислота) НСООН.
Впромышленности муравьиную кислоту получают из еѐ натриевой соли, которая образуется при пропускании оксида углерода (ІІ) через расплавленный едкий натр:
|
p, t |
|
|
|
O |
H2SO4 |
|
|
|
O |
|
|
|
|
|
H |
|
C |
|
||
CO + NaOH |
|
H C |
O- Na+ |
- NaHSO4 |
|
ОH |
||||
|
|
|
|
|||||||
|
|
формиат натрия |
|
муравьиная кислота |
||||||
В связи с особенностью строения (наличием альдегидной группы) муравьиная кислота даѐт реакцию «серебряного зеркала», окисляясь до угольной кислоты, которая разлагается на оксид углерода (IV) и воду:
|
|
|
O |
|
NH4OH |
|
|
|
O |
|
|||
H |
|
C |
|
+ Ag2O |
|
|
|
|
|
||||
|
ОH |
|
HO |
|
C |
ОH |
+ 2Ag |
||||||
|
|
|
|||||||||||
альдегидная |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||
группа |
|
|
|
CO2 |
|
|
+ |
H2O |
|
||||
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|||||
При нагревании с концентрированной серной кислотой муравьиная кислота разлагается с образованием оксида углерода (ІІ) и воды:
O |
H2SO4 |
|
|
|
H C ОH |
СО |
+ Н2О |
||
|
Среди производных муравьиной кислоты широкое практичекое применение в качестве сильно полярного растворителя имеет N,N- диметилформамид:
O
H C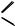 N
N CH3
CH3
CH3
157

Ук с у с н а я к и с л о т а (этановая кислота) СН3СООН.
Впромышленности существует несколько способов получения уксусной кислоты, рассмотренных ранее: из ацетилена через уксусный альдегид; при окислении алканов, этанола; уксуснокислым брожением и др. Разработан также метод получения уксусной кислоты оксосинтезом из метанола:
|
Ni (СО)4 |
|
|
O |
|
CH3OH + СО |
CH3 |
|
C ОH |
||
|
|
|
|||
р |
|
||||
============================================================
6.3. НАСЫЩЕННЫЕ ДИКАРБОНОВЫЕ КИСЛОТЫ
============================================================
Насыщенные дикарбоновые кислоты – это производные предельных углеводородов, содержащие две карбоксильные группы.
Для насыщенных дикарбоновых кислот наиболее часто используют тривиальные названия. По правилам заместительной номенклатуры ИЮПAK их названия образуют из названий алканов с тем же числом атомов углерода в главной углеродной цепи (включая углероды карбоксильных групп),
прибавляя –диовая кислота.
|
|
|
ФОРМУЛА КИСЛОТЫ |
|
|
ТРИВИАЛЬНАЯ |
ЗАМЕСТИТЕЛЬНАЯ |
||||||||||||||||||||||||||||||
|
|
|
|
|
НОМЕНКЛАТУРА |
НОМЕНКЛАТУРА |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
Щавелевая |
Этандиовая |
|||||
|
|
|
|
|
|
H |
|
|
O C |
|
|
|
C |
O |
|
|
|
H |
|
|
|
|
|
кислота |
кислота |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
O |
|
|
C |
|
|
|
CH2 |
|
|
C |
O |
|
|
|
|
|
Малоновая |
Пропандиовая |
||||||||||||
|
H |
|
|
|
O |
|
|
|
|
|
|
|
O |
|
|
|
H |
кислота |
кислота |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
Янтарная |
Бутандиовая |
|||||||
H |
|
|
O C |
|
|
CH2 |
|
|
CH2 |
|
|
C |
O |
|
H |
кислота |
кислота |
||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
O |
C |
|
|
|
(CH2)3 |
|
|
C |
|
O |
|
|
Глутаровая |
Пентандиовая |
|||||||||||||||||
H |
|
|
|
O |
|
|
|
|
|
O |
|
|
H |
кислота |
кислота |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
O |
C |
|
|
|
(CH2)4 |
|
|
C |
|
O |
|
|
Адипиновая |
Гександиовая |
|||||||||||||||||
H |
|
|
|
O |
|
|
|
|
O |
|
|
H |
кислота |
кислота |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
158 |
|

6.3.1. СПОСОБЫ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ ДИКАРБОНОВЫХ КИСЛОТ
П о л у ч е н и е щ а в е л е в о й к и с л о т ы
Окисление этиленгликоля. Продуктом глубокого окисления этиленгликоля является щавелевая кислота:
|
CH2 |
|
|
CH2 |
4[ O ] |
O |
C |
|
|
O |
|
|
|
|
|
HO |
|
C |
OH |
||||
|
|
||||||||||
- 2Н2О |
|||||||||||
|
|
|
|||||||||
|
|
|
|||||||||
OH |
|
|
|
|
|
|
|||||
|
OH |
|
|
|
|||||||
|
|
|
|
|
|
|
|||||
этиленгликоль |
|
щавелевая кислота |
|||||||||
Гидролиз динитрила щавелевой кислоты. При нагревании с водными растворами кислот и щелочей динитрил щавелевой кислоты подвергается гидролизу с образованием щавелевой кислоты:
|
|
|
|
|
|
|
|
|
2HCl |
O |
C |
|
|
|
|
O |
|
+ |
2 NH4Cl |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
4H2O |
|
HO |
|
|
OH |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
N |
|
C |
|
C |
|
|
N |
|
щавелевая кислота |
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
динитрил |
2NaOH |
|
C |
|
|
C |
|
+ |
2 NH4OH |
||||||||||||||||||
щавелевой кислоты |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
+ |
|||||||||||||||||
|
+ |
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
O Na |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
Na O |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
оксалат натрия |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2HCl |
|
O |
C |
|
C |
O |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- 2NaCl |
|
HO |
|
OH |
||||||
щавелевая кислота
Из натриевой соли муравьиной кислоты – промышленный способ получения щавелевой кислоты. Дегидрированием формиата натрия получают динатриевую соль щавелевой кислоты и подкисляют еѐ до образования щавелевой кислоты:
|
|
|
O |
|
|
|
O |
|
||||
H |
|
C |
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
O Na+ |
t |
O Na+ |
+ 2HCl |
||||||||
|
|
|
|
|
||||||||
|
|
|
O |
- H2 |
|
|
O |
- 2NaCl |
||||
H |
|
C |
C |
|||||||||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
||||
|
O Na+ |
|
O Na+ |
|
||||||||
|
|
|
|
|
|
|
||||||
O
C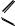 ОH
ОH
O
C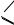 ОH
ОH
формиат натрия оксалат натрия щавелевая кислота
П о л у ч е н и е м а л о н о в о й к и с л о т ы
Из монохлоруксусной кислоты. Под действием цианистого натрия монохлоруксусную кислоту превращают в циануксусную, гидролиз которой
приводит к образованию малоновой кислоты: |
|
|
|
|
|
|
|
|
|||||||||||||||||||||
Cl |
|
CH |
|
|
C |
O |
+ Na C |
|
N |
|
|
|
N |
|
|
|
|
|
|
|
O |
+2 H2O; HCl |
|||||||
|
|
|
|
|
|
|
|
|
C |
|
CH |
|
|
C |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
2 |
OH |
|
|
|
|
|
|
2 |
OH |
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
- NaCl |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
монохлоруксусная кислота |
|
|
|
|
|
|
|
|
|
|
циануксусная кислота |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
O |
C |
|
|
CH2 |
|
|
|
|
O |
|
|
|
NH4Cl |
|
|
|
|
||||
|
|
|
|
|
|
|
|
HO |
|
|
|
C |
OH |
+ |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
малоновая кислота
159

П о л у ч е н и е я н т а р н о й к и с л о т ы
Из 1,2-дихлорэтана. Янтарную кислоту получают гидролизом еѐ динитрила, который образуется при действии цианистого натрия на 1,2- дихлорэтан:
CH2 |
|
|
CH2 + 2NaC |
|
N |
|
|
N |
|
C |
|
CH2 |
|
CH2 |
|
C |
|
N |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
Cl |
Cl |
- 2NaCl |
||||||||||||||||
|
|
|
динитрил янтарной кислоты |
|||||||||||||||
1,2-дихлорэтан
+4 H2O; 2 HCl
O |
|
|
|
|
|
|
|
O |
|
HO |
C |
|
CH2 |
|
CH2 |
|
C |
+ |
2 NH4Cl |
|
|
|
|||||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
янтарная кислота |
|
|
||||
Г л у т а р о в а я и а д и п и н о в а я к и с л о т ы могут быть получены окислением соответствующих циклических кетонов:
CH2 |
|
|
|
CH2 |
O |
|
3 [O] |
O |
|
|
|
|
|
|
|
|
|
O |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
HO |
C |
|
|
(CH2)3 |
|
|
C |
OH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
(HNO3) |
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
циклопентанон |
|
|
|
|
|
|
|
глутаровая кислота |
|
||||||||||||||||||
|
CH2 |
|
|
|
CH2 |
|
|
|
3 [O] |
O |
C |
|
|
(CH2)4 |
|
|
C |
O |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
CH2 |
|
|
|
C |
|
|
O |
|
|
|
|
HO |
|
|
|
OH |
|||||||||||
|
|
|
|
|
|
(HNO3) |
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
CH2 |
|
|
|
|
CH2 |
|
|
|
адипиновая кислота |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
циклогексанон |
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Адипиновая кислота используется для производства синтетического волокна найлона. Поликонденсацией адипиновой кислоты с гексаметилендиамином получают полиамиды, способные в размягчѐнном состоянии вытягиваться в чрезвычайно прочные нити (см. раздел «Фенолы»).
6.3.2. ХИМИЧЕСКИЕ СВОЙСТВА НАСЫЩЕННЫХ ДИКАРБОНОВЫХ КИСЛОТ
По химическим свойствам дикарбоновые кислоты во многом сходны с монокарбоновыми. Они образуют одни и те же функциональные производные, с тем лишь отличием, что реакции могут идти с участием как одной, так и двух карбоксильных групп. Например, они образуют полные и неполные сложные эфиры, галогенангидриды, амиды карбоновых кислот, нейтральные и кислые соли. Причѐм, как указывалось ранее, по первой ступени диссоциации дикарбоновые кислоты значительно сильнее, чем по второй:
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ H+ |
HO |
|
C |
|
|
(CH2)n |
|
|
C |
|
|
|
OH |
|
|
|
HO |
|
C |
|
(CH2)n |
|
C |
|
O |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ H+ |
|||||
HO |
|
|
C |
|
|
(CH2)n |
|
C |
|
O |
|
|
|
|
|
O |
|
C |
|
(CH2)n |
|
C |
|
O |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
Вместе с тем дикарбоновые кислоты проявляют некоторые
специфические химические свойства.
160

В молекуле малоновой кислоты атомы водорода метиленовой группы имеют значительную подвижность. Это объясняется с одной стороны электроноакцепторным влиянием карбоксильных групп, а с другой – устойчивостью карбаниона, образующегося из малоновой кислоты после отрыва от неѐ протона метиленовой группы. Устойчивость карбаниона в значительной степени объясняется тем, что отрицательный заряд в нѐм делокализован за счѐт эффекта сопряжения с карбонильными группами:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
H |
O |
|
|
|
|
|
O |
|
O |
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
H+ |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
HO C |
|
|
|
|
|
|
|
|
|
|
|
HO C C |
|
|
|
|
|
|||||||||||||||
|
C C H |
|
|
|
|
C H |
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
малоновая кислота |
|
|
|
|
|
|
карбанион |
|
|
||||||||||||||||||||||
Поэтому возникает возможность проведения реакций замещения α- водородных атомов. В частности в эфирах малоновой кислоты они легко замещаются атомами щелочных металлов. Так, из диэтилового эфира малоновой кислоты при действии натрия или алкоголята натрия получается
натриймалоновый эфир:
|
COOH |
|
|
|
|
|
|
|
|
COOC2H5 |
+ Na |
|
COOC2H5 |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
CH |
|
+ |
2C H OH |
|
|
|
CH |
|
|
|
|
|
Na+ + |
1/2 H |
|
|||||||
|
|
|
|
|
|
|
|
|
НC |
|
2 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
2 |
|
2 |
5 |
- 2H2O |
|
|
|
2 |
|
C H OH |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
5 |
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
COOC2H5 |
|
|
|
COOC2H5 |
|
|
|||||||||
малоновая кислота |
|
|
|
|
|
диэтиловый эфир |
|
|
|
натриймалоновый эфир |
|
|||||||||||
|
|
|
|
|
|
|
|
|
малоновой кислоты |
|
|
|
|
|
|
|
|
|
||||
Натриймалоновый эфир легко алкилируется, ацилируется и реагирует с другими электрофильными реагентами. Эти свойства широко используются в практике для получения моно- и дикарбоновых кислот.
Синтезы на основе натриймалонового эфира
Синтез линейных монокарбоновых кислот. Натриймалоновый эфир алкилируют галогеналканом до алкилмалонового эфира, который в процессе гидролиза превращается в алкилмалоновую кислоту. Алкилмалоновые кислоты, содержащие две карбоксильные группы у одного углеродного атома, легко декарбоксилируются с образованием линейных монокарбоновых кислот:
|
COOC2H5 |
R-Cl |
|
COOC2H5 |
2 H2O; H2SO4 |
|
|
COOH |
t |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
НC Na+ |
|
НC |
|
R |
|
НC |
|
R |
|
R |
|
CH2 |
COOH |
|||||||||||
|
- NaCl |
|
|
-2 C2H5OH |
|
|
|
|
|
|
||||||||||||||
|
|
|
|
- СО2 |
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
COOC2H5 |
|
COOC2H5 |
|
|
COOH |
|
|
|
|
линейная |
||||||||||||||
натриймалоновый |
|
алкилмалоновый |
|
|
алкилмалоновая |
|
|
|
монокарбоновая |
|||||||||||||||
|
|
эфир |
|
|
|
эфир |
|
|
кислота |
|
|
|
|
кислота |
||||||||||
Синтез разветвлѐнных монокарбоновых кислот. Для получения разветвлѐнных монокарбоновых кислот надо последовательно заменить алкильными группами оба атома водорода метиленовой группы в малоновом эфире:
161

|
|
COOC2H5 |
|
|
COOC2H5 |
|
|
|
|
|
|
|
|
|
|
|
COOC2H5 |
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
Na+ |
|
|
|
|
R-Cl |
|
|
|
|
|
|
|
|
|
+ Na |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R'-Cl |
|||||||
НC |
|
|
|
|
|
|
|
НC |
|
R |
|
|
|
|
|
|
|
|
|
Na+C |
|
|
R |
|
|
|
||||||||||||||||
|
|
|
|
|
- NaCl |
|
|
- 1/2 H2 |
|
|
- NaCl |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
COOC2H5 |
COOC2H5 |
|
|
|
|
|
|
|
|
|
COOC2H5 |
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
COOC2H5 |
2 H2O; H2SO4 |
|
|
|
|
|
COOH |
t |
|
|
|
|
|
|
R |
|
CH |
|
|
COOH |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
R' |
|
C |
|
R |
R' |
|
|
C |
|
R |
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
-2 C H OH |
|
|
|
|
|
|
|
|
|
- СО2 |
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
2 |
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R' |
|
|
|
||||
|
|
|
|
|
|
|
COOC2H5 |
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
разветвлённая |
||||||
монокарбоновая кислота
Синтез дикарбоновых кислот. При действии на натриймалоновый эфир эфиров α-галогенкарбоновых кислот образуются дикарбоновые кислоты:
|
COOC2H5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOC2H5 |
|
|
3 H2O; H2SO4 |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
НC |
|
Na+ + |
CH |
|
|
|
COOC H |
|
|
|
|
|
|
НC |
|
CH |
|
|
|
COOC H |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
2 |
2 |
5 |
- NaCl |
|
|
|
|
2 |
|
|
|
2 |
5 |
-3 C2H5OH |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
COOC2H5 |
|
|
|
|
|
|
|
|
|
|
|
|
COOC2H5 |
|
|
|
|
||||||||||||||||
|
этиловый эфир |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
натриймалоновый |
монохлоруксусной |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
эфир |
|
|
|
|
|
кислоты |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
t |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
НC |
|
|
|
COOH |
|
|
|
НООС |
|
|
CH2 |
|
CH2 |
COOH |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
- СО2 |
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
бутандиовая (янтарная) кислота |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
||||||||||||||||||
============================================================
6.4. ГАЛОГЕНОЗАМЕЩЁННЫЕ НАСЫЩЕННЫЕ МОНОКАРБОНОВЫЕ КИСЛОТЫ
============================================================
Галогенозамещѐнные насыщенные монокарбоновые кислоты – это производные насыщенных монокарбоновых кислот, в углеводородном радикале которых один или несколько атомов водорода замещены атомами галогенов.
По правилам заместительной номенклатуры ИЮПAK названия галогенозамещѐнных насыщенных монокарбоновых кислот образуют из названий насыщенных монокарбоновых кислот, указывая положение атома галогена цифрами. Часто названия строят из тривиальных названий предельных монокарбоновых кислот, используя в качестве локантов греческие буквы:
CH2 |
|
|
COOH |
2-хлорэтановая кислота, |
||||
|
|
|||||||
Cl |
|
|
|
|
|
|
-хлоруксусная кислота |
|
CH3 |
|
|
|
CH |
|
COOH |
2-хлорпропановая кислота, |
|
|
|
|
||||||
|
|
|||||||
|
|
|
Cl |
-хлорпропионовая кислота |
||||
|
|
|
|
|
|
|
|
162 |
