
11. Химия - Chemistry / Біонеорганічна, фізколоїдна і біоорганічні хімія. Вибрані лекції _Л.О. Гоцуляк, О.О. Мардашко та ін. - О_ ОДМУ, 1999. - 248 с
.pdf
OH |
Фермент |
OH |
|
O |
|
|
|
|
H N |
|
|
N |
N HNO2 N |
|
N |
N H |
|
H2N N N |
N2, H2O |
|
|
|
|
HO N |
N |
O N |
N |
||
H |
|
|
H |
H |
|
Гуанін |
|
|
|
Ксантин |
|
Велике значення для медичної практики мають метильовані за атомом азоту ксантини: теофілін, теобромін і кофеїн. Вони збуджують ЦНС, а малими дозами — підвищують працездатність.
H3C |
|
O |
|
|
|
|
H |
|
O |
|
|
|
|
|
|
O |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
N |
1 |
5 |
|
7 |
N H |
N |
1 |
6 |
5 |
|
7 |
N CH |
6 |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
3 |
N1 |
5 |
|
7 N CH3 |
||||||||
|
2 |
|
|
4 |
|
8 |
|
2 |
|
|
4 |
|
8 |
|
|
|
|
|
||||
O |
3 |
9 |
O |
3 |
9 |
|
|
2 |
3 |
4 |
9 |
8 |
||||||||||
|
N |
|
N |
|
|
|
N |
|
N |
|
|
|
O |
N |
|
N |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Теофілін |
|
|
|
|
Теобромін |
|
|
|
Кофеїн |
|
||||||||||||
(1,3-диметилксантин) |
(3,7-диметилксантин) |
|
(1,3,7-триметилксантин) |
|||||||||||||||||||
Теобромін міститься в зернах какао (близько 1,8 %), теофілін і кофеїн — у листі чаю та зернах кави.
Сечова кислота, чи 2,6,8-тригідроксипурин, є одним із кінцевих продуктів метаболізму нуклеїнових кислот. Вона виводиться з сечею (близько 1 г на добу).
H |
O |
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N1 |
6 |
5 |
|
|
7 N |
|
H |
|
|
|
|
N1 |
6 5 |
|
7N |
|
H |
|||
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
2 |
3 |
4 |
9 |
8 |
O |
|
|
|
HO |
2 |
3 |
4 |
9 |
8 |
OH |
|||||
|
|
|
||||||||||||||||||
O |
N |
|
N |
|
|
|
|
|
N |
|
N |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
H |
|
|
Сечова кислота |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
(2,6,8-тригідроксипурин)
В організмі тварин сечова кислота синтезується з сечовини. Амонійні солі сечової кислоти дуже погано розчиняються у воді.
219
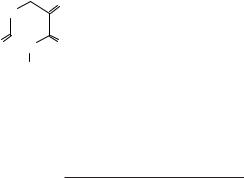
При порушенні обміну речовин в організмі солі сечової кислоти (урати) відкладаються в суглобах (подагра), а також у вигляді ниркового каміння.
Окислення сечової кислоти за лабораторних умов, наприклад, при дії азотної кислоти, призводить до руйнування імідазольного кільця й утворення алоксану.
O
H

 O
O
N
O  N O
N O
H
Алоксан
Лекція 4
ХІМІЯ БІЛКІВ І НУКЛЕЇНОВИХ КИСЛОТ
α-Амінокислоти як структурні ланки білків
Класифікація, номенклатура й ізомерія амінокислот
Органічні сполуки, що містять у молекулі карбоксильну групу –СООН і аміногрупу –NH2, називаються амінокислотами.
Значення амінокислот надзвичайно велике, бо всі пептиди і білки побудовані із залишків α-амінокислот. Серед них виділено групу з 20 найбільш важливих α-амінокислот, які постійно наявні в усіх білках (табл. 6.1).
Основним джерелом α-амінокислот для живого організму є харчові білки. Багато α-амінокислот синтезується в живому організмі. Але деякі α-амінокислоти, необхідні для синтезу білків і підтримання азотистого балансу, синтезуватися не можуть і повинні надходити ззовні. Такі амінокислоти називають незамінними. До них належать валін, лейцин, ізолейцин, лізин, треонін, метіонін, фенілаланін, триптофан. До організму незамінні амінокислоти надходять з білковою їжею.
При деяких, здебільшого природжених хворобах, кількість незамінних амінокислот збільшується.
220

Таблиця 6.1. Фізичні константи найважливіших α-амінокислот
Аміно- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Умовне |
|
Ізоелек- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Формула |
Т , °С |
трична |
||||||||||||
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
позна- |
пл. |
точка, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
чення |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
рІ |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
2 |
|
|
|
|
|
|
3 |
|
4 |
5 |
|||||||||||||||
Гліцин |
|
|
CH2–COOH |
Глі |
292 |
6,0 |
|||||||||||||||||||||||
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Аланін |
CH3– |
|
CH–COOH |
Ала |
297 |
6,0 |
|||||||||||||||||||||||
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
NH2 |
|
|
|
|
|||||||||||||||||||
Валін |
(CH3)2CH– |
|
CH–COOH |
Вал |
315 |
6,0 |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|||||||||
Лейцин |
(CH3)2CH–CH2 |
|
–CH–COOH |
Лей |
337 |
6,0 |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Ізолейцин |
C2H5 |
CH–CH–COOH |
Ілей |
284 |
6,0 |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
CH3 NH2 |
|
|
|
|
|||||||||||||||||||||
Аспарагінова |
HOOC–CH2 |
|
–CH–COOH |
Асп |
270 |
2,8 |
|||||||||||||||||||||||
|
|||||||||||||||||||||||||||||
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|||||||||
Глутамінова |
HOOC–CH2–CH2 |
|
–CH–COOH |
Глу |
249 |
3,2 |
|||||||||||||||||||||||
|
|||||||||||||||||||||||||||||
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|||
Орнітин |
CH2–CH2–CH2 |
|
–CH–COOH |
Орн |
140 |
9,5 |
|||||||||||||||||||||||
|
|||||||||||||||||||||||||||||
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|||||||||
Лізин |
CH2–CH2–CH2–CH2 |
|
–CH–COOH |
Ліз |
224 |
9,7 |
|||||||||||||||||||||||
|
|||||||||||||||||||||||||||||
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
||||
Серин |
|
CH2 |
|
–CH–COOH |
Сер |
228 |
5,7 |
||||||||||||||||||||||
|
|||||||||||||||||||||||||||||
|
|
OH |
|
|
|
|
NH2 |
|
|
|
|
||||||||||||||||||
Треонін |
CH3 |
|
–CH–CH–COOH |
Тре |
253 |
5,9 |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
OH NH2 |
|
|
|
|
|||||||||||||||||||||
Цистеїн |
CH2 |
|
–CH–COOH |
цис-SH |
178 |
5,1 |
|||||||||||||||||||||||
|
|||||||||||||||||||||||||||||
|
SH |
NH2 |
|
|
|
|
|||||||||||||||||||||||
Цистин |
|
|
|
|
|
|
|
|
|
NH2 |
цис-S |
260 |
5,0 |
||||||||||||||||
|
S–CH2–CH–COOH |
||||||||||||||||||||||||||||
|
|
S–CH2 |
|
–CH–COOH |
|
|
|
|
|||||||||||||||||||||
|
|
|
цис-S |
|
|
||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|||||||||||||
221
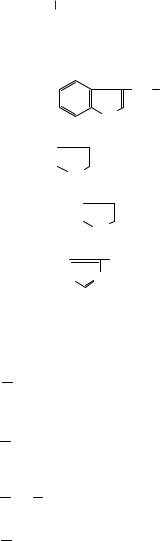
Закінчення табл. 6.1
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
3 |
4 |
5 |
||||
Метіонін |
|
|
CH2–CH2 |
|
–CH–COOH |
Мет |
283 |
5,7 |
||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||
|
|
|
S–CH3 |
|
|
NH2 |
|
|
|
|||||||||||||||||||||
Фенілаланін |
CH2 |
|
–CH–COOH |
Фен |
275 |
5,5 |
||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
C6H5 NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Тирозин |
параHO–C6H4–CH2 |
|
–CH–COOH |
Тир |
344 |
5,7 |
||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
||
Триптофан |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
CH |
|
COOH |
Три |
282 |
5,9 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
NH2 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Пролін |
|
|
|
|
|
|
|
|
|
COOH |
Про |
299 |
6,3 |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
NH |
|
|||||||||||||||||||||||||||
Гідрокси- |
HO |
|
|
|
|
|
|
|
|
|
COOH |
Про-ОН |
270 |
5,8 |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
пролін |
|
|
|
|
|
|
|
|
|
NH |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
CH |
|
COOH |
|
|
|
||||||||||
Гістидин |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
Гіс |
277 |
7,5 |
|||||||||||||
HN |
N |
|
|
|
NH2 |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Назва амінокислоти за номенклатурою IUPAC складається з назви відповідної кислоти і префікса «аміно-» з означенням положення групи NH2 в радикалі.
Наприклад,
|
|
CH2 |
COOH |
Гліцин, глікокол, або амінооцтова |
||||
|
||||||||
|
|
|
|
|
|
|
(2-аміноетанова) кислота |
|
NH2 |
|
|
|
|
||||
|
|
|
|
|
|
|||
|
|
|
α |
|
|
|||
CH3 |
|
CH |
|
COOH |
α -Аланін, або |
α-амінопропіонова |
||
|
|
|||||||
|
|
|
||||||
|
|
|
|
|
|
|
(2-амінопропанова) кислота |
|
|
|
|
NH2 |
|||||
|
|
|
|
|
||||
βα
|
|
CH2 |
CH2 |
COOH |
β-Аланін, або |
β-амінопропіонова |
||||||
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
(3-амінопропанова) кислота |
|
NH2 |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|||
CH3 |
|
|
CH |
|
|
CH |
|
COOH |
Валін, або α-аміноізовалеріанова |
|||
|
|
|
|
|||||||||
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
(2-аміно-3-метилбутанова) кислота |
|
|
|
|
CH3 |
NH2 |
||||||||
|
|
|
|
|
||||||||
222
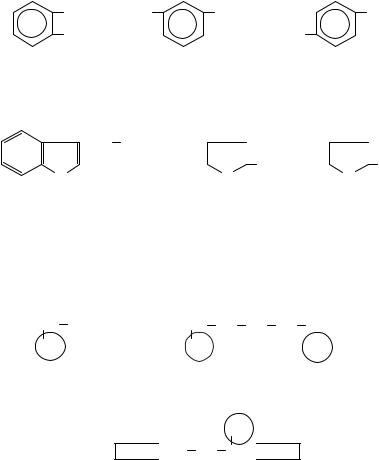
Однак для амінокислот, що беруть участь у побудові білків, застосовуються в основному тривіальні назви.
У назві ароматичних амінокислот як родоначальник структури використовується бензойна кислота. Ароматичні амінокислоти існують у вигляді орто-, мета- і параізомерів:
COOH |
H2N |
COOH |
COOH |
NH2 |
|
|
H2N |
орто-Амінобензойна |
мета-Амінобензойна |
пара-Амінобензойна |
|
кислота |
|
кислота |
кислота |
Наприклад, гетероциклічними є такі амінокислоти:
|
|
|
CH2 |
|
CH |
|
COOH |
4 |
3 |
|
|
HO |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
NH2 |
5 |
1 2 |
|
COOH |
|
|
|
|
|
COOH |
||||
|
|
|
|
|
|
|||||||||||||
N |
|
N |
|
|
|
|
N |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
H |
|
|
|
|
H |
|||||||||||
|
Триптофан |
|
Пролін |
|
|
Гідроксипролін |
||||||||||||
Амінокислоти, в яких кількість аміногруп перебільшує кількість карбоксильних, називають основними (наприклад, лізин), а при надлишку карбоксильних груп — кислими (наприклад, глутамінова кислота).
|
|
|
|
ε |
δ |
γ |
β |
α |
|
||||
|
CH2 |
COOH |
|
|
CH2 |
CH2 |
CH2 |
CH2 |
|
CH |
|
|
COOH |
|
|
|
|
||||||||||
|
NH2 |
|
NH2 |
|
|
|
|
|
|
|
|||
|
|
|
|
NH2 |
|||||||||
|
Гліцин |
|
|
|
|
Лізин |
|
|
|
|
|
||
(нейтральна кислота) |
|
|
(основна кислота) |
||||||||||
NH2
HOOC  CH2 CH2 CH
CH2 CH2 CH
 COOH
COOH
Глутамінова кислота (кисла)
Ізомерія амінокислот
Для амінокислот характерна структурна і просторова ізомерія. Структурна ізомерія зумовлена будовою вуглецевого ланцюга і положенням аміногрупи в радикалі.
223

Структурна ізомерія
1. Ізомерія вуглецевого ланцюга:
α
4 |
|
|
|
3 |
|
|
|
|
2 |
|
1 |
2-амінобутанова (α-аміномасляна) кислота |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
CH2 |
|
|
CH |
|
COOH |
|||||||||||
|
|
|
|
|
||||||||||||||
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|||
|
|
|
|
|
CH |
31 |
|
|
|
|
|
|
|
|||||
3 |
|
|
2 |
|
α |
|
|
|
|
|
|
2-аміно-2-метилпропанова (α-аміноізомасляна) |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
C |
COOH |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислота |
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
2. Ізомерія положення функціональної групи: |
||||||||||||||||||
γ |
|
β |
|
|
α |
|
|
|
||||||||||
4 |
|
|
|
3 |
|
|
|
|
2 |
|
1 |
2-амінобутанова (α-аміномасляна) кислота |
||||||
CH3 |
|
CH2 |
|
|
CH |
|
|
COOH |
||||||||||
|
|
|
|
|||||||||||||||
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
||
γ |
|
β |
|
|
α |
1 |
|
|||||||||||
4 |
|
|
|
3 |
|
|
|
|
2 |
|
3-амінобутанова (β-аміномасляна) кислота |
|||||||
CH3 |
|
|
|
CH |
|
CH2 |
|
COOH |
||||||||||
|
|
|||||||||||||||||
|
|
|
||||||||||||||||
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|||||
γ |
|
β |
|
|
α |
|
|
|
||||||||||
4 |
|
|
3 |
|
|
|
|
2 |
|
1 |
4-амінобутанова (γ-аміномасляна) кислота |
|||||||
|
CH |
|
|
CH2 |
CH2 |
|
COOH |
|||||||||||
2 |
|
|
||||||||||||||||
|
|
|
||||||||||||||||
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Оптична ізомерія
Оптична ізомерія пов’язана з тим, що в усіх амінокислотах, крім гліцину, є асиметричний (хіральний) атом вуглецю, зв’я- заний з чотирма різними замісниками.
|
|
COOH |
|
|
COOH |
|||||
H N |
|
C* |
H |
H |
|
C* |
NH |
|||
|
|
|||||||||
2 |
|
|
CH3 |
|
|
2 |
||||
|
|
|
||||||||
|
|
|
|
|
|
CH3 |
||||
L-Аланін |
D-Аланін |
|||||||||
Відносна конфігурація D- і L-амінокислот визначається як і у гідроксикислот за конфігураційним еталоном — гліцериновим альдегідом.
За R-, S-системою позначень α-амінокислоти L-ряду мають S-, а D-ряду — R-конфігурацію (за виключенням цистеїну).
224

HO O |
HO O |
||||||||
|
|
C |
|
|
C |
||||
H2N |
|
C* |
H |
H |
|
C* |
NH2 |
||
|
|
||||||||
|
|||||||||
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
R |
||||
L(S)-Амінокислота |
D(R)-Амінокислота |
||||||||
Пара енантіомерів
Майже всі природні α-амінокислоти на відміну від вуглеводів належать до L-ряду. α-Амінокислоти D-ряду іноді називають «неприродними», тому що вони не беруть участі в біосинтезі білків у організмі людини та тварин.
Амінокислоти, що належать до різних стереохімічних рядів, різняться за смаком. Наприклад, D-глутамінова кислота не має смаку, а L-глутамінова має смак м’яса.
Використання для побудови білків організму людини та тварин тільки одного виду стереоізомерів α-амінокислот, а саме енантіомерів L-ряду, має важливе значення для формування просторової структури білків і виявлення ними біологічної активності. З цим безпосередньо пов’язана стереоспецифічність дії ферментів.
Макромолекули ферментів також побудовані з L-α-аміно- кислот, тобто з хірального матеріалу. В цілому вони є хіральними, тому вступають у взаємодію тільки з тими субстратами, які також мають визначену конфігурацію.
Методи одержання і властивості амінокислот
За лабораторних умов α-амінокислоти одержують двома способами:
1. Ціаногідринний синтез (реакція Зелінського — Стаднікова)
NH4Cl + KCN  NH4 C
NH4 C N + KCl
N + KCl
NH4 C  N
N  NH3 + H C
NH3 + H C  N
N
Ціанід амонію
|
|
|
δ |
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
δ+ |
O |
δ+ δ |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
+ |
H |
|
C |
|
N |
|
R |
|
C |
|
C |
|
N |
||||||
|
|
|
|
|
|
|
||||||||||||||
R |
|
C |
|
|
|
|
|
|
||||||||||||
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
H |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Гідроксинітрил |
|||||||
225

NH3 |
|
|
|
|
NH2 |
3HOH |
|
|
|
NH2 |
OH |
||||||||||||
|
|
||||||||||||||||||||||
|
R |
|
C |
|
C |
|
N |
|
|
|
|
|
R |
|
C |
|
C |
|
OH |
||||
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||
H2O |
|
|
|
|
|
|
|
|
|
|
|
NH3 |
|
|
|
|
|
|
OH |
||||
|
H |
|
|
H |
|||||||||||||||||||
|
α-Амінонітрил |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
O |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
R |
|
CH |
|
C |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
H2O |
|
|
|
|
OH |
|
|
||||||||||
Амінокислота
2. Амоноліз α-галогенокарбонових кислот
R |
|
|
|
CH |
|
COOH + 2NH3 |
|
R |
|
|
|
CH |
|
COOH + NH4Cl |
|
|
|
|
|
||||||||||
|
|
|
|
|||||||||||
|
|
|
|
Hal |
|
|
|
NH2 |
||||||
У живих організмах синтез відбувається з використанням доступних метаболітів іншої хімічної природи (наприклад, кетокислот) й інших амінокислот.
1. Відновне амінування. Відновлюючий реагент-кофермент НАДН + Н+ — нікотинамід аденіндинуклеотид.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
НАДН+ Н+ |
||
HOOC |
|
CH2 |
CH2 |
C |
|
COOH + NH3 |
|
|
|
||||||||
|
|
|
|
||||||||||||||
|
|
|
|
|
|||||||||||||
|
НАД+ |
||||||||||||||||
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
O |
|
||||||||||
|
α-Кетоглутарова кислота |
|
|
|
|||||||||||||
|
|
|
|
HOOC |
|
|
CH2 |
CH2 |
CH |
|
COOH + H2O |
||||||
|
|
|
|
|
|
||||||||||||
NH2
L-Глутамінова кислота
α-Кетоглутарова кислота завжди міститься в клітинах (як продукт метаболізму вуглеводів). У процесі цієї реакції in vivo утворюється тільки один стереоізомер, а саме α-амінокисло- та L-ряду, що зумовлене стереоспецифічною будовою ферменту, який каталізує цю реакцію.
2. Переамінування (трансамінування)
Потрібна для організму α-амінокислота (II) синтезується з α-амінокислоти (І), що міститься в клітинах достатньою або надлишковою кількістю. Реакція відбувається з участю ферментів трансаміназ і коферменту піридоксальфосфату. В цілому переамінування зводиться до взаємного обміну двох функціональних груп — аміно і карбонільної.
226

Наприклад, синтез в організмі L-глутамінової кислоти з L- аспарагінової:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Трансаміназа |
||||||
HOOC |
|
|
CH2 |
|
CH |
|
|
COOH + |
HOOC |
|
|
CH2 |
CH2 |
C |
|
COOH |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
O |
|||||||||||||||||||
|
L-Аспарагінова2 кислота (І) |
α-Кетоглутарова кислота |
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
HOOC |
|
CH2 |
C |
|
COOH + |
HOOC |
|
CH2 |
CH2 |
|
CH |
|
COOH |
|||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|||||||||
|
|
|
|
|
|
Щавлевооцтова кислота |
L-Глутамінова кислота (ІІ) |
|||||||||||||||||||||||||||
Процес переамінування є сполучною ланкою між метаболізмом білків (амінокислоти) і ліпідів (кетокислоти). Таким чином, ліквідується надлишок окремих амінокислот і регулюється їх вміст у клітинах.
Фізичні властивості
α-Амінокислоти — безбарвні кристалічні речовини з високою температурою плавлення (понад 200 °С), добре розчинні у воді, дуже слабко — в органічних розчинниках. Водні розчини одноосновних амінокислот мають рН = 6,8. Висока температура плавлення, відсутність у спектрах ліній, характерних для карбоксильної й аміногруп, пояснюється їх своєрідною будовою. Вони є внутрішніми солями (біполярні іони):
|
|
O |
|
|
|
|
|
O |
|
CH2 |
C |
|
|
|
|
CH2 |
C |
|
|
|
||||||
|
|
|
|
|||||
|
|
OH |
|
|
|
+ |
|
O |
NH |
NH |
|||||||
2 |
|
3 |
|
|||||
Такий біполярний іон у кислому середовищі переходить у катіонну, а в лужному — в аніонну форму.
Хімічні властивості
Кислотно-основні властивості. a-Амінокислоти є амфотер-
ними сполуками, тобто утворюють солі як з лугами, так і кислотами. Це зумовлене наявністю в їх молекулі функціональних груп кислотного (СООН) і основного (NH2) характеру:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
R |
|
|
|
|
|
CH |
|
|
COO |
|
+ |
H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
CH |
|
COOH |
|
|
|
R |
|
CH |
|
COO |
|
|
|
|
+ |
|
|
NH2 |
|
||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
H |
|
|||||||||||||
|
|
|
NH |
|
|
|
|
NH |
|
|
|
R |
|
CH |
|
COOH |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
2 |
|
3 |
|
|
|
|
|
+ |
|
NH |
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|||||||||
227

У водному розчині існує рівновага між катіонною й аніонною формою і біполярним іоном. Положення рівноваги залежить від рН середовища.
|
|
|
|
|
|
|
H+ |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
||||||||||||||
R |
|
CH |
|
COOH |
|
|
|
R |
|
CH |
|
COO |
|
|
|
|
|
R |
|
CH |
|
COO |
|||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
+ |
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
NH3 |
|
|
NH3 |
|
|
|
|
|
|
|
NH2 |
||||||||||||||||
Катіонна форма |
Біполярний іон |
|
|
|
|
|
Аніонна форма |
||||||||||||||||||||||
Якщо сумарний заряд молекул дорівнює чи близький до 0, наприклад, у біполярному іоні гліцину, то молекула електронейтральна, тобто перебуває в ізоелектричному стані.
В ізоелектричній точці амінокислоти мають мінімальну електрофоретичну рухливість.
Розділення суміші амінокислот хроматографічним методом грунтується на відмінності кислотно-основних властивостей — здатності адсорбуватися на твердій фазі.
Реакції за карбоксильною групою
1. Утворення солей α-Амінокислоти утворюють з основами звичайні солі, а з
катіонами важких металів — забарвлені розчинні у воді внутрішньокомплексні сполуки:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H N |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
C |
O |
2 .. |
HC |
|
|
R |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
R |
|
CH |
|
COOH |
+ Cu(OH)2 |
|
|
|
|
|
|
|
|
|
|
|
|
Cu |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
2H2O R |
|
|
|
|
CH .. |
|
O |
|
C |
|
|
O |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Синій колір |
|
|
||||||
2. Утворення ефірів (реакція етерифікації) |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
H+ |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|||||
R |
|
CH C |
+ HO |
|
CH |
|
|
|
|
|
R |
|
|
CH |
C |
|
|
+ H |
O |
||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
O |
2 |
|
|
|||||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
||||||||||||
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Складні ефіри не мають біполярної будови, тому добре розчиняються в органічних розчинах, леткі.
228
