
-
Умова квантування атомних орбіт в теорії Бора
Т еорія
Бора була першою спробою впровадження
квантових уявлень в атомну фізику і
тому була досить недовершеною. Спроби
її удосконалення мали місце, зокрема,
в роботах Зоммерфельда котрий розглянув
наслідки існування для електрону в
атомі водню не лише колових, але також
і еліптичних орбіт. Якщо для колових
орбіт єдиною змінною координатою в
полярній системі координат (
еорія
Бора була першою спробою впровадження
квантових уявлень в атомну фізику і
тому була досить недовершеною. Спроби
її удосконалення мали місце, зокрема,
в роботах Зоммерфельда котрий розглянув
наслідки існування для електрону в
атомі водню не лише колових, але також
і еліптичних орбіт. Якщо для колових
орбіт єдиною змінною координатою в
полярній системі координат (![]() )
є лише полярний кут
)
є лише полярний кут
![]() (тоді як
(тоді як
![]() ),
то для еліптичних орбіт змінними під
час руху є як полярний кут
),
то для еліптичних орбіт змінними під
час руху є як полярний кут
![]() ,
так і радіус-вектор
,
так і радіус-вектор
![]() (мал.5.1.3)
(мал.5.1.3)
Дискретний
квантовий набір стаціонарних орбіт
електрону в теорії Бора визначався
єдиним квантовим числом
![]() :
:
|
|
(5.1.7) |
Як
видно з наведених вище формул, квантове
число
![]() визначає в теорії Бора квантування:
визначає в теорії Бора квантування:
-
радіусів орбіт та швидкостей електрону на них
-
квантування моментів імпульсу на стаціонарних орбітах
-
квантування рівнів повної механічної енергії електрону.
Результати
теорії Зоммерфельда впроваджують в
теорію атому водню додаткові квантові
числа (![]() )
і ускладнюють умови квантування як
модуля моменту імпульсу електрону:
)
і ускладнюють умови квантування як
модуля моменту імпульсу електрону:
|
|
(5.1.8) |
так
і його проекції на полярну вісь
![]() :
:
|
|
(5.1.9) |
Передбачається також чітка ієрархія трьох квантових чисел:
|
Назва квантового числа |
Символ |
Діапазон зміни |
Місце в ієрархії |
|
Головне квантове число |
|
|
Незалежне |
|
Орбітальне (або азимутальне) квантове число |
|
|
Підкорене
головному:
|
|
Магнітне квантове число |
|
|
Підкорене
орбітальному:
|
Як
видно з умови квантування Зоммерфельда
(5.1.8) квадрат моменту імпульсу електрону
на стаціонарній орбіті з головним
квантовим числом
![]() може приймати дискретний ряд значень
(загалом
може приймати дискретний ряд значень
(загалом
![]() різних значень):
різних значень):
|
|
(5.1.10) |
тоді
як в теорії Бора квадрат моменту імпульсу
на тій самій орбіті може приймати
одне-єдине значення
![]() ,
яке, до того ж, відрізняється від
максимального значення у наборі
Зоммерфельда:
,
яке, до того ж, відрізняється від
максимального значення у наборі
Зоммерфельда:
![]() .
.
Ця
розбіжність випливає з того, що Зоммерфельд
припускав для кожного стаціонарного
по енергії стану електрону декілька (а
саме
![]() )
різних орбіт відповідно до низки
припустимих орбітальних чисел:
)
різних орбіт відповідно до низки
припустимих орбітальних чисел:
![]() (колова орбіта),
(колова орбіта),
![]() (еліптичні орбіти різного ексцентриситету).
Отже розглянутий випадок з
(еліптичні орбіти різного ексцентриситету).
Отже розглянутий випадок з
![]() ,
коли можуть існувати одна колова і дві
еліптичні орбіти. Умови квантування
орбіт Зоммерфельда, таким чином, є більш
реалістичними, а набір квантових чисел
більш повним, ніж в теорії Бора.
,
коли можуть існувати одна колова і дві
еліптичні орбіти. Умови квантування
орбіт Зоммерфельда, таким чином, є більш
реалістичними, а набір квантових чисел
більш повним, ніж в теорії Бора.
-
Закономірності атомних спектрів поглинання та випромінювання воднеподібних атомів
Дискретність
енергетичних рівнів електрона в атомі
водню автоматично означає і дискретність
спектрів випромінювання та поглинання
цих атомів. Згідно з другим постулатом
Бора та виразом (5.1.7)частота випромінюваного
кванту під час переходу
![]() відповідає рівнянню:
відповідає рівнянню:
|
|
(5.1.11) |
де
константу
![]() - називають сталою
Ридберга.
- називають сталою
Ридберга.
Зафіксуємо
у формулі значення:
![]() .
Тобто розглянемо переходи з усіх
збуджених рівнів на основний рівень
енергії. Тоді формула (5.1.11) спроститься
до вигляду:
.
Тобто розглянемо переходи з усіх
збуджених рівнів на основний рівень
енергії. Тоді формула (5.1.11) спроститься
до вигляду:
|
|
(5.1.12) |
Згідно
з (5.1.12) існує необмежений (інфінітний)
дискретний набір частот (спектральних
ліній) поміж значеннями частот: мінімальної
![]() (для переходів на основного рівня на
збуджений рівень з
(для переходів на основного рівня на
збуджений рівень з
![]() )
та максимальної
)
та максимальної
![]() (для переходів на рівень
(для переходів на рівень
![]() ).
Такий набір спектральних ліній є відомим
експериментально в ультрафіолетовому
діапазоні спектру і має назву серії
Лаймана.
).
Такий набір спектральних ліній є відомим
експериментально в ультрафіолетовому
діапазоні спектру і має назву серії
Лаймана.
Аналогічні
переходи на рівень
![]() ,
які мають частоти у видимому діапазоні
(в інтервалі частот
,
які мають частоти у видимому діапазоні
(в інтервалі частот
![]() ),
є відомими у спектроскопії як серія
Пальмера).
),
є відомими у спектроскопії як серія
Пальмера).
Аналогічний
до водню вигляд спектру поглинання та
випромінювання мають так звані
воднеподібні системи: наприклад, іони
із зарядом ядра
![]() і одним електроном (однократно іонізований
гелій
і одним електроном (однократно іонізований
гелій
![]() ,
або двократно іонізований літій
,
або двократно іонізований літій
![]() ).
Іншими прикладами воднеподібних систем
є атоми з одним, досить слабо пов’язаним
валентним електроном, тоді як решта
електронів утворюють з ядром сильно
зв’язану систему (так званий кор,
серцевину атому із повним зарядом
).
Іншими прикладами воднеподібних систем
є атоми з одним, досить слабо пов’язаним
валентним електроном, тоді як решта
електронів утворюють з ядром сильно
зв’язану систему (так званий кор,
серцевину атому із повним зарядом
![]() ).
Отже, з’являється додатковий множник
).
Отже, з’являється додатковий множник
![]() :
:
|
|
(5.1.13) |
але самі спектри поглинання таких систем являють собою дискретні лінії, упорядковані в серії.
Пояснення серіальних спектральних закономірностей, як якісне, так і кількісне, було сильним аргументом на користь квантових теорій атому водню та воднеподібних систем.
|
Факультет машинобудування |
|
|
|
Лектор Дон Н.Л. |
|
стор.
|

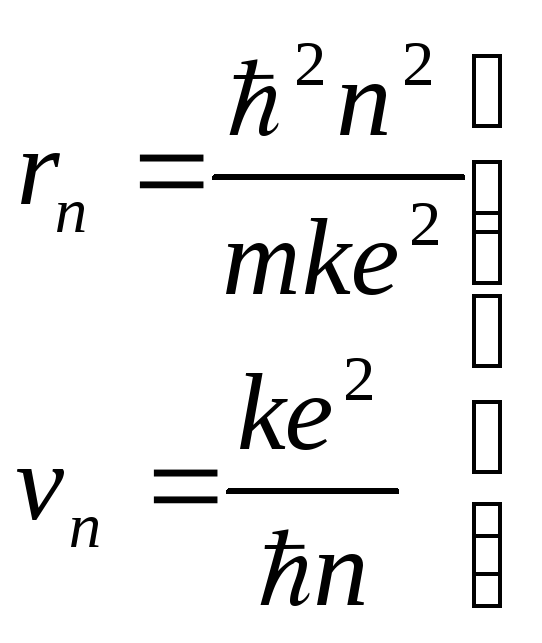 ;
;