
- •Київ кнуБіА пробірочний практикум
- •Якісний аналіз органічних речовин
- •Лабораторна робота № 1 якісні реакції органічних речовин
- •Дослід і. Виявлення карбону й гідрогену
- •Дослід 2. Виявлення нітрогену за реакцією лассеня
- •Дослід 3. Виявлення сульфуру
- •Дослід 4. Виявлення галогенів
- •Вуглеводні
- •Насичені вуглеводні
- •Лабораторна робота № 2
- •Дослід 2. Взаємодія алканів із бромною водою і розчином калій перманганату
- •Дослід 3. Добування етилену і вивчення його властивостей
- •Дослід 7. Добування ацетилену з карбіду кальцію та вивчення його властивостей
- •Дослід 11. Добування ацетиленіду аргентуму та ацетиленіду купруму
- •Ароматичні вуглеводні ( арени )
- •Лабораторна робота № 3 добування й властивості ароматичних вуглеводнів
- •Дослід 1. Добування бензену з бензоату натрію
- •Дослід 2. Взаємодія бензену із бромом
- •Дослід 3. Взаємодія гомологів бензену із бромом
- •З розчином калій перманганату
- •Дослід 6. Окислення гомологів бензену
- •Дослід 7. Нітрування бензену
- •Дослід 9. Сульфування фенолу
- •Дослід11. Окислення фенолу
- •Дослід12. Сублімація нафталену
- •Дослід 13. Нітрування нафталену
- •Дослід 14. Бромування нафталену
- •Галогенопохідні вуглеводнів
- •Лабораторна робота № 4 добування й властивості галогенопохідних
- •Дослід 1. Добування хлористого етилу
- •Дослід 2. Синтез брометану
- •Дослід 3. Добування йодоформу зi спирту
- •Дослід 6. Порівняння рухливості атомів галогену у бензеновому кільці та у боковому ланцюзі
- •Оксигенвмісні сполуки та їх похідні.
- •Одноатомні спирти
- •Лабораторна робота № 5 хімічні властивості одноатомних спиртів
- •Дослід 2. Виділення тепла під час розчинення етилового спирту у воді
- •Дослід 3. Горючість спиртів
- •Дослід 4. Виявлення води в спирті
- •Дослід 5. Висолювання етилового спирту
- •Дослід 6. Утворення алкоголятів натрію та їх гідроліз
- •Дослід 7. Окислення етилового спирту калій перманганатом
- •Дослід 8. Окислення спиртів оксидом купруму (II)
- •Дослід 9. Добування ectepib
- •Дослід 10. Виявлення сивушного масла у спирті
- •Дослід 11. Реакція на ненасичені одноатомні спирти
- •Дослід 12. Взаємодія етиленгліколю з натрієм
- •Дослід 13. Утворення гліколяту і гліцерату купруму
- •Дослід 14. Дегідратація гліцерину
- •Дослід 15. Розчинність фенолу у воді та його кислотні властивості
- •Дослід 16. Добування феноляту натрію
- •А л ь д e гіди та k e t o н и
- •Лабораторна робота № 6
- •Дослід 4. Реакція срібного дзеркала
- •Дослід 5. Реакція відновлення альдегідами гідроксиду купруму (II)
- •Дослід 6. Реакція відновлення альдегідами реактиву фелінга
- •Дослід 8. Взаємодія альдегідів із лугом
- •Дослід 13. Реакція канніццаро
- •Дослід 14. Окислювальні властивості хінону
- •Карбонові кислоти та їх похідні одноосновні карбонові кислоти. Жири
- •Лабораторна робота № 7
- •Карбонових кислот і жирів
- •Дослід 1. Розчинність карбонових кислот
- •Дослід 2. Виявлення карбонових кислот за допомогою індикаторів
- •Дослід 3. Утворення солей карбонових кислот
- •Дослід 4. Гідроліз солей карбонових кислот
- •Дослід 7. Відновлення амоніачного
- •Дослід 13. Взаємодія олеїнової кислоти із бромом
- •Дослід 15. Акролеїнова проба на жири
- •Дослід 16 визначення ненасиченост1 жиру
- •Дослід 18. Розчинність жирів
- •Дослід 20. Декарбоксилування малонової кислоти
- •Дослід 21. Гідроліз аспірину
- •Нітрогенobmichi органічні сполуки hitpo- і аміносполуки жирного ряду
- •Лабораторна робота № 8. Хімічні властивості hitpo- та аміносполук жирного та ароматичного ряду
- •Дослід 1. Кислотні властивості нітрометану
- •Дослід 7. Взаємодія амінів із солями феруму й купруму
- •Дослід 8. Реакція первинних аміносполук з нітритною кислотою
- •Дослід 9. Взаємодія аніліну з мінеральними кислотами
- •Дослід 12. Реакція аніліну із хлорним вапном
- •Дослід 16. Реакція діазотування
- •Амінокислоти і білкові речовини
- •Лабораторна робота №9 хімічні властивості амінокислот і білків
- •Дослід 2. Утворення комплексної солі купруму амінооцтової кислоти
- •Дослід 6. Висолювання білків
- •Дослід 7. Кольорові реакції на білки
- •Вуглеводи моносахариди (монози)
- •Полісахариди (поліози, несахароподібні вуглеводи)
- •Лабораторна робота № 10 хімічні властивості моносахаридів, дисахаридів та полісахаридів
- •Дослід 1. Якісна реакція на вуглеводи 3 α-нафтолом (реакція Моліша)
- •Дослід 2. Окислення моноз оксидом аргентуму (реакція срібного дзеркала)
- •Дослід 3. Окислення глюкози реактивом фелінга
- •Дослід 5. Реакція селіванова на кетогексози
- •Дослід 6. Реакція на наявність гідроксильних груп у дисахаридах
- •Дослід 7. Відношення дисахаридів до фелінгової рідини
- •Дослід 8. Відношення дисахаридів до амоніачного розчину оксиду аргентуму
- •Дослід 9. Гідроліз (інверсія) сахарози
- •Дослід 10. Якісна реакція на сахарозу
- •Дослід 12. Виявлення крохмалю в картоплі та зерні
- •Дослід 13. Розчинення клітковини у купрум-амоніачному розчині (реактив Швейцера)
- •Дослід 14. Розчинення клітковини в сульфатній кислоті
- •Полімери. Високомолекулярні сполуки
- •Лабораторна робота № 11
- •Дослід 1. Добування полібутилметакрилату
- •Лабораторна робота № 12
Дослід 5. Реакція відновлення альдегідами гідроксиду купруму (II)
У пробірку наливають 0,5 мл формаліну або оцтового альдегіду 3–4 мл 10 %-ного розчину гідроксиду натрію і добавляють краплями 2 %-ний розчину сульфату купруму до утворення каламуті. Верхню частину вмісту пробірки нагрівають. З'являється осад оксиду купруму (II) жовтого кольору, що переходить у червоний.
Мурашиний альдегід на відміну, від інших альдегідів, відновлює оксид купруму до "мідного дзеркала".
Дослід 6. Реакція відновлення альдегідами реактиву фелінга
У пробірку наливають 3–4 мл свіжо приготовленого реактиву Фелінга і добавляють 0,5– 1,0 мл формаліну або оцтового альдегіду. Реакційну суміш нагрівають. Спочатку розчин забарвлюється в зелений колір, потім у жовтий і, нарешті, випадає оксид купруму (II) червоного кольору:
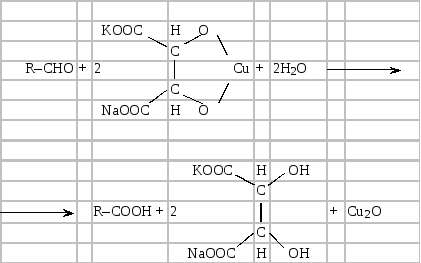
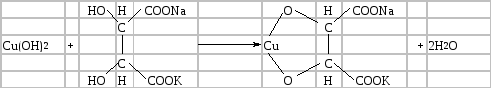
Добування фелінгової рідини: розчин Фелінга І – розчин мідного купоросу; розчин Фелінга II – лужний розчин сегнетової солі. Щоб добути фелінгову рідину, беруть у пробірку 5–6 мл розчину Фелінга І і стільки ж розчину Фелінга ІІ. При цьому відбуваються такі реакції:
CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2;
Дослід 8. Взаємодія альдегідів із лугом
До 3–4 мл 10-20 %-ного розчину гідроксиду натрію добавляють 0,5–1,0 мл формаліну, оцтового або ізовалер'янового альдегіду, і реакційну суміш нагрівають. У пробірках з оцтовим чи ізовалер'яновим альдегідом відбувається осмолення, рідина жовтіє, буріє і через деякий час утворюється забарвлена альдегідна смола. Мурашиний альдегід у цих умовах смолу не утворює.
Дослід 9. УТВОРЕННЯ АЛЬДЕГІДАМИ
Й КЕТОНАМИ ГІДРОСУЛЬФІТНИХ СПОЛУК
У пробірку до 2–3 мл насиченого розчину гідросульфіту натрію добавляють рівний об'єм формаліну, оцтового або ізовалер'янового альдегіду, або ацетону й суміш енергійно збовтують. Пробірку охолоджують і труть скляною паличкою по стінках пробірки. Випадає кристалічний осад гідросульфітної сполуки.
Дослід 11. ДОБУВАННЯ Й РОЗКЛАД
ГЕКСАМЕТИЛЕНТЕТРАМІНУ (УРОТРОПІНУ)
У фарфоровій чашці або тиглі змішують 5 мл 10 %-ного формаліну з 10–20 мл розчину амоніаку, і випарюють суміш на водяній бані або азбестовій сітці у витяжній шафі. Утворюються білі кристали гексаметилентетраміну.
Уперше таким методом гексаметилентетрамін був синтезований O.M. Бутлеровим у 1859 р.
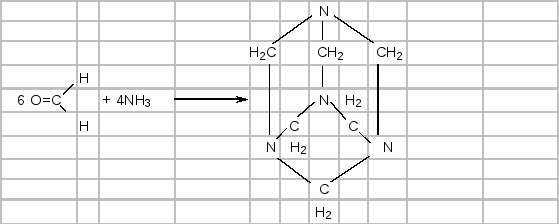
Отриманий продукт розчиняють у воді, підкислюють 1 %-ним розчином сульфатної кислоти і нагрівають. Виділяється формальдегід із характерним різким запахом:
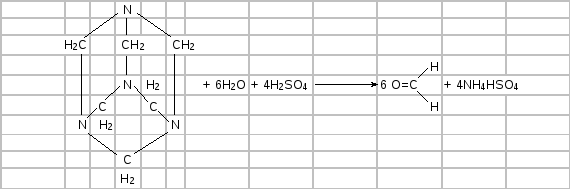 Гексаметилентетрамін
під назвою уротропін широко застосовується
в медицині.
Гексаметилентетрамін
під назвою уротропін широко застосовується
в медицині.
Дослід 12. ОКИСЛЕННЯ БЕНЗЕНОВОГО АЛЬДЕГІДУ КИСНЕМ ПОВІТРЯ
Кілька крапель бензенового альдегіду наливають на годинникове скло тонким шаром по всій поверхні і залишають на повітрі. Через деякий час спостерігають перехід рідкого безненового альдегіду в кристалічну бензенову кислоту завдяки реакції самоокислення (аутооксидації) альдегіду киснем повітря. Реакція проходить з утворенням проміжного продукту – надбензенової кислоти, що окислює другу молекулу бензенового альдегіду до відповідної кислоти.
Кристалічну масу збирають у пробірку, розчиняють у гарячій воді і випробовують розчин лакмусовим папірцем. Зміна кольору лакмусу на червоний засвідчує наявність кислоти.
