
- •Введение
- •Глава 1. Состояние проблемы очистки фильтрационных вод
- •1.1. Теоретические основы биодеструкции тбо и условия образования фильтрационных вод
- •Качество фильтрационных вод на различных фазах деградации тбо
- •1.2. Количественная оценка образования фильтрационных вод полигонов тбо
- •1.3. Методы очистки фильтрационных вод полигонов тбо
- •1.3.1. Биохимическая очистка фильтрационных вод
- •Декарбоксилирование Восстановительное
- •1.3.2. Физико-химические методы очистки фильтрационных вод и перспективы их применения
- •Электрохимический метод.
- •1.4. Состояние проблемы очистки фильтрационных вод г. Кунгура
- •Глава 2. Экспериментальная часть
- •2.1. Выбор методов очистки фильтрационных вод полигонов тбо в постэксплуатационный период
- •Концентрации загрязняющих веществ в фильтрационных водах типичных полигонов тбо.
- •2.1.1. Выбор сорбционных материалов для исследования и характеристика их адсорбционных свойств
- •2.1.2. Выбор модельных растворов и их приготовление. Определение концентрации железа и меди в растворе
- •2.2. Методики проведения экспериментов
- •2.3. Исследование очистки фильтрационных вод и модельных растворов от ионных примесей
- •2.3.1.Исследование ионообменной очистки сточных вод от ионов металлов
- •2.3.2. Исследование очистки воды от гуматов металлов
- •Сорбционные и ионообменные характеристики материалов
- •2.3.3. Исследование адсорбции гуминовых соединений
- •2.4. Исследование биосорбционной очистки фильтрационных вод и модельных растворов
- •Выводы глава 3. Технологическая часть
- •3.1. Разработка технологической схемы очистки фильтрационных вод
- •3.2. Расчет основных технологических сооружений.
- •Глава 4. Оценка экономической целесообразности внедрения разработанной системы очистки фильтрационных вод.
- •Глава 5. Охрана труда в химической лаборатории
2.2. Методики проведения экспериментов
Исследования по очистке фильтрационных вод полигонов ТБО проводили на модельных и реальных растворах фильтрационных вод.
Эксперименты осуществляли в статических и динамических условиях.
При проведении статических экспериментов определяли оптимальную дозу сорбента, необходимую для эффективной очистки. Для этого дозу сорбента в экспериментах варьировали в широких пределах 5-25 г/дм3. Концентрация исходных растворов составляла 100-500 мг/дм3.
Сорбционную емкость материалов определяли по формуле:
![]()
где: А – статическая сорбционная емкость, мг О2/г;
Со, Ср – исходная и равновесная концентрация фильтрационных вод по ХПК, мг О2/дм3;
V – объем исследуемой воды, л;
m – доза сорбента, г.
На основании полученных данных строили изотермы адсорбции и ионного обмена.
Динамические испытания проводили в сорбционных колонках диаметром 15 мм с высотой слоя сорбента 25 см. Анализируемый раствор пропускали через слой сорбента со скоростью 250 мл/час или м/час до полного проскока.
По полученным данным строили выходные кривые сорбции.
Эффективность очистки контролировали по цветности и содержанию ионов металлов в очищенной воде.
2.3. Исследование очистки фильтрационных вод и модельных растворов от ионных примесей
2.3.1.Исследование ионообменной очистки сточных вод от ионов металлов
На выбранных материалах исследовалась возможность извлечения ионов Fe3+ и Сu2+ из модельных растворов, содержащих соли этих металлов.
Концентрация ионов металлов в модельных растворах, содержащих хлориды металлов, составляла 500 мг/л.
В результате экспериментов, проводимых в статических условиях, были построены изотермы ионоого обмена и определены ионообменные емкости материалов при равновесной концентрации 100 и 50 мг/л, которые представлены в таблице 9.
Таблица 9.
Ионообменная емкость материалов
|
№ |
Материал |
Ионообменная емкость, мг/л | |
|
Ионы железа (III) |
Ионы меди (II) | ||
|
1 2 3 4 |
Диатомит Шлак Сорбент–Н Отход АУ |
5700-5500 4000-4500 500-600 400-500 |
6000-5800 4500-5000 550-650 550-600 |
Исходные материалы обладали разной плотностью и для более корректного сравнения их активности ионообменные емкости рассчитывали в мг/л сорбента.
Как видно из приведенных данных, наибольшей ионообменной способностью при извлечении гидратированных ионов металлов обладает диатомит.
2.3.2. Исследование очистки воды от гуматов металлов
Опыты проводили в статических и динамических условиях.
В статических экспериментах определяли изотермы ионного обмена. Степень извлечения гуматов металлов контролировали по величине цветности (оЦв) и концентрации ионов металлов в растворе. Исходная цветность составляла 250 оЦв, концентрация ионов Fe3+ или Cu (II) – 200 мг/л.
Полученные изотермы ионного обмена на исследуемых материалах представлены на рисунке 4 и 5.
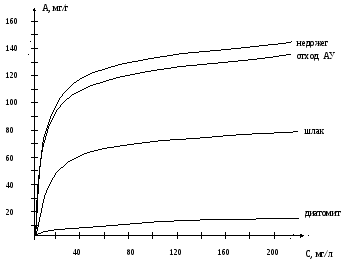
Рис.4.

Рис.5. Изотерма ионного обмена на исследуемых материалах
В таблице 10 представлена максимальная ионообменная емкость исследуемых сорбентов и осветляющия спосбность.
Результаты показывают, что наибольшей сорбционной и осветляющей способностью обладают недожог, шлак, отход АУ.
Диатомит, являясь узко микропористым материалом, практически не способен извлекать крупные молекулы гуматов.
Недожог (сорбент -Н) и отход АУ, характеризующиеся развитой удельной поверхностью и высокой порозностью, являются эффективными и дешевыми материалами для извлечения высокомолекулярных соединений из фильтрационных вод.
Достаточно высокая емкость шлака на единицу веса объясняется более высокой насыпной плотностью этого материала по сравнению с сорбентом-Н (dшл.=750 г/дм3, dсорб-Н =240-250 г/дм3).
Таблица 10.
