
- •Процессы при кристаллизации из раствора металлов и сплавов
- •Несамопроизвольная кристаллизация
- •Аморфное состояние металлов
- •Форма кристаллов и строение слитков
- •1, 2 И 3 - оси соответственно первого, второго и
- •Методы построения диаграмм состояния
- •Основные равновесные диаграммы состояния двойных сплавов
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ
ФЕДЕРАЦИИ
ИНЖЕНЕРНО ТЕХНОЛОГИЧЕСКАЯ АКАДЕМИЯ
ЮЖНОГО ФЕДЕРАЛЬНОГО УНИВЕРСИТЕТА
В Г. ТАГАНРОГЕ
Реферат на тему:
Процессы при кристаллизации из раствора металлов и сплавов
Выполнил:
Студент группы Э-62
Тимощенко Д.В.
Проверил:
Джуплин В.Н.
Таганрог 2013
Кристаллизация металлов Переход металла из жидкого или парообразного состояния в твердое с образованием кристаллической структуры называется первичной кристаллизацией. Образование новых кристаллов в твердом кристаллическом веществе называется вторичной кристаллизацией. Процесс кристаллизации состоит из двух одновременно идущих процессов - зарождения и роста кристаллов. Кристаллы могут зарождаться самопроизвольно (самопроизвольная кристаллизация) или расти на имеющихся готовых центрах кристаллизации (несамопроизвольная кристаллизация). Самопроизвольная кристаллизация
Самопроизвольная
кристаллизация обусловлена стремлением
вещества иметь более устойчивое
состояние, характеризуемое уменьшением
термодинамического потенциала G. С
повышением температуры термодинамический
потенциал вещества как в твердом, так
и в жидком состоянии уменьшается, что
показано на рисунке.
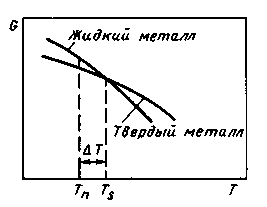 Изменение
термодинамического потенциала в
зависимости от температуры для металла
в твердом и жидком состояниях
Температура,
при которой термодинамические
потенциалы вещества в твердом и
жидком состояниях равны, называется
равновесной температурой кристаллизации.
Кристаллизация происходит в том
случае, если термодинамический
потенциал вещества в твердом состоянии
будет меньше термодинамического
потенциала вещества в жидком состоянии,
т. е. при переохлаждении жидкого металла
до температур ниже равновесной. Плавление
- процесс, обратный кристаллизации,
происходит при температуре выше
равновесной, т. е. при перегреве. Разница
между реальными температурами
плавления и кристаллизации называется
температурным гистерезисом.
Поскольку
жидкий металл с присущим ему ближним
порядком в расположении атомов
обладает большей внутренней энергией,
чем твердый со структурой дальнего
порядка, при кристаллизации выделяется
теплота. Между теплотой и температурой
кристаллизации Тк существует
определенная связь. Так как при равновесной
температуре кристаллизации термодинамические
потенциалы в жидком и твердом
состояниях равны, то
Изменение
термодинамического потенциала в
зависимости от температуры для металла
в твердом и жидком состояниях
Температура,
при которой термодинамические
потенциалы вещества в твердом и
жидком состояниях равны, называется
равновесной температурой кристаллизации.
Кристаллизация происходит в том
случае, если термодинамический
потенциал вещества в твердом состоянии
будет меньше термодинамического
потенциала вещества в жидком состоянии,
т. е. при переохлаждении жидкого металла
до температур ниже равновесной. Плавление
- процесс, обратный кристаллизации,
происходит при температуре выше
равновесной, т. е. при перегреве. Разница
между реальными температурами
плавления и кристаллизации называется
температурным гистерезисом.
Поскольку
жидкий металл с присущим ему ближним
порядком в расположении атомов
обладает большей внутренней энергией,
чем твердый со структурой дальнего
порядка, при кристаллизации выделяется
теплота. Между теплотой и температурой
кристаллизации Тк существует
определенная связь. Так как при равновесной
температуре кристаллизации термодинамические
потенциалы в жидком и твердом
состояниях равны, то
![]()
![]() =>
=> ![]() =>
Параметр
=>
Параметр
 S
= Q/TK характеризует
упорядоченность в расположении атомов
при кристаллизации. В зависимости от
сил межатомной связи теплота кристаллизации
для различных металлов изменяется от
2500 Дж/моль (Na, К и др.) до 20000 Дж/моль (W и
др.).
Когда кристаллизуется
чистый элемент, отвод теплоты,
происходящий вследствие охлаждения,
компенсируется теплотой кристаллизации.
В связи с этим на кривой охлаждения,
изображаемой в координатах
температура-время, процессу кристаллизации
соответствует горизонтальный
участок:
S
= Q/TK характеризует
упорядоченность в расположении атомов
при кристаллизации. В зависимости от
сил межатомной связи теплота кристаллизации
для различных металлов изменяется от
2500 Дж/моль (Na, К и др.) до 20000 Дж/моль (W и
др.).
Когда кристаллизуется
чистый элемент, отвод теплоты,
происходящий вследствие охлаждения,
компенсируется теплотой кристаллизации.
В связи с этим на кривой охлаждения,
изображаемой в координатах
температура-время, процессу кристаллизации
соответствует горизонтальный
участок:
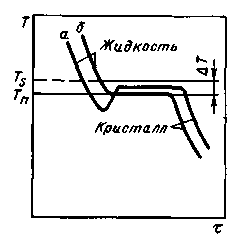 Кривые
охлаждения металла
При
большом объеме жидкого металла
выделяющаяся при кристаллизации
теплота повышает температуру практически
до равновесной (кривая а);
при малом объеме металла выделяющейся
теплоты недостаточно, вследствие чего
кристаллизация происходит с переохлаждением
по сравнению с равновесной температурой
(кривая б).
Разница
между равновесной (Ts)
и реальной (Тn)
температурой кристаллизации называется
степенью переохлаждения ?T. Степень
переохлаждения зависит от природы
металла. Она увеличивается с повышением
чистоты металла и с ростом скорости
охлаждения. Обычная степень
переохлаждения металлов при кристаллизации
в производственных условиях колеблется
от 10 до 30 °С; при больших скоростях
охлаждения она может достигать сотен
градусов.
Степень перегрева при
плавлении металлов, как правило, не
превышает нескольких градусов.
В
жидком состоянии атомы вещества
вследствие теплового движения
перемещаются беспорядочно. В то же
время в жидкости имеются группировки
атомов небольшого объема, в пределах
которых расположение атомов вещества
во многом аналогично их расположению
в решетке кристалла. Эти группировки
неустойчивы, они рассасываются и вновь
появляются в жидкости. При переохлаждении
жидкости некоторые из них, наиболее
крупные, становятся устойчивыми и
способными к росту. Эти устойчивые
группировки атомов называют центрами
кристаллизации (зародышами). Образованию
зародышей способствуют флуктуации
энергии, т. е. отклонения энергии
группировок атомов в отдельных зонах
жидкого металла от некоторого среднего
значения. Размер образовавшегося
зародыша зависит от величины зоны
флуктуации.
Появление центров
изменяет термодинамический потенциал
системы
Кривые
охлаждения металла
При
большом объеме жидкого металла
выделяющаяся при кристаллизации
теплота повышает температуру практически
до равновесной (кривая а);
при малом объеме металла выделяющейся
теплоты недостаточно, вследствие чего
кристаллизация происходит с переохлаждением
по сравнению с равновесной температурой
(кривая б).
Разница
между равновесной (Ts)
и реальной (Тn)
температурой кристаллизации называется
степенью переохлаждения ?T. Степень
переохлаждения зависит от природы
металла. Она увеличивается с повышением
чистоты металла и с ростом скорости
охлаждения. Обычная степень
переохлаждения металлов при кристаллизации
в производственных условиях колеблется
от 10 до 30 °С; при больших скоростях
охлаждения она может достигать сотен
градусов.
Степень перегрева при
плавлении металлов, как правило, не
превышает нескольких градусов.
В
жидком состоянии атомы вещества
вследствие теплового движения
перемещаются беспорядочно. В то же
время в жидкости имеются группировки
атомов небольшого объема, в пределах
которых расположение атомов вещества
во многом аналогично их расположению
в решетке кристалла. Эти группировки
неустойчивы, они рассасываются и вновь
появляются в жидкости. При переохлаждении
жидкости некоторые из них, наиболее
крупные, становятся устойчивыми и
способными к росту. Эти устойчивые
группировки атомов называют центрами
кристаллизации (зародышами). Образованию
зародышей способствуют флуктуации
энергии, т. е. отклонения энергии
группировок атомов в отдельных зонах
жидкого металла от некоторого среднего
значения. Размер образовавшегося
зародыша зависит от величины зоны
флуктуации.
Появление центров
изменяет термодинамический потенциал
системы
 Gобщ. С
одной стороны, при переходе жидкости в
кристаллическое состояние термодинамический
потенциал уменьшается на V
Gобщ. С
одной стороны, при переходе жидкости в
кристаллическое состояние термодинамический
потенциал уменьшается на V Gv (G1),
с другой стороны, он увеличивается
вследствие появления поверхности
раздела между жидкостью и кристаллическим
зародышем на величину, равную
S
Gv (G1),
с другой стороны, он увеличивается
вследствие появления поверхности
раздела между жидкостью и кристаллическим
зародышем на величину, равную
S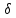 (G2):
(G2):
 Gобщ. =
- V
Gобщ. =
- V Gv +
S
Gv +
S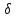
 где
V-объем зародыша; S-поверхность
зародыша; -удельное поверхностное
натяжение на границе кристалл-жидкость;
где
V-объем зародыша; S-поверхность
зародыша; -удельное поверхностное
натяжение на границе кристалл-жидкость;
 Gv-удельная
разность термодинамических потенциалов
при переходе жидкости в кристаллическое
состояние.
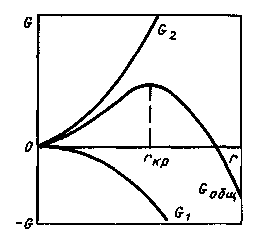
Изменение
термодинамического потенциала при
образовании зародышей в зависимости
от их размера
Если
принять, что зародыш имеет форму куба
с ребром А, то общее изменение
термодинамического потенциала
Gv-удельная
разность термодинамических потенциалов
при переходе жидкости в кристаллическое
состояние.
Изменение
термодинамического потенциала при
образовании зародышей в зависимости
от их размера
Если
принять, что зародыш имеет форму куба
с ребром А, то общее изменение
термодинамического потенциала
 Gобщ. =
A3
Gобщ. =
A3 Gv +
6A2
Gv +
6A2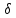 Отсюда
следует, что графическая зависимость
изменения термодинамического
потенциала от размера зародыша имеет
максимум при некотором значении А,
названном критическим. Зародыши с
размером больше критического вызывают
уменьшение
Отсюда
следует, что графическая зависимость
изменения термодинамического
потенциала от размера зародыша имеет
максимум при некотором значении А,
названном критическим. Зародыши с
размером больше критического вызывают
уменьшение
 Gобщ. и
поэтому являются устойчивыми,
способными к росту. Зародыши, имеющие
размер меньше критического, нестабильны
и растворяются в жидкости, поскольку
вызывают увеличение
Gобщ. и
поэтому являются устойчивыми,
способными к росту. Зародыши, имеющие
размер меньше критического, нестабильны
и растворяются в жидкости, поскольку
вызывают увеличение
 Gобщ.
Gобщ.
![]()
![]()
![]()
![]() =>
=> ![]() =>
Скорость
процесса и окончательный размер
кристаллов при затвердевании определяются
соотношением скоростей роста кристаллов
и образования центров кристаллизации.
Скорость образования зародышей
измеряется числом зародышей, образующихся
в единицу времени в единице объема;
скорость роста - увеличением линейного
размера растущего кристалла в единицу
времени. Оба процесса связаны с
перемещениями атомов и зависят от
температуры. Графическая зависимость
скорости образования зародышей и
скорости их роста от степени переохлаждения
представлена на рисунке.
=>
Скорость
процесса и окончательный размер
кристаллов при затвердевании определяются
соотношением скоростей роста кристаллов
и образования центров кристаллизации.
Скорость образования зародышей
измеряется числом зародышей, образующихся
в единицу времени в единице объема;
скорость роста - увеличением линейного
размера растущего кристалла в единицу
времени. Оба процесса связаны с
перемещениями атомов и зависят от
температуры. Графическая зависимость
скорости образования зародышей и
скорости их роста от степени переохлаждения
представлена на рисунке.
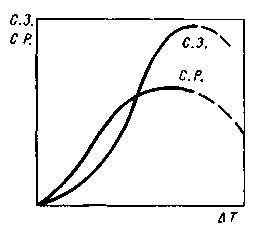 Изменение
скорости образования зародышей (с. з.) и
скорости роста кристаллов (с. р.) в
зависимости от степени переохлаждения
Для
металлов, которые в обычных условиях
кристаллизации не склонны к большим
переохлаждениям, как правило,
характерны восходящие ветви кривых.
Это значит, что при равновесной
температуре, когда степень переохлаждения
равна нулю, скорость образования
зародышей и скорость роста также равны
нулю, т. е. кристаллизации не происходит.
При небольших степенях переохлаждения,
когда велик зародыш критического
размера, а скорость образования
зародышей мала, при затвердевании
формируется крупнокристаллическая
структура. Небольшие степени переохлаждения
достигаются при заливке жидкого
металла в форму с низкой теплопроводностью
(земляная, шамотовая) или в подогретую
металлическую форму. Увеличение
переохлаждения происходит при заливке
жидкого металла в холодные металлические
формы, а также при уменьшении толщины
стенок отливки. Поскольку при этом
скорость образования зародышей
увеличивается более интенсивно, чем
скорость их роста, получаются более
мелкие кристаллы.
Изменение
скорости образования зародышей (с. з.) и
скорости роста кристаллов (с. р.) в
зависимости от степени переохлаждения
Для
металлов, которые в обычных условиях
кристаллизации не склонны к большим
переохлаждениям, как правило,
характерны восходящие ветви кривых.
Это значит, что при равновесной
температуре, когда степень переохлаждения
равна нулю, скорость образования
зародышей и скорость роста также равны
нулю, т. е. кристаллизации не происходит.
При небольших степенях переохлаждения,
когда велик зародыш критического
размера, а скорость образования
зародышей мала, при затвердевании
формируется крупнокристаллическая
структура. Небольшие степени переохлаждения
достигаются при заливке жидкого
металла в форму с низкой теплопроводностью
(земляная, шамотовая) или в подогретую
металлическую форму. Увеличение
переохлаждения происходит при заливке
жидкого металла в холодные металлические
формы, а также при уменьшении толщины
стенок отливки. Поскольку при этом
скорость образования зародышей
увеличивается более интенсивно, чем
скорость их роста, получаются более
мелкие кристаллы.
