
Физика - ответы на экзамен 1-29 / Идеальный газ
.docxИдеальный газ — газ, молекулы которого представляют собой материальные точки с ничтожно малыми объёмами и не обладают силами взаимодействия
Понятие об идеальном газе введено для упрощения изучения термодинамических процессов и получения более простых расчетных формул.
равнение состояния идеального газа (иногда уравнение Клапейронаили уравнение Клапейрона — Менделеева) — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:
![]()
где
-
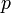 —
давление,
—
давление, -
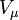 —
молярный
объём,
—
молярный
объём, -
 —
абсолютная
температура,
—
абсолютная
температура, -
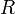 — универсальная
газовая постоянная.
— универсальная
газовая постоянная.
Так
как ![]() ,
где
,
где ![]() — количество
вещества,
а
— количество
вещества,
а ![]() ,
где
,
где ![]() —
масса,
—
масса, ![]() — молярная
масса,
уравнение состояния можно записать:
— молярная
масса,
уравнение состояния можно записать:
![]()
Эта форма записи носит имя уравнения (закона) Менделеева — Клапейрона.
Уравнение можно записать в виде:
![]()
![]()
1.
Изотермический процесс
:
объем данного количества газа при
постоянной температуре обратно
пропорционален его давлению (Закон
Бойля-Мариотта)
2. Изобарный процесс: объем данного количества газа при постоянном давлении линейно зависит от температуры (Закон Гей-Люссака)
3. Изохорный процесс: давление данного количества газа при постоянном объеме линейно зависит от его температуры (Закон Шарля)
Абсолютная температура – температура по шкале Кельвина t=-273C - абсолютный нуль
