
Betekhtin
.pdfГлава 1
ЗЕМНАЯ КОРА И ОСОБЕННОСТИ ЕЕ СОСТАВА
Строение земного шара. Главным объектом геологических, в том чис ле и минералогических исследований является земная кора, под которой подразумевается самая верхняя оболочка земного шара, доступная непо средственному наблюдению.
Наши фактические знания о строении и химическом составе земной коры основываются почти исключительно на наблюдениях над самыми поверхностными частями нашей планеты.
Горообразующие процессы, совершавшиеся в различные геологиче ские эпохи и приводившие к образованию высоких горных хребтов, под няли из глубины самые различные породы, не образующиеся вблизи по верхности Земли. Наиболее глубинные по происхождению горные породы из доступных прямому изучению — мантийные ксенолиты, об наруживаемые в трубках взрыва, — являются объектом пристального внимания исследователей. Их изучение дает возможность, как показы вают геологические наблюдения и подсчеты, получить более или менее реальное представление о составе и строении земного шара только до глубины 100–150 км (радиус же его превышает 6300 км).
О строении и составе глубоких недр земного шара можно судить лишь на основании косвенных данных. Как показывает сопоставление плотно стей всего земного шара (5,527) и земной коры (2,7–2,8), внутренние ча сти нашей планеты должны обладать значительно большей плотностью, чем поверхностные. Различные данные (геофизические наблюдения, дан ные сравнения Земли с другими космическими телами, состав метеори тов и пр.) дают основания предполагать, что это обстоятельство обуслов лено не только увеличением с глубиной давления, но и изменением состава внутренних частей нашей планеты.
Согласно современным моделям, построенным на основании геофи зических данных, в строении Земли выделяется несколько концентри ческих оболочек (геосфер, рис. 3), различающихся по физическим свой ствам и составу (табл. 1).
Состав земной коры. Впервые состав твердой части земной коры
ввесовых процентах подсчитал американский исследователь Ф. Кларк
в1889 г. Большая работа по уточнению полученных цифр была проделана В. И. Вернадским, А. Е. Ферсманом, И. и В. Ноддаками, Г. Гевеши, В. М. Гольдшмидтом и А. П. Виноградовым. Последний подсчитал средний

32 |
|
Общая часть |
|
|||
|
|
|
|
|
|
Таблица 1 |
|
|
Характеристики геосфер Земли |
||||
|
|
|
|
|
|
|
|
|
Ин- |
Нижняя |
|
|
|
|
Оболочка |
грани- |
|
Плотность |
Компонентный состав |
|
|
декс |
|
||||
|
|
ца, км |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Кора |
A |
10–30 |
|
2,80–2,85 |
SiO2, Al2O3,FeO, CaO, |
|
|
|
|
|
|
MgO, Na2O, K2О |
|
Верхняя ман- |
B |
350–400 |
|
2,9–3,5 |
SiO2, MgO, FeO, CaO, |
|
тия |
|
|
|
|
Al2O3 |
|
Переходная |
C |
770 |
|
3,8–4,2 |
SiO2, MgO, FeO, CaO, |
|
зона |
|
|
|
|
Al2O3 |
|
Нижняя ман- |
D |
2875 |
|
4,5–5,6 |
SiO2, MgO, FeO, Fe, MgS, |
|
тия |
|
|
|
|
FeS |
|
|
|
|
|
|
|
|
Внешнее ядро |
E |
4711 |
|
9,8–12,2 |
FeO, Fe, FeS, Si, Ni, H, C |
|
|
|
|
|
|
|
|
Переходная |
F |
5160 |
|
12,2–12,5 |
Fe, FeS, Ni, H, C |
|
зона |
|
|
|
|
|
|
|
|
|
|
|
|
|
Внутреннее |
G |
6371 |
|
12,7–14,0 |
Fe, Ni, H, C |
|
ядро |
|
|
|
|
|
|
|
|
|
|
|
|
химический состав лишь литосфе |
|
|
||||
ры (без учета гидросферы и атмо |
|
|
||||
сферы). |
|
|
|
|
|
|
|
По предложению акад. Ферс |
|
|
|||
мана средние цифры содержаний |
|
|
||||
отдельных элементов земной коры |
|
|
||||
стали называть «числами Кларка», |
|
|
||||
или просто кларками. Он же пред |
|
|
||||
ложил выражать эти величины не |
|
|
||||
только в весовых процентах, но и |
|
|
||||
в атомных. |
|
|
|
|
|
|
|
Из более чем ста химических |
|
|
|||
элементов, приведенных в перио |
|
|
||||
дической таблице элементов Мен |
Рис. 3. Схема внутреннего строения Земли |
|||||
делеева (табл. 2), лишь немногие |
(мощность земной коры отражена |
|||||
пользуются широким распростра |
|
вне масштаба) |
||||
нением в земной коре. Такие эле |
|
|
||||
менты в таблице располагаются преимущественно в верхней ее части, т. е. относятся к числу элементов с малыми порядковыми номерами.
Наиболее распространенными элементами являются: О, Si, Al, Fe, Ca, Na, К, Mg, Ti, H и С. На долю всех остальных элементов, встречающихся

Глава 1. Земная кора и особенности ее состава |
33 |
вземной коре, приходится всего лишь несколько десятых процента (по весу). Подавляющее большинство этих элементов в земной коре присут ствует почти исключительно в виде химических соединений. К числу элементов, встречающихся в самородном виде, относятся очень немно гие. Те и другие возникают в результате химических реакций, которые протекают в земной коре при различных геологических процессах, при водящих к образованию самых разнообразных па составу массивов гор ных пород и месторождений полезных ископаемых.
Если главнейшие элементы расположить в порядке их процентного (весового) содержания в земной коре на группы по декадам1, то получит ся такая картина (табл. 3).
Из таблицы 3 видно, что подавляющая масса минералов земной коры должна представлять соединения элементов первых двух декад, на долю которых в весовом выражении приходится основная масса. В самом деле,
вземной коре чрезвычайно широко распространены кислородные соеди нения кремния, алюминия, железа, а также щелочноземельных и щелоч ных металлов — кальция, магния, натрия и калия. К их числу относятся главным образом окислы и кислородные соли (преимущественно сили каты, алюмосиликаты, карбонаты, сульфаты и др.), входящие в состав различных горных пород, слагающих земную кору.
Кларки тяжелых металлов, играющих большую роль в промышлен ности, в подавляющем большинстве выражаются ничтожными величи нами и попадают в последние столбцы элементов, разбитых на декады по степени распространения (табл. 4).
Некоторые особенности распределения тяжелых металлов в земной коре. Многие из указанных редких в земной коре элементов под влиянием совершающихся в природе геохимических процессов нередко образуют исключительно богатые скопления минерального вещества, носящие на звание рудных месторождений. Если бы не существовало процессов, при водящих к образованию таких месторождений, которые имело бы смысл разрабатывать с целью извлечения ценных для промышленности метал лов, то можно с уверенностью сказать, что не было бы и столь мощного развития техники и культуры, какое наблюдается в настоящее время.
Тогда многие металлы, извлеченные из пород в лабораторных услови ях, являлись бы исключительно дорогими. Весьма характерно, что кларки таких металлов, как ванадий, цезий, галлий и др., во много раз выше клар ков ртути, висмута, серебра, золота и др. Но, несмотря на их весьма ценные свойства, они не распространены в человеческом быту, так как их место рождения с промышленными концентрациями в природе крайне редки.
Природные соединения тяжелых металлов представляют собой в ос новном сравнительно простые соединения. Часть этих элементов (Fe, Mn,
1 От греческого слова дека — десять.

Таблица 2
Периодическая система элементов Д. И. Менделеева
S-элементы |
|
р-элементы |
|
d-элементы |
|
f-элементы |
|
||||
|
|
|
|
|
Группы элементов |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
Перио- |
ряды |
I |
II |
III |
IV |
V |
VI |
VII |
|
VIII |
|
ды |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
2 |
1 |
1 |
Водород |
|
|
|
|
|
|
|
|
Гелий |
Н |
|
|
|
|
|
|
|
|
He |
||
|
|
|
|
|
|
|
|
|
|
||
|
|
1,0079 |
|
|
|
|
|
|
|
|
4,0026 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
|
10 |
2 |
2 |
Литий |
Бериллий |
Бор |
Углерод |
Азот |
Кислород |
Фтор |
|
|
Неон |
Li |
Be |
B |
C |
N |
O |
F |
|
|
Ne |
||
|
|
|
|
||||||||
|
|
6,941 |
9,01218 |
10,81 |
12,011 |
14,0067 |
15,9994 |
18,9984 |
|
|
20,179 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
|
|
18 |
3 |
3 |
Натрий |
Магний |
Алюминий |
Кремний |
Фосфор |
Сера |
Хлор |
|
|
Аргон |
Na |
Mg |
Al |
Si |
P |
S |
Cl |
|
|
Ar |
||
|
|
22,98977 |
24,305 |
26,98154 |
28,0855 |
30,97376 |
32,06 |
35,453 |
|
|
39,948 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
19 |
20 |
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
4 |
4 |
Калий |
Кальций |
Скандий |
Титан |
Ванадий |
Хром |
Марганец |
Железо |
Кобальт |
Никель |
К |
Ca |
Sc |
Ti |
V |
Cr |
Mn |
Fe |
Co |
Ni |
||
|
|
39,0983 |
40,08 |
44,9559 |
47,88 |
50,9415 |
51,996 |
54,9380 |
55,847 |
58,9332 |
58,69 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
29 |
30 |
31 |
32 |
33 |
34 |
35 |
|
|
36 |
|
5 |
Медь |
Цинк |
Галлий |
Германий |
Мышьяк |
Селен |
Бром |
|
|
Криптон |
|
Cu |
Zn |
Ga |
Ge |
As |
Se |
Br |
|
|
Kr |
|
|
|
63,546 |
65,38 |
69,72 |
72,59 |
74,9216 |
78,96 |
79,904 |
|
|
83,80 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
37 |
38 |
39 |
40 |
41 |
42 |
43 |
44 |
45 |
46 |
5 |
6 |
Рубидий |
Стронций |
Иттрий |
Цирконий |
Ниобий |
Молибден |
Технеций |
Рутений |
Родий |
Палладий |
Rb |
Sr |
Y |
Zr |
Nb |
Mo |
Tc |
Ru |
Rh |
Pd |
||
|
|
85,4678 |
87,62 |
88,9059 |
91,22 |
92,9064 |
95,94 |
[98] |
101,07 |
102,9055 |
106,42 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
47 |
48 |
49 |
50 |
51 |
52 |
53 |
|
|
54 |
|
7 |
Серебро |
Кадмий |
Индий |
Олово |
Сурьма |
Теллур |
Иод |
|
|
Ксенон |
|
Ag |
Cd |
In |
Sn |
Sb |
Te |
I |
|
|
Xe |
|
|
|
|
|
||||||||
|
|
107,868 |
112,41 |
114,82 |
118,69 |
121,75 |
127,60 |
126,9045 |
|
|
131,2954 |
|
|
|
|
|
|
|
|
|
|
|
|

|
|
|
|
|
55 |
|
|
56 |
|
|
|
57* |
|
|
|
72 |
|
|
|
73 |
|
|
|
74 |
|
75 |
|
|
|
76 |
|
|
|
77 |
|
|
78 |
|
||||||
6 |
|
8 |
Цезий |
Барий |
|
|
|
Лантан |
|
|
Гафний |
|
Тантал |
|
Вольфрам |
Рений |
|
|
|
Осмий |
|
Иридий |
|
Платина |
|
|||||||||||||||||||
|
Cs |
Ba |
|
|
|
La |
|
|
Hf |
|
|
|
Ta |
|
|
W |
Re |
|
|
|
Os |
|
|
|
Ir |
|
|
Pt |
|
|||||||||||||||
|
|
|
|
|
132,9054 |
|
137,33 |
|
|
|
138,9055 |
|
178,49 |
|
180,9479 |
|
183,85 |
|
186,207 |
|
|
|
190,2 |
|
|
|
192,22 |
|
195,08 |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
79 |
|
|
|
80 |
|
|
|
81 |
|
82 |
|
|
|
83 |
|
84 |
|
|
85 |
|
|
|
|
|
|
|
86 |
|
|||||||||
|
|
|
9 |
|
|
|
Золото |
|
Ртуть |
|
Таллий |
Свинец |
|
|
|
Висмут |
|
|
|
Полоний |
Астат |
|
|
|
|
|
|
|
|
Радон |
|
|||||||||||||
|
|
|
|
|
|
Au |
|
|
Hg |
|
|
|
Tl |
|
|
Pb |
|
|
|
Bi |
|
|
|
Po |
|
At |
|
|
|
|
|
|
|
|
Rn |
|
||||||||
|
|
|
|
|
|
|
196,9665 |
|
200,59 |
|
204,383 |
|
207,2 |
|
208,9804 |
|
[209] |
|
[210] |
|
|
|
|
|
|
|
[222] |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
87 |
|
|
88 |
|
|
|
89** |
|
|
|
104 |
|
|
|
105 |
|
106 |
|
107 |
|
|
|
108 |
|
|
|
109 |
|
|
110 |
|
||||||||
7 |
|
10 |
Франций |
Радий |
|
|
|
Актиний |
Резерфордий |
|
Дубний |
|
Сиборгий |
Борий |
|
|
|
Хассий |
|
Майтнерий |
|
|
|
|
||||||||||||||||||||
|
Fr |
Ra |
|
|
|
Ac |
|
|
Rf |
|
|
|
Db |
|
|
Sg |
Bh |
|
|
|
Hs |
|
|
|
Mt |
|
|
Uun |
|
|||||||||||||||
|
|
|
|
|
[223] |
|
226,0254 |
|
|
227,0278 |
|
[261] |
|
|
|
[262] |
|
[263] |
|
[262] |
|
|
|
[265] |
|
|
|
[266] |
|
[?] |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
* Лантаноиды |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
58 |
59 Пра- |
|
|
60 |
|
61 Про- |
|
62 |
|
|
63 |
|
|
64 Гадо- |
|
65 |
|
|
|
66 Дис- |
|
67 |
|
68 |
69 |
|
|
70 Ит- |
|
71 Лю- |
|
||||||||||||
|
Церий |
зеодим |
|
|
Неодим |
|
метий |
|
Самарий |
|
Европий |
|
линий |
|
|
Тербий |
|
|
прозий |
|
Гольмий |
|
|
Эрбий |
|
Тулий |
|
тербий |
|
теций |
|
|||||||||||||
|
Ce |
Pr |
|
|
Nd |
|
Pm |
|
Sm |
|
|
Eu |
|
|
Gd |
|
|
Tb |
|
|
Dy |
|
Ho |
|
|
Er |
|
Tm |
|
Yb |
|
Lu |
|
|||||||||||
|
140,12 |
140,9077 |
|
|
144,24 |
|
[145] |
|
150,36 |
|
151,96 |
157,25 |
|
|
158,9254 |
|
|
162,50 |
|
164,9304 |
|
167,26 |
168,9342 |
173,04 |
|
|
174.967 |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
**Актиноиды |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
90 |
|
|
91 Прот- |
|
92 |
|
|
93 Неп- |
|
94 Плу- |
|
95 Аме- |
|
96 |
|
|
|
97 |
|
|
|
98 Кали- |
99 Эйн- |
|
100 |
|
101 Мен- |
102 Но- |
|
103 Лоу- |
|
||||||||||||
|
Торий |
|
|
актиний |
|
Уран |
|
туний |
|
|
|
тоний |
|
риций |
|
Кюрий |
|
Берклий |
|
|
форний |
штейний |
|
|
Фермий |
|
делевий |
белий |
|
ренсий |
|
|||||||||||||
|
Th |
|
|
Pa |
|
|
|
U |
|
Np |
|
|
|
Pu |
|
Am |
|
Cm |
|
|
Bk |
|
|
Cf |
Es |
|
|
Fm |
|
Md |
|
No |
|
Lr |
|
|||||||||
|
232,0381 |
|
231,0359 |
|
238,0389 |
|
237,0482 |
|
[244] |
|
|
[243] |
|
[247] |
|
|
[247] |
|
|
[251] |
|
[252] |
|
[257] |
|
[258] |
|
[255] |
|
|
[260] |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
36 |
|
|
|
Общая часть |
|
|
|
|
|
|
|
|
Таблица 3 |
|
|
Средний химический состав литосферы в вес. % |
||||
|
|
(по А. П. Виноградову, 1949, с уточнениями)* |
||||
|
|
|
|
|
|
|
I |
О — 47,0 |
V |
Ni — 0,008 |
VII |
Cd — (5 × 10–5) |
|
|
Si — 27,5 |
|
Zn — 0,0068 |
|
Sb — (4 × 10–5) |
|
|
|
|
|
Li — 0,0065 |
|
Cs — (4 × 10–5) |
|
|
|
|
Ce — 0,0045 |
|
I — 3 × 10–5 |
|
|
|
|
Sn — 0,004 |
|
Bi — (2 × 10–5) |
|
|
|
|
Co — 0,003 |
|
In — (2 × 10–5) |
|
|
|
|
Y — 0,0028 |
|
Ag — (1 × 10–5) |
|
|
|
|
La — 0,0018 |
|
|
II |
Al — 8,6 |
|
VIII |
Se — 7 × 10–6 |
||
|
Fe — 5,0 |
|
As — 0,0018 |
|
Hg — 7 × 10–6 |
|
|
Ca — 3,5 |
|
Ga — 0,0015 |
|
Os — 5 × 10–6 |
|
|
Mg — 2,26 |
|
Pb — 0,0013 |
|
Pd — 1 × 10–6 |
|
|
Na — 2,5 |
|
Nb— 0,001 |
|
|
|
|
|
|
|
|
||
|
K — 2,13 |
|
|
|
|
|
|
|
|
|
|
|
|
III |
Ti — 0,60 |
|
|
|
|
|
|
H — (0,15) |
|
|
|
|
|
|
|
|
|
|
|
|
IV |
Mn — 0,09 |
VI |
Th — 8 × 10–4 |
IX |
Au — 5 × 10–7 |
|
|
S — 0,09 |
|
Ge — 7 × 10–4 |
|
Pt — 5 × 10–7 |
|
|
P — 0,08 |
|
Bе — 7 × 10–4 |
|
Ru — (5 × 10–7) |
|
|
F — 0,06 |
|
Sc — 6 × 10–4 |
|
Те — (3 × 10–7) |
|
|
Cu — 0,05 |
|
Mo— 3 × 10–4 |
|
Ir — 1 × 10–7 |
|
|
Ba — 0,05 |
|
B — 3 × 10–4 |
|
Rh — 1 × 10–7 |
|
|
C — (0,02) |
|
U — 3 × 10–4 |
|
Re — 1 × 10–7 |
|
|
Cl — 0,018 |
|
Tl — 3 × 10–4 |
|
|
|
|
|
XI |
Ra — l × 10–10 |
|||
|
Sr — 0,04 |
|
Hf —2,4 × 10–4 |
|
Pa — (1 × 10–10) |
|
|
Cr — 0,02 |
|
Та — 2 × 10–4 |
|
|
|
|
Zr — 0,016 |
|
Br — 1,6 × 10–4 |
|
|
|
|
V — 0,015 |
|
W — 1 × 10–4 |
|
|
|
|
Rb — 0,011 |
|
|
|
|
|
|
N —(0,01) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
* В таблице приведены не все элементы из группы редких земель, а также благород ные газы, количественные определения которых ненадежны. Данные для первых вось ми элементов, а также для серы исправлены согласно последним указаниям А. П. Ви ноградова.
Sn, Сr, W, Nb, Та, Th, U) преимущественно распространена в виде кисло родных соединений, но зато многие другие элементы (Fe, Ni, Co, Zn, Cu, Pb, Hg, Mo, Bi, As, Sb, Ag и др.) встречаются главным образом в виде скоп лений сернистых, мышьяковистых и сурьмянистых соединений. Железо совмещает в себе свойства сидерофильных, литофильных и халькофиль ных элементов, обладая заметным сродством как к кислороду, так и к сере.
|
Глава 1. Земная кора и особенности ее состава |
|
37 |
||||||
|
|
|
|
|
|
|
Таблица 4 |
||
|
Распространенность главных металлов в земной коре |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
Декады |
II |
III |
IV |
V |
VI |
VII |
VIII |
IX–XI |
|
|
|
|
|
|
|
|
|
|
|
Металлы |
Al, Fe |
Ti |
Mn, |
Ni, Zn, |
Th, Cs, |
Cd, Sb, |
Hg, |
Au, Pt, |
|
|
Mg, Ca |
|
Cr, V, |
Sn, Co, |
Be, As, |
Bi, Ag, |
Os, Pd |
Ru, Ir, |
|
|
|
|
Cu |
Y, La, |
Mo, U |
In |
|
Rh, |
|
|
|
|
|
Pb, Cе, |
Tl, Та, |
|
|
Re, Ra |
|
|
|
|
|
Nb |
W |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
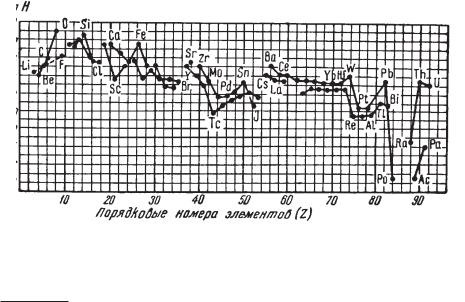
На диаграмме (рис. 4) по оси абсцисс расположены порядковые номе ра химических элементов, а по оси ординат — логарифмы их атомных кларков. Можно видеть, что с увеличением порядкового номера кривые кларков как четных, так и нечетных элементов в общем обнаруживают тенденцию к понижению. Это означает, что для большинства химических элементов имеет место обратно пропорциональная зависимость их сред него содержания в земной коре от порядкового номера, хотя встречаются и исключения (например, для Li, Be, В и др.).
Если сравнить распространенность химических элементов в земной коре в атомных кларках с числами минералов, в которые они входят, то, как ука зал П. П. Пилипенко, между ними, за небольшим исключением, устанавли вается некоторая прямая (симбатная) зависимость. Это имеет место преиму щественно для элементов, обладающих малыми атомными весами1.
Рис. 4. Распространенность элементов в верхней части литосферы. На диаграмме даны логарифмы атомных кларков (H) как функция порядкового номера (Z), причем кисло род принят за единицу
1 В число минералов не включены лишь разновидности, в которые данный элемент входит в виде изоморфной примеси.
38 |
|
Общая часть |
|
|
|
||
|
|
|
|
|
|
Таблица 5 |
|
|
Взаимосвязь числа минералов легких элементов и их атомных кларков |
||||||
|
|
|
|
|
|
|
|
|
Элемент |
Атомный |
Число ми- |
Элемент |
Атомный |
Число ми- |
|
|
|
кларк |
нералов |
|
кларк |
нералов |
|
|
|
|
|
|
|
|
|
|
О |
53,39 |
3550 |
Fe |
1,31 |
1170 |
|
|
|
|
|
|
|
|
|
|
Н |
17,25 |
2581 |
К |
1,05 |
439 |
|
|
|
|
|
|
|
|
|
|
Si |
16,11 |
1327 |
С |
0,51 |
361 |
|
|
|
|
|
|
|
|
|
|
Al |
4,80 |
978 |
Ti |
0,22 |
281 |
|
|
|
|
|
|
|
|
|
|
Na |
1,82 |
782 |
Cl |
0,10 |
288 |
|
|
|
|
|
|
|
|
|
|
Mg |
1,72 |
695 |
S |
0,05 |
923 |
|
|
|
|
|
|
|
|
|
|
Ca |
1,41 |
1174 |
F |
0,07 |
335 |
|
|
|
|
|
|
|
|
|
Некоторые из легких элементов играют особую роль в минералах, являясь типичными анионами или анионообразователями. Среди та ких элементов прежде всего можно отметить кислород, а также водо род (как компонент гидроксильного иона), серу, углерод и некоторые другие. Так как подавляющее большинство минералов является поляр ными соединениями, в составе каждого из них должны присутствовать элементы, играющие роль катионов и анионов. Типичных анионов и анионообразователей среди элементов Периодической системы гораз до меньше, чем катионообразующих элементов, поскольку металлы составляют около 3/4 всех элементов. По этой причине каждый из не многих элементов анионообразователей будет представлен в относи тельно большем числе минералов по сравнению с элементами, атомы которых играют роль катионов. Этим объясняется столь значительное количество минералов — кислородных соединений, а также водосодер жащих минералов и сульфидов. Для большинства распространенных элементов металлов (главным образом легких и средних атомных ве сов) число минеральных видов проявляет устойчивую пропорциональ ность их атомным кларкам.
Для многих тяжелых металлов подобная зависимость не устанавлива ется. Так, теллур, атомный кларк которого в земной коре примерно в 40 раз меньше, чем кларк селена, в природных условиях образует около 150 са мостоятельных минералов, в то время как для селена их известно всего около 100, и то главным образом в ассоциации с серой. Для цинка с атом ным кларком в 17 раз большим по сравнению с кларком свинца мы имеем около 250 минералов, тогда как для свинца — около 450, и т. д.
Указанные различия, несомненно, вызываются химическими свой ствами самих элементов, обусловленными строением их ионов и опреде ляемыми положением этих элементов в Периодической системе Менде
Глава 1. Земная кора и особенности ее состава |
39 |
леева. Для элементов с одинаковыми свойствами, аналогичными строением и размерами ионов, но с различными концентрациями в данном растворе или расплаве естественно ожидать, что при кристаллизации элементы с мень шей концентрацией будут входить в кристаллические структуры, образуе мые господствующими элементами, как бы растворяясь в них. Если же данный элемент в окружающей среде не находит аналогичных себе по размерам и строению ионов других элементов, то в каком бы количестве он ни присутствовал в растворе при кристаллизации, он должен образо вать самостоятельное соединение. Весьма показательно, что двухвалент ный марганец в главной своей массе входит в состав минералов в виде изоморфной примеси к двухвалентным железу и кальцию, но зато четы рехвалентный марганец всегда образует явно индивидуализированные соединения. Этим же объясняется то, что такие элементы, как рубидий, скандий, гафний, индий, рений и др., обладающие низкими атомными кларками, в природе образуют лишь несколько самостоятельных мине ралов, преимущественно же находятся в рассеянном состоянии, присут ствуя в виде изоморфной примеси к другим элементам. В значительной мере это относится и к таким более распространенным элементам, как селен, ванадий, цезий, кадмий и др. Наоборот, элементы с очень низкими атомными кларками — теллур, золото, группа платиновых металлов, вис мут и др. — сравнительно часто устанавливаются в виде самостоятель ных минералов.
Глава 2
КОНСТИТУЦИЯ И СВОЙСТВА МИНЕРАЛОВ
2.1. ОБЩИЕ СВЕДЕНИЯ
Когда мы осматриваем минералы в музейных витринах или лотках со специально подобранными образцами, нас невольно поражает то разно образие внешних признаков, по которым они отличаются друг от друга.
Одни минералы кажутся прозрачными (горный хрусталь, каменная соль), другие — мутными, полупрозрачными или совершенно не пропус кающими свет (магнетит, графит).
Замечательной особенностью многих природных соединений является их окраска. Для ряда минералов она постоянна и весьма характерна. Например, киноварь (сернистая ртуть) всегда обладает карминно крас ным цветом, для малахита характерна ярко зеленая окраска, кубические кристаллики пирита легко узнаются по металлически золотистому цве ту и т. д. Наряду с этим окраска большого количества минералов измен чива. Таковы, например, разновидности кварца: бесцветные (прозрачные), молочно белые, желтовато бурые, почти черные, фиолетовые, розовые.
Блеск — также весьма характерный признак многих минералов. В од них случаях он очень похож на блеск металлов (галенит, пирит, арсено пирит), в других — на блеск стекла (кварц), перламутра (мусковит). Не мало и таких минералов, которые даже в свежем изломе выглядят матовыми, т. е. не имеют блеска.
Часто минералы встречаются в кристаллах, иногда очень крупных, иног да чрезвычайно мелких, устанавливаемых лишь с помощью лупы или мик роскопа. Для ряда минералов кристаллические формы весьма типичны, на пример, для пирита — кубические кристаллы, для гранатов — ромбические додекаэдры, для берилла — шестигранные призмы. Однако в большинстве случаев минеральные массы наблюдаются в виде сплошных зернистых аг регатов, в которых отдельные зерна не обладают кристаллографическими очертаниями. Многие минеральные вещества распространены также в виде «натечных» масс, иногда причудливой формы, ничего общего не имеющей с кристаллами. Таковы, например, почковидные массы малахита, сталактито подобные образования лимонита (гидроокислов железа).
Минералы различаются и по другим физическим свойствам. Одни из них настолько тверды, что легко оставляют царапины на стекле (кварц,
