
Betekhtin
.pdfОПИСАТЕЛЬНАЯ ЧАСТЬ
КЛАССИФИКАЦИЯ И НОМЕНКЛАТУРА МИНЕРАЛОВ
Принципы классификации. За последние пять шесть десятилетий почти все главные руководства по минералогии строились по схемам хи мической классификации минералов. В основе всех вариантов этой клас сификации (В. И. Вернадского, Дж. Дэна, П. Грота, А. К. Болдырева, Х. Штрунца и др.) в той или иной форме лежит периодический закон хи мических элементов, открытый Д. И. Менделеевым.
Этим объясняется то, что основное деление всех минералов на классы по типам химических соединений за небольшими изменениями прочно укоре нилось в современной систематике минералов. Однако подразделения внут ри классов на подклассы и группы минералов в связи с величайшими дости жениями в области изучения строения кристаллических веществ, особенно за последние 70–80 лет, претерпели весьма существенные изменения.
Рентгеноструктурные исследования кристаллов, основанные на вы воде Е. С. Федоровым 230 пространственных групп, доказали взаимосвязь между химическим составом и кристаллическим строением вещества, что позволило уточнить химические формулы многих сложных соединений. Этим путем удалось совершенно определенно выяснить, что такие соеди нения, как минералы группы шпинели, большинство титанатов и ниобо танталатов, выделявшиеся ранее в виде самостоятельных классов, пред ставляют не что иное, как сложные окислы. Коренным образом изменились наши представления и о химической природе силикатов, в кристаллических структурах которых раскрыты самые различные по форме и строению комплексные анионы.
Не менее существенным для нас следствием этих достижений является установление функциональной зависимости от особенностей кристалличе ского строения не только внешних форм кристаллов, но и таких свойств, как оптические, электрические, механические (твердость, спайность, упругость) и пр. Оказалось, что все эти свойства минералов обусловлены как простран ственным расположением структурных единиц (ионов, атомов или молекул) при определенных соотношениях их размеров, так и природой связи между
152 |
Описательная часть |
ними и свойствами самих ионов или атомов, определяемыми положени ем их в таблице химических элементов Менделеева, а следовательно, и их строением.
Мало того, закономерности сочетания химических элементов при минералообразовании приводят к более глубоким представлениям о ге незисе минералов. Становится понятным, почему и в каком порядке про исходит «отбор» и сочетание тех или иных ионов при образовании крис таллов, выпадающих из растворов или расплавов, в зависимости от физико химических факторов равновесия системы (температуры, давле ния и концентрации химических компонентов). Отсюда нетрудно дога даться, почему в природе происходит направленное распределение хи мических элементов и типов химических соединений в различных последовательно возникающих продуктах магматической деятельности (изверженных горных породах, пегматитах, гидротермальных образова ниях) или в продуктах экзогенных процессов, приводящих к образова нию коры выветривания и химических осадков в водных бассейнах, и т. д.
В течение XX в. минералогия прошла большой путь в своем разви тии, претерпев постепенное превращение из науки чисто описательной в науку аналитическую, способную обнаруживать связь между фактами и давать им объяснение. Одним из важнейших инструментов естествозна ния и необходимым условием для понимания закономерностей в устрой стве природы, частью которой является царство минералов, служит сис тематика, имеющая своей задачей распределить объекты науки по классам и другим таксонам (подразделениям) с учетом естественных связей и раз личий. Взамен устаревших классификаций, основанных на сопоставле нии свойств минералов, появлялись классификации, учитывающие хи мический состав, а в последнее время все более принимаются во внимание особенности конституции минерала в целом. Давно уже стало немысли мым понимание свойств минералов без увязки с химическим составом и разбора кристаллических структур. И наоборот, как показал В. С. Собо лев, в тех случаях, когда мы еще не знаем кристаллической структуры минерала, мы можем по физическим и химическим свойствам судить о принадлежности его к тому или иному структурному типу соединений, обладающих общими свойствами.
Таким образом, классификация минералов должна быть кристаллохи' мической и основываться на данных изучения взаимосвязи всех свойств природных химических соединений с их химическим составом и кристал' лической структурой.
При разработке классификации минералов, принятой в данном учеб нике, были учтены следующие главные положения.
Все природные образования, составляющие предмет минералогии, так же как и все искусственные вещества в химии, необходимо делить преж де всего на две большие самостоятельные группы:
Классификация и номенклатура минералов |
153 |
1)неорганические минералы, к которым, кроме редко встречающихся самородных элементов, относятся природные соединения (за исключе нием органических) всех элементов;
2)органические минералы, представленные разнообразнейшими соеди нениями углерода (исключение составляют лишь карбонаты и карбиды, относимые к неорганическим соединениям).
Органические соединения, как известно, весьма существенно отлича ются от неорганических не только по химическим свойствам, но и по кри сталлическому строению и природе связей между структурными едини цами. Степень изученности этих групп минералов крайне неодинакова.
Вто время как наши знания по неорганическим минералам в настоящее время далеко продвинулись вперед, минералогия органических соедине ний находится еще в самой начальной стадии развития.
Если 70 лет назад такие природные вещества, как торф, бурые и камен ные угли, смолы и нефти рассматривались еще как самостоятельные мине ралы, то теперь, в результате исследований, в частности, твердых органи ческих веществ с применением новейших методик исследования, стало совершенно ясно, что они представляют собой далеко не однородные по составу массы, состоящие из различных органических веществ и минера лов, истинную природу которых начали изучать в самое последнее время.
Классификация неорганических минералов построена на следующих принципах. Так как минералы являются кристаллическими продуктами естественных химических реакций, то для наших целей наиболее рацио нальной должна быть систематизация их по химическому составу и кри сталлической структуре. Именно с этими признаками связаны те важней шие химические и физические свойства, по которым мы распознаем минералы и условия их образования.
Все минералы неорганической природы с химической точки зрения разбивают прежде всего на большие группы, отличающиеся друг от друга по типу химического соединения и типу химических связей между струк турными единицами. Первоначальное разбиение соединений на наибо лее крупные разделы целесообразно проводить по анионам, так как их число по сравнению с катионами относительно невелико.
Особое положение при этом занимают самородные элементы (простые вещества), представленные главным образом металлами с характерной для них металлической связью между атомами. К ним же должны быть отнесены и интерметаллические соединения, представляющие собой при родные аналоги сплавов.
Самостоятельный раздел составляют сернистые и им подобные соеди нения, по ряду свойств занимающие промежуточное положение между типичными металлами и соединениями с ионной связью; при этом в боль шинстве сульфидов существенную роль играет также ковалентная состав ляющая химической связи. К этому же разделу условно присоединим так

154 |
Описательная часть |
называемые сульфосоли, имеющие к сульфидам такое же отношение, какое кислородные соли имеют к окислам.
Характерный тип химических соединений, но уже с типичной ион ной связью, представляют галогениды, или галоидные соли, т. е. соедине ния металлов с фтором, хлором, бромом и йодом.
К следующему разделу должны быть отнесены окислы и гидроокислы (простые и сложные соединения металлов с кислородом или гидроксилом).
Наконец, чрезвычайно многочисленную группу минералов составля ют соли кислородных кислот, т. е. соединения катионов металлов с раз личными комплексными анионами, содержащими кислород.
В ряде указанных разделов необходимо проводить дальнейшее подраз деление минералов по типам анионов на классы и подклассы. Внутри послед них в определенном порядке выделяются группы минералов по признакам сходства кристаллических структур и химических особенностей минералов, обусловливаемых главным образом катионами, входящими в их состав.
Таким образом, общая классификация неорганических минералов в схе ме может быть представлена в следующем виде (без деления на группы). Раздел I. Самородные элементы и интерметаллические соединения. Раздел II. Карбиды, нитриды и фосфиды1.
Раздел III. Сульфиды, сульфосоли и им подобные соединения.
Класс 1. Простые и двойные сернистые и им подобные соединения (селениды, теллуриды, арсениды и др.).
Класс 2. Сульфосоли.
Раздел IV. Галоидные соединения (галогениды) и галогеносоли. Класс 1. Фториды и алюмофториды.
Класс 2. Хлориды, бромиды и иодиды. Раздел V. Окислы (оксиды).
Класс 1. Простые и сложные окислы. Класс 2. Гидроокислы (гидроксиды).
Раздел VI. Кислородные соли. Класс 1. Иодаты1.
Класс 2. Нитраты. Класс 3. Карбонаты.
Класс 4. Сульфаты и селенаты. Класс 5. Хроматы.
Класс 6. Молибдаты и вольфраматы. Класс 7. Фосфаты, арсенаты и ванадаты. Класс 8. Арсениты, селениты и теллуриты1.
1 Эти соединения в данном курсе не рассматриваются.
Классификация и номенклатура минералов |
155 |
Класс 9. Бораты.
Класс 10. Силикаты и алюмосиликаты (бериллосиликаты, боросиликаты). А. Силикаты с изолированными тетраэдрами аниона SiO4.
Б. Силикаты с изолированными группами тетраэдров SiO4.
В. Силикаты с непрерывными цепочками и лентами тетраэдров SiO4. Г. Силикаты с непрерывными слоями тетраэдров SiO4.
Д. Силикаты с непрерывными трехмерными каркасами тетраэд ров SiO4 и АlО4.
При описании минералов характеристику зависимости главнейших свойств минералов от состава и кристаллической структуры, во избежание многократных повторений, приведем во введениях к каждому разделу, клас су, подклассу и группе, поскольку эта общность связей в минералах являет ся основой для объединения их при группировке. При описании отдельных минералов добавим лишь дополнительные характеристики их свойств, обус ловленных специфическими особенностями строения и состава.
Минеральные виды и разновидности. Основной классификационной единицей при систематике природных химических соединений является минеральный вид, обладающий химическим составом, изменяющимся в определенном интервале и однотипной кристаллической структурой. Правила выделения и наименования видов в минералогической систе матике составляют так называемую номенклатуру минералов. Учитывая непостоянство химического состава реальных минералов, становится ясно, что понятие минерального вида является необходимой абстракци ей, позволяющей отнести любые конкретные индивиды минералов к оп ределенным классификационным единицам.
Явление полиморфизма приводит к существованию минералов оди накового состава с существенно различными кристаллическими струк турами. С этой точки зрения полиморфные модификации одного и того же кристаллического вещества представляют собой самостоятельные минеральные виды (графит и алмаз, α сера и β сера и др.).
Втех случаях, когда два изоструктурных вещества образуют друг с дру
гом непрерывный ряд твердых растворов (например, Аu — Ag, MnWO4 — FeWO4, Na[AlSi3O8] — Ca[Al2Si2O8] и др.), с физико химической точки зрения мы имеем одну фазу. Однако в практике минералогии во многих случаях укоренилось несколько названий не только для крайних, но и для промежуточных по составу членов изоморфного ряда (например: золото — электрум — серебро; гюбнерит— вольфрамит — ферберит; альбит — оли гоклаз — андезин — лабрадор — битовнит — анортит).
Внастоящее время минеральные виды в системах с изоморфизмом выделяются по доминирующему компоненту (элементу) в каждом типе позиций, в которых происходит замещение. Формально минеральному виду в рядах (сериях) и полях составов с совершенным изоморфизмом приписывается химическая формула чистого крайнего члена, индивиды
156 |
Описательная часть |
спромежуточными составами относятся к тому или иному минерально му виду по преобладающему в них изоморфному элементу. Традиционно же употреблявшиеся наименования промежуточных составов не счита ются видовыми, однако допускается их употребление для ряда в целом, так что они приобретают статус названия для минеральных групп. Так, в ряду форстерит Mg[SiO4] — фаялит Fe[SiO4] все минеральные индивиды
сMg, преобладающим над Fe, будут отнесены к форстериту, прочие — к фаялиту. В то же время для любого представителя этого ряда может быть употреблено общее название «оливин» как для представителя группы, но «оливин» не является названием минерального вида.
Таким образом, в двухкомпонентных системах при установлении гра ницы между минеральными видами действует правило 50 %, в случае трехкомпонентной системы — 33,(3) % и т. д. В случае систем с несовер шенным изоморфизмом границы видов определяются краями разрывов смесимости, кроме этого также по прежнему учитываются и процентные границы, определяемые доминированием того или иного изоморфного компонента над остальными в данной позиции структуры. Подобное раз деление проводится и для серий с изодиморфизмом, когда чистые ком поненты принадлежат к разным структурным типам и в ряду твердых растворов есть состав, при котором скачком изменяется структура. Этот состав также будет границей различных минеральных видов.
Под разновидностями подразумевают такие одинаковые или почти одинаковые по составу и кристаллическому строению минералы (т. е. принадлежащие к одному минеральному виду), которые лишь несколько отличаются по следующим признакам:
1)по особенностям химического состава, когда какой либо из химических компонентов, характеризующих состав данного минерала, отчасти изоморф
но замещен другим компонентом (например, кобальтистый пирит (Fe,Co)S2, разновидность пирита, не отличимая от него без химических реакций);
2)по структуре, в зависимости от политипной модификации минера ла (так как политипы, в отличие от полиморфов, относятся за редкими исключениями к одной и той же фазе), например, двухслойный гексаго
нальный MoS2 — молибденит 2H и трехслойная ромбоэдрическая моди фикация MoS2 — молибденит 3R;
3)по физическим признакам, когда состав и структура практически одни и те же, но некоторые физические свойства отличаются (например, диаллаг от обычного диопсида отличим по характерной отдельности; или
сажистая разновидность пиролюзита (МnО2) отличается от кристалли ческих индивидов (полианит) лишь по степени дисперсности, матовому блеску и ложной низкой твердости);
4)по составу и физическим свойствам одновременно (например, сильно железистая разновидность сфалерита (Zn, Fe)S отличается от основной, ма ложелезистой разновидности, обычно светлоокрашенного вида, гораздо бо лее темной, почти черной окраской и некоторыми другими признаками);
Классификация и номенклатура минералов |
157 |
5) по морфологии, в зависимости от различий в форме выделений (на пример, немалит — параллельно волокнистая разновидность брусита, обыкновенно таблитчатого или короткостолбчатого, арканзит — изомет рического облика дипирамидальные кристаллы брукита, обычные крис таллы которого — удлиненные пластинки).
Каждый минеральный вид определенного химического состава носит специальное название. Полиморфные модификации в большинстве сво ем также имеют свои названия или одно общее название, но с приставка ми греческих букв α , β , γ ... Что касается разновидностей минералов, то
впрежнее время им широко давались особые названия даже в тех случа ях, когда они имели несущественное отличие в химическом составе. К на стоящему времени многие из этих названий утратили свое существова ние. Сохранились лишь названия драгоценных камней (изумруд, рубин, сапфир, аметист, цитрин, морион и др.).
Разновидности минералов по химическому составу обычно называют собственными именами с прилагательным, характеризующим какую либо особенность состава данной разновидности (например, магнезиальный маг нетит, стронцистый арагонит и др.). Употребление приставок для имено вания разновидностей по составу (например — титанавгит, манганкальцит)
внастоящее время не приветствуется, так как подобные приставки закон но используются для именования определенных минеральных видов, на пример — ферроаксинит, манганколумбит и др. Для разновидностей по составу общепринята следующая форма записи названий: Mn кальцит — марганцовистый кальцит, Ti андрадит — титанистый андрадит, Cr диоп сид — хромистый диопсид (но не хромдиопсид). Следует при этом обра тить внимание на то, что существует особая форма записи наименований минеральных видов для минералов с изоморфизмом редкоземельных эле ментов: монацит (La) — лантан доминантный монацит, монацит (Nd) — неодим доминантный монацит, паризит (Y) — иттрий доминантный па ризит (или иттриевый паризит, но не иттристый) и т. п.
Подобная практика недавно утвердилась и в отношении минералов явно перегруженной группы цеолитов, в которой реализуется около 40 различных структурных типов. Для именования различных минераль ных видов — крайних членов изоморфных рядов изоструктурных цеоли тов — также применяются суффиксы, но без скобок: шабазит Ca —
Ca2[Al4Si8O24] . 12H2O, шабазит Na — (Na,Ca2)[Al4Si8O24] . 12H2O и т. п. Число названий лишь минеральных видов, благодаря открытиям но
вых минералов, каждый год увеличивается на несколько десятков и сейчас превосходит 4000, так что во избежание путаницы и засорения геологи ческой литературы излишними терминами, следует по возможности воз держиваться от употребления многочисленных синонимов, а названия разновидностей приводить лишь в дополнение к видовому, которое долж но употребляться обязательно.
Раздел I
САМОРОДНЫЕ ЭЛЕМЕНТЫ И ИНТЕРМЕТАЛЛИЧЕСКИЕ СОЕДИНЕНИЯ
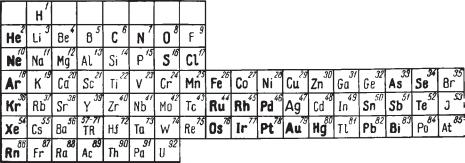
Общие замечания. В самородном состоянии в земной коре устанав ливается свыше 30 химических элементов, главным образом металлов. Сюда же относятся ряд газов и редко встречающиеся элементы в жид ком состоянии (ртуть, некоторые амальгамы). На рисунке 61 символы элементов, встречающихся в самородном состоянии, показаны полужир ным шрифтом.
Рис. 61. Элементы, встречающиеся в самородном виде (выделены полужирным шрифтом)
Общее весовое значение самородных элементов в земной коре очень невелико (не превышает 0,1 % всей массы земной коры). Из этого коли чества на долю азота приходится около 0,04 %, кислорода — 0,01–0,02 %. Все остальные элементы, встречающиеся в самородном виде, составля ют, следовательно, не больше 0,05 %. Из них в наибольших относитель ных количествах представлены: водород, аргон, гелий, углерод, сера, зо лото, элементы платиновой группы, медь и висмут.
Некоторые химические элементы в природе встречаются исключи тельно или почти исключительно в самородном состоянии и носят на звание благородных элементов.
К числу их прежде всего относится группа благородных газов: Не, Ne, Ar, Кr; Хe и Rn. Атомы их, как известно, обладают устойчивой двух и восьмиэлектронной наружной оболочкой, чем и обусловлена их хими ческая инертность, т. е. неспособность вступать в какие либо соединения с кислородом, водородом и другими элементами.
Раздел I. Самородные элементы и интерметаллические соединения |
159 |
Особое положение в таблице занимает также группа благородных ме таллов (Ru, Rh, Pd, Ag, Os, Ir, Pt и Аu), располагающихся в больших пери одах менделеевской таблицы — пятом и шестом. Характерно, что в этих периодах атомные радиусы элементов в вертикальных группах почти тож дественны (явление так называемого лантаноидного сжатия атомных объе мов). Это обстоятельство играет очень важную роль в химизме этих эле ментов в природных условиях, особенно в образовании изоморфных смесей для благородных металлов. Металлы платиновой группы, образуя твердые растворы, в месторождениях распространены всегда совместно. Элементы триады Fe, Co, Ni в составе этих минералов занимают обычно подчиненное положение. Еще резче проявлен изоморфизм для Аu и Ag, тогда как Сu в виде твердого раствора в них встречается очень редко.
Из остальных встречающихся в самородном состоянии элементов, расположенных в субпериодах правой части таблицы, чаще других рас пространены так называемые полуметаллы: As, Sb и Bi. Несмотря на общ ность некоторых химических свойств этих элементов, они в природе на блюдаются в разных условиях. Лишь иногда мышьяк и сурьма дают интерметаллическое соединение AsSb (аллемонтит).
Для углерода характерно нахождение его в двух различных по кристал лическому строению модификациях. Самородная сера в главной своей мас се возникает путем частичного окисления H2S, реже при восстановлении SO2, а также некоторых сернокислых и органических соединений, богатых серой.
Собственно самородные элементы составляют чуть более 30 минераль ных видов. Некоторые элементы, как известно, устанавливаются в двух или более полиморфных модификациях (алмаз, графит, α сера, β сера и др.). Большинство элементов, кроме того что встречается в чистом виде, образует твердые растворы друг с другом, например: электрум (Аu,Ag), палладистая платина (Pt,Pd), рассматриваемые, соответственно, в каче стве разновидностей золота и платины.
Распространены также чрезвычайно близкие по свойствам к метал лам интерметаллические соединения, обладающие стехиометрическими формулами и характеризующиеся своими особенностями кристалличе ской структуры (например, мальдонит Au2Bi, нигглиит PtSn, аурикуприд Сu3Au, кабриит Pd2СuSn, потарит PdHg и др.). Кроме стехиометриче ских соединений, среди интерметаллидов встречаются и соединения пе ременного состава, например тетраферроплатина (Pt,Fe)Fe, полярит Pd(Pb,Bi), хатыркит (Cu,Zn)Al2 и др.
Общее число минеральных видов (за счет, главным образом, интерметал лидов), относящихся к данному разделу, превышает 100, т. е. оно значительно больше, чем число элементов, в них входящих. Количество искусственно по лучаемых интерметаллических соединений достигает огромной цифры.
Кристаллические структуры и физические свойства минералов.
Самородные элементы, встречающиеся в твердом состоянии, обладают
160 |
Описательная часть |
различными кристаллическими структурами. По типу сил связей между атомами преобладающее значение имеют атомные структуры плотней шей упаковки с металлической связью, иногда с признаками связей, пе реходных к гетерополярной и вандерваальсовской. Этими особенностя ми обусловлен ряд важных общих свойств самородных металлов.
Из всех природных веществ самородные металлы обладают наилучшей электропроводностью и теплопроводностью. Все они в полированном виде обладают сильным металлическим блеском, т. е. высокой отражательной способностью. Показатели преломления, от которых зависит блеск, явля ются наивысшими. Лишь для золота, серебра и меди они меньше 1, но это также обусловливает высокую отражательную способность (см. рис. 26). Точно так же и показатели поглощения света исключительно высоки.
Большинство этих характеристик находится в прямой связи с элект ронной структурой металлов. Энергетические уровни электронных со стояний в металлах лишены дискретности и образуют широкие сплош ные полосы — энергетические зоны. Зоны валентных электронов и электронов проводимости в соединениях с преобладающей металличе ской связью перекрываются, что позволяет валентным электронам быть подвижными носителями заряда и обеспечивать высокую электропровод ность. Далее большая ширина зон позволяет электронам совершать пере ходы в широком диапазоне энергий. Возможность таких переходов обес печивает поглощение квантов электромагнитного излучения различных длин волн — практически всего видимого спектра, что и приводит к пол ной непрозрачности металлов.
Цвет преобладающего большинства самородных металлов серебряно или оловянно белый. Бросающимся в глаза исключением являются цве та золота и меди. Эти элементы могут обнаруживать более высокие ва лентности, чем следует по их положению в таблице элементов (Сu2+Сl12, Аu3+Сl13). Допускают, что избирательное отражение света связано с осо бенностями зонной структуры этих металлов.
Из всех известных минералов самородные металлы обладают наи большим удельным весом (особенно минералы элементов платиновой группы). Металлы, структура которых характеризуется координацион ным числом 12 и отсутствием направленных сил связей, обладают вы сокой ковкостью, отсутствием ясно выраженной спайности в изломе и обычно невысокой твердостью. В отношении твердости исключение составляют лишь иридий и минералы, содержащие этот элемент в зна чительных количествах.
Ковкость и пластичность металлов обусловлены главным образом числом направлений, нормально к которым расположены плотнейшие упакованные слои. В средах, обладающих кубической плотнейшей упа ковкой, таких направлений мы имеем четыре, тогда как в гексагональной структуре — одно. Поэтому металлы со структурами кубической упаков
