- •Предисловие
- •Введение
- •Спектральные методы.
- •Почему вещество способно поглощать электромагнитное излучение
- •Частота, длина волны и энергия электромагнитных колебаний
- •Спектральные диапазоны
- •Ультрафиолетовая спектроскопия.
- •Закон Бугера – Ламберта – Бера.
- •Инфракрасная спектроскопия и спектроскопия комбинационного рассеяния
- •Спектроскопия ядерного магнитного резонанса
- •Масс-спектрометрия
- •Хроматография
- •Газовая хроматография (гх и гжх)
- •Формальные аспекты газовой хроматографии
- •Составные части газового хроматографа
- •Газы, применяемые в хроматографии
- •Ввод пробы
- •Колонки,применяемые в газовой хроматографии
- •Неподвижная фаза
- •Детекторы применямые в газовой хроматографии
- •Детектор электронного захвата (дэз)
- •Пламенно-ионизационный детектор (пид)
- •Детектор по теплопроводности (дтп)
- •Качественный анализ
- •Количественный анализ
- •Тонкослойная хроматография
- •Формальные аспекты тонкослойной хроматографии
- •Преимущества и недостатки тсх
- •Экспрессность
- •Расход анализируемого вещества
- •Простота техники тсх
- •Наглядность и информативность
- •Простота протоколирования результатов
- •Простота оборудования
- •Стоимость
- •Характеристика основных “участников” тсх
- •Подложка
- •Сорбент
- •Растворители в тсх
- •Камеры для тсх
- •Методы проявления хроматограмм
- •Особенности качественного и количественного тсх-анализа
- •Качественный анализ
- •Количественный анализ
Камеры для тсх
В простейшем случае – для восходящей ТСХ на пластинках с закрепленным слоем хроматографическая камера представляет собой “банку с крышкой”. Единственным условием предъявлемым к таким камерам является их герметичность. Чем меньше отношение общего объема камеры к используемому объему элюента, тем ближе состав подвижной фазы на пластинке к приготавливаемому. Особенно это актуально, когда элюент содержит один из компонентов в малых количествах. Например, 10 см3элюента, состава ксилол-метанол (10:0.5), помещенных в камеру, объемом 1 дм3, содержат метанола лишь незначительно больше, чем его необходимо для насыщения всего объема камеры его парами. В результате, состав элюента, поступающего на пластинку, будет существенно отличаться от заданного соотношения. В высоких камерах сталкиваются с другой проблемой – градиентом концентрации компонентов элюента по высоте, что может в значительной степени исказить результаты. Для преодоления этой проблемы вдоль вертикальной стенки камеры следует закрепить полосу или лист фильтровальной бумаги, который смачивают элюентом по всей длине до начала элюирования.
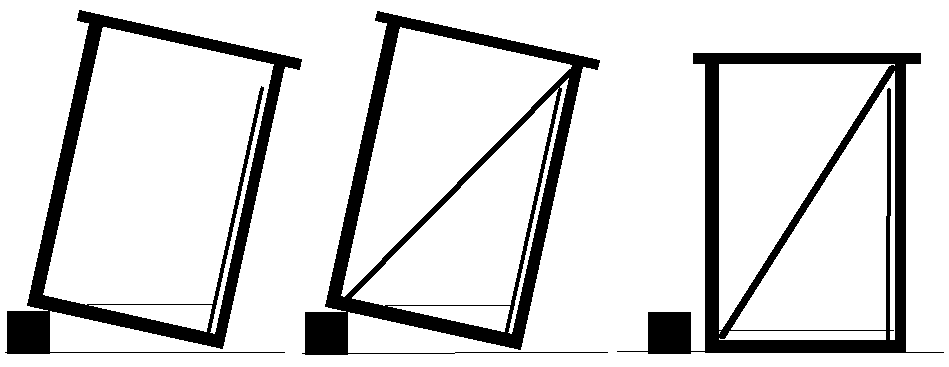
В ряде случаев для получения качественной хроматограммы оказывается необходимым насытить сорбент парами элюента до начала элюции. Для этого используют камеру с невысокой перегородкой, идущей по дну и разделяющей придонное пространство на два “отсека” (рисунок 6 .10A). В один отсек помещают элюент, в другой – устанавливают плас, в другой - устанавливают нтей по дну и разделяющей придонное пространство на два “отсекаи лист фильтровальной бумаги, который тинку. После насыщения парами элюента всего объема камеры и сорбента камеру наклоняют так, чтобы элюент перетек во второй отсек. При этом начинается элюция хроматограммы. Того же эффекта можно добиться, подставив под дно обычной камеры с плоским дном с одной стороны какой-либо предмет и установив пластинку нижним краем в приподнятый угол камеры. После насыщения этот предмет извлекается, и камера устанавливается ровно (рисунок 6 .10B). Для ТСХ на пластинках с незакрепленным слоем камера должна обеспечить почти горизонтальное расположение пластинки. Для градиентной хроматографии в камере должно быть два отверстия – одно для подачи элюента изменяющегося состава, второе – для удаления избытка элюента из камеры. В продаже имеются самые разнообразные камеры для различных видов ТСХ, в том числе, и для ТСХ под давлением.
|
|
| |||
|
A |
B | |||
|
Рисунок |
6.10 |
– Камеры для восходящей ТСХ с предварительным насыщением |
| |
сорбента. A – камера с перегородкой (CAMAG), B – использование камеры с плоским дном. Тонкой линией вдоль вертикальной стенки камеры обозначен лист фильтровальной бумаги, жирной диагональной – хроматографическая пластинка.
Методы проявления хроматограмм
Целью проявления хроматограммы является визуализация всех имеющихся на ней пятен. Чем меньше минимальное количество вещества, которое удается обнаружить при применении того или иного метода проявления, тем выше чувствительность этого метода. При изучении физико-химических свойств веществ чувствительность обнаружения значения не имеет. Напротив, чем выше чувствительность обнаружения веществ, являющихся нежелательными примесями, например, в лекарственном препарате, тем на более высоком уровне можно контролировать качество продукта. Метод обнаружения зависит, прежде всего, от спектральных свойств веществ в видимом или УФ-диапазоне.
Неокрашенные вещества, хорошо поглощающие УФ-излучение в области 254 и/или 365 нм (производные полициклических карбо- и гетероциклических соединений), удается обнаружить в достаточно малых количествах на пластинках с флуоресцентным индикатором. Так, примеси флуореновой природы в амиксине (коэффициент молярной экстинкции при 254 нм 50000 – 100000) обнаруживаются в количествах 0.05 – 0.1 мкг в зависимости от фирмы-производителя пластинок в виде темно-фиолетовых пятен на голубом или голубовато-зеленом фоне флуоресценции индикатора на пластинке. Если вещество само способно флуоресцировать при возбуждении УФ-светом, то предел его обнаружения на пластинках без флуоресценитного индикатора, как правило, значительно ниже. Так, изомерные 9-метоксиакридин и 10-метилакридон могут быть обнаружены в количествах 0.001 – 0.01 мкг, причем цвет их флуоресценции различается, что дает возможность различить эти два вещества даже в тех случаях, когда их Rfсовпадают.
Окрашенные вещества в большинстве случаев дают хорошо различимые визуально пятно, однако чувствительность их обнаружения, как правило, ниже, чем под УФ-облучением. Так, чувствительность обнаружения амиксина под УФ-светом более чем в 200 раз превышает чувствительность его обнаружения в видимом свете, а упомянутых выше 9-метоксиакридина и 10-метилакридона – в 100 – 1000 раз.
Если вещество не способно поглощать УФ-свет при 254 и 365 нм (или эффективность поглощения мала) и при этом неокрашено, то для его обнаружения необходимо применять специальные реагенты. Реагенты делятся на общие, групповые и индивидуальные.
К общим реагентам относятся йод, серная кислота при нагревании, сильные окислители в кислой среде. К наиболее популярным относится йод. Преимущества его обусловлены безопасностью, экспрессностью и простотой применения. Хроматограмму можно проявлять в герметичной емкости, в которой помещено небольшое количество кристалличего йода. Кирхнер рекомендует раствор иода в метаноле или гексане. Одним из наиболее удобных представляется способ, при котором йод адсорбируют встряхиванием кристаллического йода с сорбентом, а хроматограмму проявляют ее обсыпанием полученным проявителем. Если обнаруживаемое вещество обладает заметной липофильностью, то получают коричневые пятна (темно-синие – на слоях с крахмалом в качестве связующего после увлажнения пластинки парами воды). Сильногидрофильные вещества, напротив, оказываются менее окрашенными, чем фон. Сильные восстановители (например, гидразины, полиаминобензолы, полифенолы) дают ярко-белые пятна на бледно окрашенном фоне. Подробный список реагентов общего назначения и методов их применения приведен в монографии Ю. Кирхнера.
К групповым реагентам относятся реагенты, обработка хроматограммы которыми приводит к появлению специфической окраски пятен веществ, содержащих определенные функциональные группы. Так раствор нингидрина в кислой среде проявляет пятна аминокислот как темно-фиолетовые. Вещества, содержащие амидные группы (вместо аминов), не окрашиваются. Последние, так же как и амины дают синие пятна после обработки хроматограммы газообразным хлором с последующим опрыскиванием йод-толуидиновым реактивом. Первичные амины (в том числе и анилины) дают желто-оранжевые пятна при опрыскивании хроматограммы раствором 9-метоксиакридина в метаноле с последующим нагревом пластинки. Под действием этого же реактива пятна гидразинов и гидразидов приобретают окраску от желтой до красно-оранжевой немедленно без нагревания. Сам гидразин обнаруживается в виде темно-красного пятна. Фенолы (и некоторые сильные восстановители) образуют ярко синие пятна при обработке смесью растворов Na3[Fe(CN)6] и FeCl3, причем яркость окраски и, следовательно, чувствительность определения возрастают с увеличением числа гидроксильных групп в соединении. Так, 4,4'-дигидроксидифенил-2-карбоновая кислота (полупродукт в синтезе амиксина) обнаруживается таким образом в количествах около 1 нг.
Таким образом, использование проявляющих реактивов позволяет не только визуализывать пятна веществ на хроматограмме, но и определить в их составе весь набор основных функциональных групп. Нанесение на широкую пластинку стартового пятна в виде полосы позволяет после элюции, высушивания и разрезания хроматограммы на отдельные узкие полоски применить множество разных реактивов для проявления.