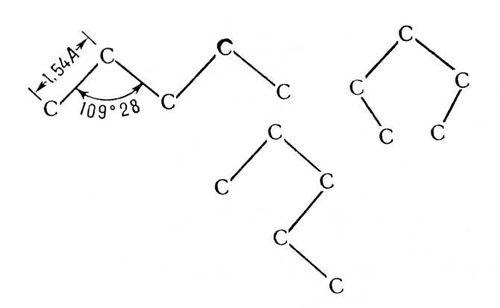
- •1. Электронное строение бутадиена. Химические свойства сопряженных алкадиенов. Механизм реакции электрофильного присоединения галогеноводородов к бутадиену-1,3.
- •2. С помощью каких химических превращений можно получить метан из:
- •4. Для сжигания 30 л метана израсходовали 300 л воздуха. Рассчитайте объемную долю кислорода потребовавшегося для данной реакции?
- •5. Приведите примеры реакций с участием предельных углеводородов, протекающих: а) с удлинением углеродной цепи; б) с уменьшением углеродной цепи (по 2 примера в каждом случае).
- •6. Как можно различить следующие соединения:
- •1. Циклические углеводороды. Строение, теория Байера, способы получения.
- •2.Дайте определение понятиям: атом, катион,радикал,электрофил, нуклеофил. Приведите примеры.
- •3.Напишите структурные формулы третичных аминов состава с6h15n. Назовите их.
- •5.Как получить бутанол-2, исходя из ацетилена и необходимых неорганических веществ?
- •1 .В каком случае донорно-акцепторное взаимодействие приводит к семиполярной связи? в чём её отличие от ионной и ковалентной? Приведите примеры.
- •2.Как можно получить:
- •4. Осуществите переход:
- •5. Теория Бутлерова. Привести примеры
1. Циклические углеводороды. Строение, теория Байера, способы получения.
Циклические УВ - это соединения с замкнутой (кольцевой или циклической) цепью атомов. Они делятся на изоциклические и гетероциклические.
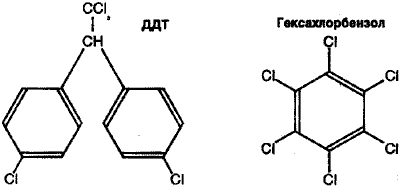
А. Байер выдвинул знаменитую теорию напряжения, согласно которой в молекуле бензола и в других подобных веществах связи между атомами углерода находятся под напряжением из-за присутствия в молекуле других атомов (помимо атомов углерода).
Получение: Гидрирование ароматических углеводородов, отщепление двух атомов галогена от дигалогеналканов
2.Дайте определение понятиям: атом, катион,радикал,электрофил, нуклеофил. Приведите примеры.
Атом — это наименьшая частица химического элемента, сохраняющая все его химические свойства.
Катио́н — положительно заряженный ион. Характеризуется величиной положительного электрического заряда: например, NH4+ — однозарядный катион, Ca2+ — двузарядный катион. В электрическом поле катионы перемещаются к отрицательному электроду — катоду.
Радикал — группа атомов, содержащая углеводородный остаток в молекуле.
Электрофил — катион или молекула, имеющая незаполненную электронную орбиталь, стремящийся к заполнению её электронами, т.к. это приводит к более выгодной электронной конфигурации атома (ион Н+).
Нуклеофил — атом или молекула, имеющий неподеленную пару электронов, взаимодействующих с участками молекул, на которых сосредоточен эффективный положительный заряд (CH3O-, Cl-, OH-).
3.Напишите структурные формулы третичных аминов состава с6h15n. Назовите их.
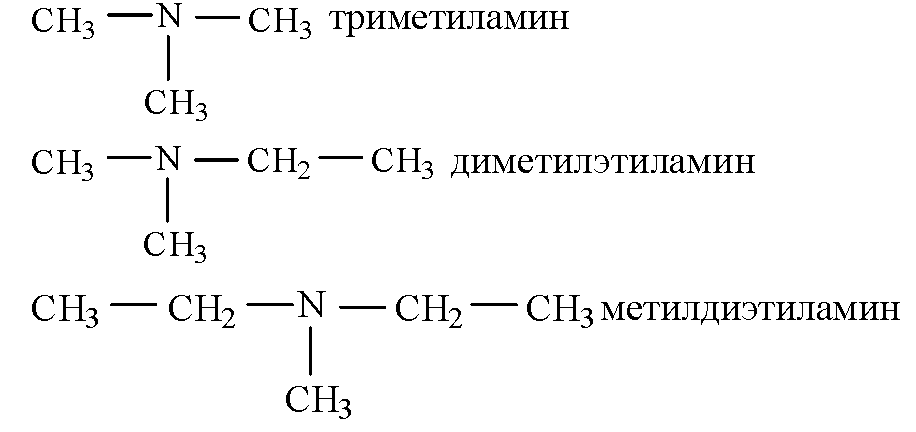
6.Как получить бутанол-2, исходя из ацетилена и необходимых неорганических веществ? Напишите уравнения реакции.
С2H2+2H2----> C2H6 этан С2Н6 +CL2----->C2H5CL +HCL хлорєтил 2 C2H5CL +2Na------>2NaCL + C4 H1O- бутан С4Н10 ---(-2H)----> CH3-CH2-CH=CH2 бутен-1 СH3--CH2-CH=CH2 +H2O----->CH3-CH2-CHOH-CH3 бутанол-2
19.
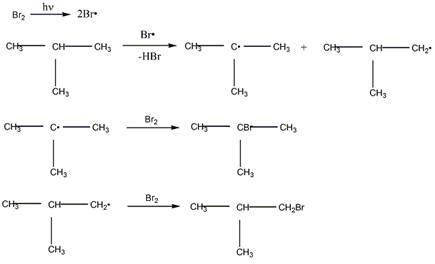
1. Химические свойства алканов. Механизм реакции SR на примере бромирования изобутана.
1. Горючесть алканов.
СnН2n+2 + O2 ––>CO2 + H2O + Q
2. Разложение алканов.
СnН2n+2= C + H2
СН4 =C + 2H2
С4Н10 = 4C + 5H2
Метан в термическом отношении более устойчив, чем другие алканы. Причина этого в достаточной прочности С – Н связей.
3. Реакции замещения (протекают с галогенами и другими окислителями при определённых условиях: свет, температура).
СН4 + Cl2= CH3Cl + HCl
СН3Cl + Cl2 =CH2Cl2 + HCl
СН2Cl2 + Cl2= CHCl3 + HCl
СНCl3 + Cl2 =CCl4 + HCl
3.Приведите структурные формулы всех диеновых углеводородов состава С5Н8. Назовите их.
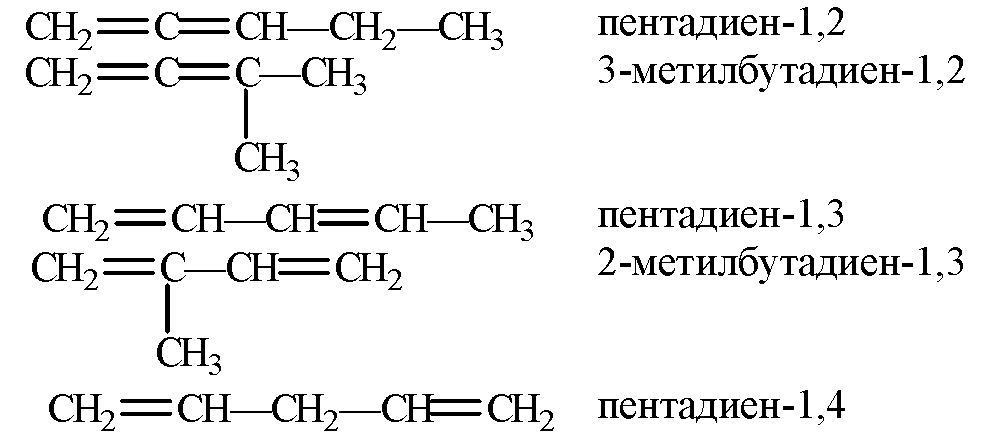
4.Какие соединения называют геометрическими изомерами? Чем они отличаются от конформационныз изомеров? Приведите примеры.
еометрические изомеры – это стереоизомеры различающие расположением заместителей относительно двойной связи.
! Условием существования геометрических изомеров является наличие у каждого углеродного атома двойной связи двух разных заместителей.
Для обозначения геометрических изомеров используется цис,транс-номенклатура:
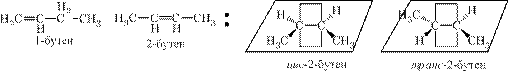
Однако часто данная номенклатура не позволяет однозначно назвать геометрические изомеры, поэтому используется более совершенная E,Z-номенклатура, которая основана на принципах системы Кана-Ингольда-Прелога.
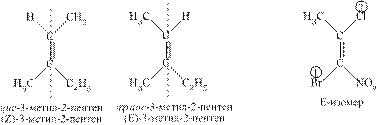
E-изомеры – это геометрические изомеры, в которых старшие заместители у атомов углерода двойной связи находятся по разные стороны от двойной связи, а в Z-изомерах – по одну сторону.
!Геометрические изомеры отличаются физическими и химическими свойствами.
В отличие от геометрических и оптических изомеров, конформеры при обычных условиях легко переходят друг в друга (без разрыва связей) и поэтому их нельзя изолировать (ср. Конфигурация). Молекулы органических соединений обычно существуют в виде смеси находящихся в равновесииконформеров, среди которых преобладают энергетически наиболее выгодные, т. е. обладающие наименьшей энергией. Конформационное состояние молекул влияет на физические свойства веществ, на направление и скорость их химических превращений.