
- •С. Г. Авдєєв, т. І. Бабюк
- •Частина 3 атом водню Основні формули
- •Приклади розв’язування задач
- •Елементи квантової механіки Основні формули
- •3. Часове рівняння Шредінгера має вигляд
- •Приклади розв’язування задач
- •Молекулярно-кінетична теорія ідеального газу Основні формули
- •Приклади розв’язання задач
- •Елементи термодинаміки Основні формули
- •Приклади розв’язання задач
- •Фізика твердого тіла Основні формули
- •Приклади розв’язання задач
- •Фізика атомного ядра Основні формули
- •Приклади розв’язування задач
- •Додаток а Деякі відомості з математики
- •2. Формули диференціального й інтегрального числень
- •3. Формули для наближених обчислень
- •Довідкові дані
- •Сергій Григорович Авдєєв
Приклади розв’язання задач
Приклад 1. Визначити число молекул, які містяться в об'ємі 1 мм3 води, і масу молекули води. Знайти також діаметр молекул. Вважати умовно, що молекули води мають вигляд кульок, які щільно прилягають одна до одної.
Дано:
H2O
V= 1 мм3 = 10-9м3
______________
N – ? m1 – ? d – ?
Розв’язування. Число N молекул, які втримуються в деякій системі масою m, дорівнює добутку постійної Авогадро NA на кількість речовини
![]()
Оскільки = m/, де – молярна маса, то N = (m / ) NA. Виразивши в цій формулі масу як добуток густини на об'єм V, одержимо
![]() ( 1)
( 1)
Виконаємо обчислення, врахувавши, що = 18 . 10-3 кг/моль,
= 1,0.103 кг/м3
![]() молекул.
молекул.
Масу m1 однієї молекули можна знайти за формулою
![]() ( 2)
( 2)
Підставивши в (2) значення і NA , знайдемо масу молекули води
![]() кг.
кг.
Якщо молекули води щільно прилягають одна до одної, то можна вважати, що на кожну молекулу приходиться об'єм V1 = d3, де d – діаметр молекули. Звідки
![]() ( 3)
( 3)
Об'єм V1
знайдемо, розділивши об'єм моля
![]() на число молекул у молі, тобто наNА
на число молекул у молі, тобто наNА
![]() ( 4)
( 4)
Підставивши вираз (4) в (3), одержимо
![]() ,
,
де V![]() =
/ .
=
/ .
Тоді
![]() . ( 5)
. ( 5)
Зробимо необхідні розрахунки
![]()
Приклад 2. Знайти масу сірчистого газу (SO2), який займає об'єм 25 л при температурі 27о С і тиску 101 кПа.
Дано:
SO2
V = 25 л = 25.10-3 м3
t = 27оC
P = 101 кПа = 1,01.105 Па
___________________
m – ?
Розв’язування. З рівняння Клапейрона маса газу дорівнює
![]() .
.
Визначаємо молярну
масу сірчистого газу за даними таблиці
Менделєєва
![]() й абсолютна температураT
= t + 273о
= 27о
+ 273о
= 300о
K.
й абсолютна температураT
= t + 273о
= 27о
+ 273о
= 300о
K.
Обчислюємо масу
![]()
Приклад 3. Балон містить 80 г кисню й 300 г аргону. Тиск суміші 10 атм, температура 15оС. Приймаючи дані гази за ідеальні, визначити ємність балона.
Дано:
O2
m1 = 80 г = 8.10-2 кг
Аr
m2 = 300 г = 3.10-1 кг
t = 15о C
P = 10 атм = 1,01.106 Па
_____________________
V – ?
Розв’язування. За законом Дальтона тиск суміші дорівнює сумі парціальних тисків газів, що входять до складу суміші. Парціальним тиском газу називається тиск, який здійснював би газ, якби тільки він один перебував у посудині, зайнятій сумішшю.
З рівняння Клапейрона парціальні тиски кисню p1 й аргону p2 виражаються формулами
![]() і
і
![]()
Отже, за законом Дальтона для суміші газів p = p1 + p2 або
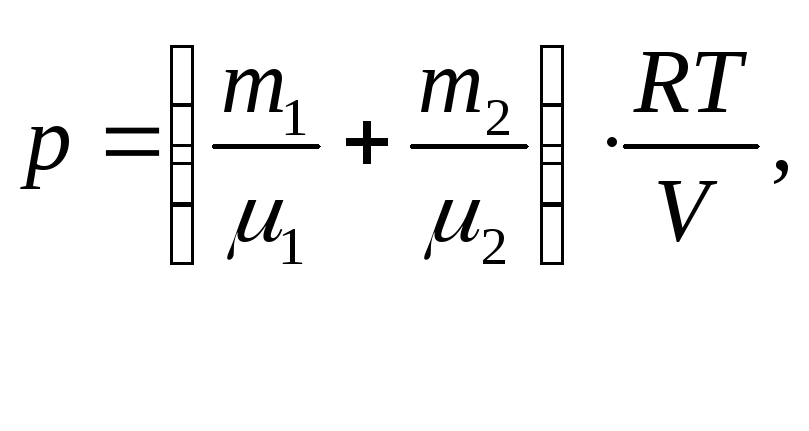
звідки об’єм балона дорівнює
![]() (
1)
(
1)
Виразимо в одиницях СІ числові значення величин, які входять у цю формулу: m1 = 0,08 кг; 1 = 32.10-3 кг/моль; m2 = 0,3 кг; 2 = 40.10 -3 кг/моль; p = 10.1,01. 105 Па; T = 288K; R = 8,31 Дж /(моль . К).
Підставимо числові значення у формулу (1) і виконаємо необхідні розрахунки
![]()
Приклад 4. Знайти кінетичну енергію обертального руху однієї молекули кисню при температурі 130С, а також кінетичну енергію обертального руху всіх молекул, які містяться в 4 г кисню.
Дано:
O2
m = 4 г = 4.10-3 кг
t = 13оC
_____________
об – ? Wоб – ?
Розв’язування. Відомо, що на кожну ступінь вільності молекули газу доводиться однакова енергія, яка виражається формулою
![]() (
1)
(
1)
де k – стала Больцмана;
T– абсолютна температура газу.
Оскільки обертальному руху двохатомної молекули (молекула кисню – двохатомна) приписуються дві ступені вільності, то енергія обертального руху молекули кисню виразиться формулою
![]() (
2)
(
2)
Підставивши у формулу (2) k = 1,38 . 10-23 Дж/К й T =286 K, одержимо
![]() Дж.
Дж.
Кінетична енергія обертального руху всіх молекул газу визначається з рівності
![]() ,
( 3)
,
( 3)
де N – число всіх молекул газу.
Число молекул N можна одержати за формулою
![]() ( 4)
( 4)
де NA – число Авогадро;
– число молів газу.
Число молів газу дорівнює
![]()
де m – маса газу;
![]() –маса одного
моля газу,
–маса одного
моля газу,
Кількість молекул газу визначається із формули (4)
![]() ( 5)
( 5)
Підставивши цей вираз N у рівність (3), одержимо
![]() ( 6)
( 6)
Виразимо величини, що входять у цю формулу, в одиницях СІ:
![]() моль-1;
моль-1;
![]() кг;
кг;
![]() кг/моль;
кг/моль;
![]() Дж.
Дж.
Підставивши ці значення у формулу (6), знайдемо
![]()
Приклад 5. На якій висоті над рівнем моря густина повітря зменшується у 2 рази? Вважати, що температура повітря не залежить від висоти й дорівнює 0оС. Молярна маса повітря дорівнює 29.10-3 кг/моль.
Дано:
1/ 2 = 2
t = 0оC
__________
h – ?
Розв’язування. Густина ідеального газу ( і його концентрація n) зв'язані співвідношенням
= nm0 ,
де m0 = / NA – маса однієї молекули повітря;
– молярна маса повітря;
NA – число Авогадро.
Таким чином, відношення густин газу 1/2 дорівнює відношенню концентрацій молекул n1/n2. Відповідно до розподілу Больцмана концентрація n молекул повітря на висоті h дорівнює
![]() ,
,
де n0 – концентрація молекул на рівні моря (h = 0);
Un – потенціальна енергія молекули на висоті h визначається за формулою Un = m0gh (якщо h = 0 то Un= 0) .
Концентрації молекул на висоті h = 0 і h відповідно дорівнюють
n1
= n0
й
n2
= n0
e![]() .
.
Відношення концентрацій на цих висотах дорівнює
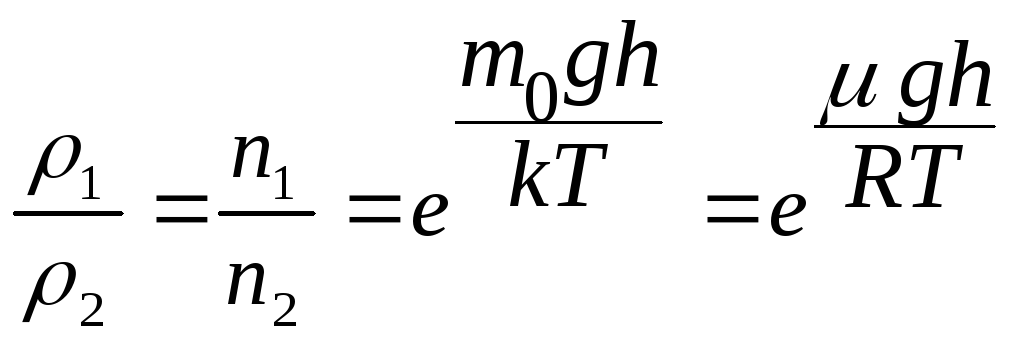 ,
,
де NAk
= R і
NAm0
=
![]() .
.
Беремо натуральний логарифм від обох частин відношення й знаходимо висоту h
![]()
Підставивши в отриману формулу дані з умови задачі, одержимо
h
=
![]() = 5,5.103м.
= 5,5.103м.
