
- •1. Алканы
- •Введение
- •1. Классификация органических соединений
- •2. Классификация органических реакций
- •3. Способы образования ковалентной связи
- •4. Гибридизация атомных орбиталей и форма органических молекул
- •4.1. Sp3-Гибридизация
- •4.2. Sр2-Гибридизация
- •4.3. Sp-Гибридизация
- •5. Алканы
- •Гомологический ряд алканов. Число структурных изомеров
- •5.1. Физические свойства
- •5.2. Химические свойства
- •5.2.1. Галогенирование
- •Зависимость реакционной способности галогенов от энергии связи h–Hal
- •5.2.2. Нитрование
- •5.3.4. Декарбоксилирование карбоновых кислот
- •6.2. Плоскополяризованный свет. Оптическая активность
- •6.3. Строение молекул и оптическая активность
- •6.4. Обозначение конфигураций
- •7. Циклоалканы
- •7.1 Номенклатура. Изомерия
- •7.2. Физические свойства
- •7.3. Типы напряжения
- •7.4. Строение
- •Теплоты сгорания и энергии напряжения циклоалканов
- •7.4.1. Особенности пространственного строения некоторых циклоалканов
- •7.5. Химические свойства
- •7.6. Способы получения
- •8.1. Физические свойства
- •Физические свойства алкенов
- •8.2. Химические свойства
- •8.2.1. Присоединение галогенов
- •8.2.1.1. Механизм реакции
- •8.2.1.2. Реакционная способность галогенов в реакции АdЕ
- •8.2.2. Присоединение галогеноводородов
- •8.2.2.1. Механизм реакции
- •8.2.2.2. Направление электрофильного присоединения
- •8.2.2.3. Реакционная способность и селективность
- •8.2.2.4. Перегруппировка
- •Механизм реакции
- •8.2.3. Присоединение бромистого водорода в присутствии
- •1. Инициирование:
- •2. Рост цепи:
- •3. Обрыв цепи:
- •8.2.4. Присоединение серной кислоты
- •8.2.5. Гидратация алкенов. Присоединение спиртов
- •8.2.6. Гидроборирование алкенов
- •8.2.7. Алкилирование алкенов
- •8.2.8. Гидрирование. Теплота гидрирования
- •8.2.9. Теплота гидрирования и устойчивость алкенов
- •8.2.10. Окисление
- •8.2.11. Полимеризация алкенов
- •8.2.12. Реакция аллильного замещения. Галогенирование
- •8.3. Способы получения алкенов
- •9.1. Устойчивость сопряженных диенов
- •9.2. Химические свойства
- •9.2.1. Электрофильное присоединение
- •9.2.2. 1,2- И 1,4-Присоединение. Кинетический контроль, термодинамический контроль
- •9.2.3. Диеновый синтез. Реакция Дильса-Альдера
- •9.2.4. Полимеризация
- •9.3. Способы получения
- •10. Алкины
- •Характеристики химических связей в молекуле алкинов
- •10.1. Физические свойства
- •10.2. Химические свойства
- •10.2.1. Реакции присоединеня
- •10.2.1.1. Каталитическое гидрирование и восстановление
- •10.2.1.2. Реакции электрофильного присоединения Галогенирование
- •Гидрогалогенирование
- •Гидратация
- •10.2.1.3. Нуклеофильное присоединение
- •10.2.2. Кислотность алкинов
- •Константы кислотности некоторых соединений
- •10.2.3. Взаимодействие алкинов с карбонильными соединениями
- •10.2.4. Окисление алкинов
- •10.2.5. Радикальное присоединение бромоводорода
- •10.3. Способы получения
- •11. Арены
- •11.1. Сравнение свойств бензола со свойствами алкенов
- •11.2. Теплота гидрирования. Энергия резонанса
- •11.3. Строение бензола
- •11.4. Ароматичность
- •11.5. Физические свойства
- •Физические свойства аренов
- •11.6. Химические свойства
- •11.6.1. Электрофильное замещение
- •11.6.2. Свободнорадикальное замещение в боковой цепи аренов
- •11.6.3. Реакции окисления
- •11.7. Методы синтеза аренов
- •12.1. Влияние заместителей на реакционную способность бензольного кольца
- •12.2. Влияние заместителя на выбор места электрофильной атаки
- •13. Многоядерные ароматические соединения
- •13.1. Нафталин
- •13.2. Антрацен и фенантрен
- •14. Гетероциклические соединения
- •14.1. Пятичленные гетероциклы
- •14.1.1. Строение
- •14.1.2. Химические свойства
- •14.1.3. Способы получения
- •14.2. Пиридин
- •14.2.1. Строение пиридина
- •14.2.2. Химические свойства
- •14.3. Хинолин
- •15. Галогеналканы
- •15.1. Нуклеофильное замещение
- •15.1.1. Бимолекулярное нуклеофильное замещение
- •15.1.2. Мономолекулярное нуклеофильное замещение
- •15.1.3. Сравнение реакций sn 1 и sn 2
- •15.2. Реакции отщепления (элиминирование)
- •15.2.1. Бимолекулярное отщепление е2
- •15.2.2. Мономолекулярное отщепление е1
- •15.2.3. Сравнение реакций нуклеофильного замещения и элиминирования
- •15.3. Методы синтеза галогеналканов
- •16.2. Нуклеофильное замещение, протекающее через стадию образования дегидробензола, - отщепление - присоединение
- •16.3. Бимолекулярное нуклеофильное замещение sn2Ar
- •16.4. Ориентация при нуклеофильном замещении в ароматическом кольце
- •17. Магнийорганические соединения
- •17.1. Получение и строение магнийорганических соединений
- •17.2. Синтез спиртов и кислот
- •Библиографический список
- •Оглавление
- •Часть 1
8.2.10. Окисление
Окисление без разрыва углерод-углеродной связи.
Характер окисления алкенов зависит от используемого окислителя и условий реакции. Действие окислителя, который является электрофилом, всегда направлено в место повышенной электронной плотности - на атомы углерода, связанные двойной связью. При действии холодного раствора перманганата калия (слабый окислитель) разрывается только -связь и образуется две -связи с кислородом (реакция Вагнера).

Каталитическое окисление алкенов над серебром приводит к алкоксидам.
![]()
Действие другого мягкого окислителя - надкислоты - также приводит к образованию алкоксидов (реакция Н. А. Прилежаева).

Окисление с разрывом углерод-углеродной связи.
Под влиянием сильного окислителя ( КМnO4, Н ) разрывается не только -, но и -связь, разрушается углеродный скелет. В продуктах окисления все связи атомов углерода фрагмента >С=С<, кроме связей с соседними алкильными группами, насыщены кислородом:

Концевая группа =СН2 окисляется до оксида углерода и воды.

Озонолиз (озонирование и последующий гидролиз озонида) проводится в две стадии: присоединение озона по двойной связи с образованием озонида и гидролиз полученного озонида в присутствии восстанавливающего агента, например, цинковой пыли. Восстановитель необходим для связывания пероксида водорода, который может реагировать с альдегидами.


Озонолиз является методом определения структуры неизвестного алкена путём разрушения его на несколько меньших фрагментов, которые легко идентифицируются. Зная строение полученных альдегидов и кетонов, можно установить структуру исходного алкена.
Окисление алкенов в присутствии солей палладия (Вакер-процесс). Алкены окисляются кислородом в присутствии солей палладия и меди.
![]()
Этот способ является промышленным способом получения ацетальдегида. Окисление других алкенов идет по наименее гидрогенизированному атому углерода.
8.2.11. Полимеризация алкенов
Полимер - это макромолекула, состоящая из очень большого числа повторяющихся звеньев. Он образуется путем последовательного присоединения малых молекул, называемых мономерами.
Полимер, получаемый из одинаковых мономеров, называется гомополимером, а полученный из двух различных мономеров - сополимером или гетерополимером.
|
nA –A–A–A–A– или An |
|
гомополимер |
|
mB + nA –A–B–B–A–B–A–A–B–B–A– |
|
сополимер (случайное расположение) |
Полимер представляет собой смесь молекул с разной молекулярной массой, которая колеблется в определенных пределах. Полимеры содержат "концевые группы", которые отличаются от повторяющихся звеньев.
|
X |
| |
|
Инициатор полимеризации |
концевые группы | |
Концевые группы представляют собой незначительную часть полимера, поэтому их характер не учитывается при рассмотрении свойств полимера.
Катионная полимеризация
Катионная полимеризация протекает под действием кислот Льюиса (Н+, А1С13, BF3) по механизму, сходному с механизмом электрофильного присоединения по двойной связи. На первой стадии протон (или другая кислота) присоединяется к алкену, образуя карбокатион.
![]()
Затем другая молекула алкена вступает в реакцию за счет электронной пары двойной связи, и образуется карбокатион с более длинной цепью.
![]()
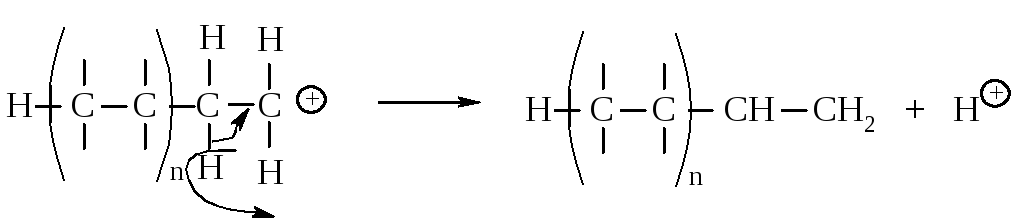
Далее процесс многократно повторяется и образуется карбокатион с высокой молекулярной массой. Эта цепь, в конце концов, может оборваться из-за разрушения катионного центра по какой-либо причине, например, из-за отрыва протона.
Изобутилен легко полимеризуется по катионному механизму, поскольку содержит электронодонорные алкильные группы.

Цепь полиизобутилена формируется таким образом, что на ее конце образуется наиболее стабильный карбокатион. Поэтому присоединение происходит упорядоченно - "голова к хвосту".
В условиях, близких к безводным, образуется полимер с очень длинной цепью. В присутствии серной кислоты с массовой долей 60 % изобутилен дает смесь димеров. Обрыв цепи происходит после соединения двух молекул изобутилена, промежуточный карбокатион теряет протон, отдавая его воде прежде, чем успеет прореагировать со следующей молекулой алкена. Вода выступает в роли основания, забирая протон у карбокатиона димера.

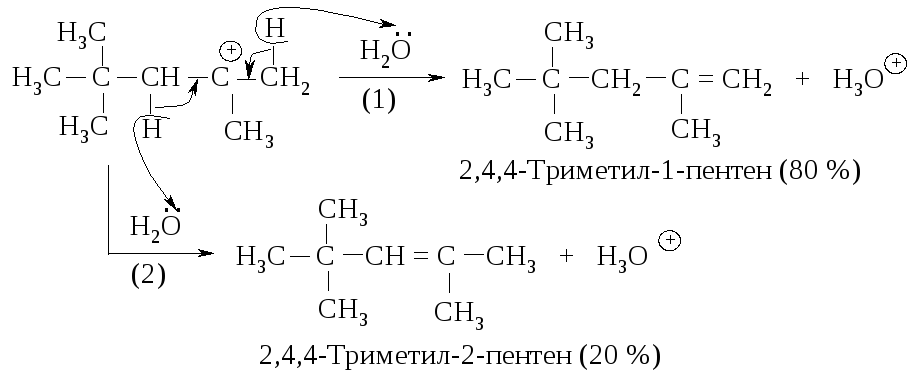
Можно ожидать, что 2,4,4-триметил-2-пентен благодаря центральному расположению двойной связи более устойчив, чем 2,4,4-триметил-1-пентен, имеющий концевую двойную связь. Однако в данном конкретном случае наличие объёмистой трет-бутильной и метильной групп в цис-положении у соседних атомов углерода создаёт пространственные затруднения образованию алкена:

Гидрирование 2,4,4-триметил-1-пентена и 2,4,4-триметил-2-пентена приводит к 2,2,4-триметилпентану (изооктану), используемому в качестве топлива для бензиновых двигателей внутреннего сгорания. Для изооктана принята стандартная антидетонационная характеристика (октановое число), равная 100 (октановое число н-гептана - 0).
Анионная полимеризация.
При анионном механизме полимеризация алкена инициируется атакой нуклеофильного реагента (NaNH2, NaOC4H9-н) по одному из концов двойной связи.

В этом примере амид-анион NH2– - нуклеофил атакует двойную связь акрилонитрила, возникающий карбанион стабилизирован делокализацией отрицательного заряда между атомом углерода и соседней электроноакцепторной группой –С N.
Если промежуточный анион окажется достаточно устойчивым, происходит его присоединение к другой молекуле алкена.

Растущая цепь может оборваться при любой реакции, которая приведёт к исчезновению отрицательного заряда на конце цепи.
Простые алкены, не имеющие электроноакцепторных заместителей, не присоединяют анионы и не образуют устойчивых карбанионов.
Свободнорадикальная полимеризация.
Этилен может полимеризоваться в присутствии пероксидов при высоком давлении и повышенной температуре.

Обрыв цепи происходит вследствие рекомбинации
![]()
или диспропорционирования радикалов.
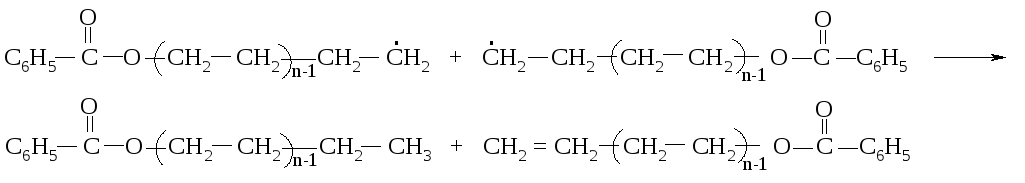
Полиэтилен содержит в углеводородной цепи 100-1000 звеньев этилена. Он обладает рядом ценных свойств и широко используется в производстве упаковочной плёнки, для изготовления большого числа изделий методом литья и формования.
При свободнорадикальной полимеризации несимметричного алкена растущий конец полимера представляет собой наиболее стабильный радикал, полимеризация идёт по типу “голова к хвосту”.

Пропилен и изобутилен не полимеризуются по свободнорадикальному механизму.
Координационная полимеризация осуществляется с помощью катализаторов Циглера-Натта. Наиболее распространённый из них - комплекс триэтилалюминия с хлоридом титана Al(C2H5)·TiCl4. С помощью таких катализаторов мономер внедряется в связь между металлом М и растущей полимерной цепью.
![]()
В полипропилене, который получают без этого катализатора, метильные группы расположены беспорядочно относительно основной полимерной цепи. Такой полимер называется атактическим.
Катализатор Циглера-Натта позволяет получать полипропилен, в котором метильные группы расположены упорядоченно по обеим сторонам полимерной цепи (синдиотактический).

Кроме того, можно получать полипропилен, в котором все метильные группы расположены по одну сторону от основной полимерной цепи (изотактический).

