
- •.Химия белков
- •1.2. Образование и номенклатура пептидов
- •1.3. Природные пептиды
- •1.4. Первичная структура белков
- •1.5. Конформация глобулярных белков. Вторичная, третичная, четвертичная структуры
- •1.6. Особенности структурной организации фибриллярных белков
- •1.7. Физико- химические свойства белков Общая характеристика физико-химических свойств белков
- •1.8. Номенклатура и общие принципы классификации белков
- •1. Классификация по форме белковых молекул (по степени асимметрии - отношению длинной оси молекулы к короткой).
- •2. Классификация по электрохимическим признакам.
- •3. Классификация по полярным признакам
- •4. Классификация по структурным признакам
- •II.Глобулины
- •Классификация сложных белков
- •1.9 Функции белков
1.2. Образование и номенклатура пептидов
Важнейшим свойством аминокислот является их способность к ковалентному взаимодействию за счет -амино- и -карбоксильной группы с образованием пептидной связи.

Пептидная связь -СО-NH- характеризуется планарностью все атомы, входящие в пептидную группу, находятся в одной плоскости. Транс-конфигурация пептидной связи является более предпочтительной, поскольку она менее стерически затруднена R-группами, чем цис-форма.
В результате реакции поликонденсации аминокислот образуются пептиды (полигетероаминокислоты). Пептиды полимерные соединения, структурной единицей которых являются аминокислоты.
![]()

Поскольку в образовании пептидных связей принимают участие лишь -амино и -карбоксильные группы, пептиды имеют неразветвленный характер. Скелет (хребет, остов) пептидов состоит из регулярно повторяющихся структурных элементов.
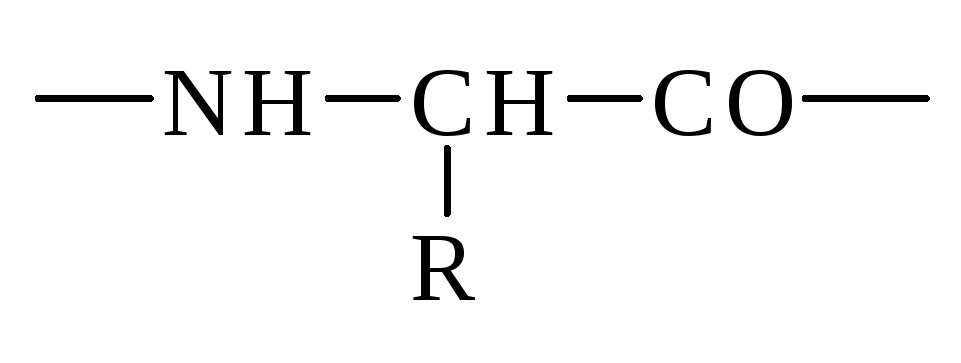
В пептидной цепи аминокислотные остатки расположены в определенной последовательности.
Пептиды обладают векторностью, пептидная цепь направлена от N-конца (начало цепи) к С-концу (конец цепи). N-конец это конец, на котором находится свободная -аминогруппа. С-конец это конец, на котором находится свободная -карбоксильная группа. В составе пептидной цепи N- и С-концы могут быть модифицированы. Векторность указывает направление, в котором происходит удлинение пептидов и белков при их синтезе. В соответствии с принятой векторностью осуществляется запись и чтение, входящих в состав пептидов, аминокислот.
Коэффициент поликонденсации характеризует число аминокислотных остатков, входящих в состав данного пептида. Условно принято, что пептиды, содержащие до 20 аминокислотных остатков, относятся к олигопептидам, среди которых различают ди-, три- тетрапептиды и т.д. Коэффициент поликонденсации полипептидов колеблется в диапазоне от 20 до 50.
Молекулярная масса пептидов зависит от характера и числа аминокислотных остатков. Поскольку средняя молекулярная масса одного аминокислотного остатка составляет около 110 Да, молекулярная масса пептидов варьирует в диапазоне от 200 до 6000Да.
НOМЕНКЛАТУРА ПЕПТИДОВ. Названия пептидов образуются в соответствии с последовательностью входящих в их состав аминокислотных остатков, начиная с N-конца. При этом в названиях всех аминокислотных остатков, за исключением последнего, меняется окончание на "ил", например : глицилаланил серилцистеин. Наряду с полным названием используются сокращенные обозначения. При этом аминокислотная последовательность пептидов обозначается, начиная с N-конца, с использованием трехбуквенных сокращенных названий аминокислот, например: глиаласерцис. При записи аминокислотной последовательности белков может быть использовано и однобуквенное обозначение аминокислот. В медицине и биологии используются тривиальные названия пептидов, отражающие место их синтеза, особенности биологического действия или другие обстоятельства. Например, один из пептидов задней доли гипофиза - вазопрессин получил свое название в связи со способностью повышать тонус сосудов.
