
- •Для сплава, диаграмма которого приведена на рисунке, характерно(Образование интерметаллического соединения) Желез реагирует с азотнокислым серебром с образованием(Серебра и нитрата железа (II))
- •Золото устойчиво на воздухе ввиду того, что(Имеет большой стандартный электродный потенциал)
- •К сетчатым полимерам не относятся(Резина)
- •Карбоцепным является полимер:(-сf2-)n –тефлон
- •Лавсан (терилен) образуется при взаимодействии(Диметилтерефталата с этиленгликолем) Латунь это сплав(Меди и цинка)
- •Медь реагирует с концентрированной азотной кислотой с образованием(Нитрата меди ( II ) , воды и двуокиси азота )
- •Наиболее активный металл : k , Au , Pt , Fe , Pb(k) Наиболее устойчивым полимером является:Тефлон ( Фторпласт-4)
- •Натуральный каучук это:Цис-полиизопрен
- •Оксид хрома (VI ) проявляет(Кислотные свойства)
- •Органические вмс содержат в своем составе(Углерод, водород, азот, кислород и серу)
- •Пенополиуретаны это(Вспененные полиуретаны)
- •При взаимодействии бромистоводородной кислоы (нВr) с двуокисью марганца образуются(Бром, вода, бромид марганца)
- •При гидролизе капрона образуются(Капроновая кислота)
- •При реакции поликонденсации формальдегида с фенолом не образуется(Резина)
- •Природным полимером является(Желатин)
- •Разбавленная серная кислота не реагирует с(Медью)
- •С водой при комнатной температуре взаимодействует(Калий)
- •Силиконы это(Полисилоксаны)
- •Старательским способом добывают(Золото)
- •Степень полимеризации это(Отношение среднего молекулярного веса полимера к молекулярному весу мономера)
Наиболее активный металл : k , Au , Pt , Fe , Pb(k) Наиболее устойчивым полимером является:Тефлон ( Фторпласт-4)
Наибольшее число молекул содержится при обычных условиях в 1 литре (воды;)
Наибольшей электропроводностью среди металлов обладают(Au, Ag, Cu)
Наибольшую склонность к образованию ионных связей проявляет элемент(F)
Наибольшую э.д.с. имеет гальванический элемент(Mg / Mg(NO3)2, 1M // AgNO3, 1M / Ag
Наименее прочная химическая связь (водородная)
Натуральный каучук это:Цис-полиизопрен
Не взаимодействуют с водой(Zn u Sn)
Не взаимодействуют с разбавленной соляной кислотой (Cu u Ag)
Не является электролитом (жидкий кислород.)
Неверное утверждение: (водород хорошо растворим в воде;)
Нейтральный раствор получается при гидролизе соли(ацетат аммония)
Некоторый элемент Z образует хлорид состава ZCl5. Наиболее вероятная формула его оксида: (Z2O5;)
Несолеобразующим является оксид: (N2O;)
Образец стали массой 5 г при сжигании в токе кислорода дал углекислый газ массой 0,1 г. Массовая доля углерода в стали составляет (0,55 %; )
Объем оксида углерода (IY) (н.у.), необходимый для получения Ca(HCO3)2 из 7,4 г Ca(OH)2, составляет (4,48 л;)
Одну из двух одинаковых порций гидрокарбоната натрия NaHCO3 прокалили, а затем обе порции раздельно обработали избытком хлороводородной кислоты. В каком случае и во сколько раз объем газа, образовавшегося при действии кислоты, больше? Правильным утверждением является следующее: (в случае обработки кислотой непрокаленной порции - в 2 раза;)
Оксид содержит 70,0 % железа. Формула этого оксида (Fe2O3)
Оксид хрома (VI ) проявляет(Кислотные свойства)
Оксид, образующий кислоту типа Н2ЭО3: (CO2; )
Опаснее всего подносить огонь к сосуду, в котором находится (смесь водорода с кислородом; )
Органические вмс содержат в своем составе(Углерод, водород, азот, кислород и серу)
Основная причина того, что температура кипения воды выше, чем температуры кипения сероводорода, теллуроводорода: (наличие сильных водородных связей между молекулами воды; )
Относятся к легким конструкционным следующие металлы (Mg u Al)
Отношение числа молекул электролита, распавшихся на ионы, к общему числу его молекул в растворе, называется(степенью диссоциации)
Парамагнитной является молекула(O2)
Пенополиуретаны это(Вспененные полиуретаны)
Первый закон термодинамики(Q = Δ U + A)
Пирамидальную форму имеет молекула(NH3)
Подберите коэффициенты в уравнении окислительно-восстановительной реакции K2SO3 + H2SO4 + KMnO4 MnSO4 + K2SO4 + H2O. В ответе укажите в уравнении сумму коэффициентов(21)
Подберите коэффициенты в уравнении окислительно-восстановительной реакции Na2Cr2O7 + H2SO4 + NaBr Cr2(SO4)3 + Br2 + Na2SO4 + H2O. В ответе укажите в уравнении сумму коэффициентов (29)
Подберите коэффициенты в уравнении окислительно-восстановительной реакции FeCl2 + HCl + KMnO4 - FeCl3 + Cl2 + MnCl2 + KCl + H2O. В ответе укажите в уравнении сумму коэффициенто(60)
Полиамиды получаются при взаимодействии(Диаминов с двухосновными кислотами)
Поликонденсационные ВМС могут быть получены реакциями взаимодействия(Гексаметилендиамина и адипиновой кислоты)
Полимерами не являются(Продукты взаимодействия щелочей с минеральными кислотами)
Получение хрома алюмотермическим методом выражается реакцией(Cr2О3 + 2А1 → 2Cr + Al2O3)
Понижение давления насыщенного пара растворителя над раствором пропорционально мольной доле растворённо вещества»(закон Рауля)
Последовательность заполнения молекулярных орбиталей в порядке возрастания их энергии σs<σs*<σz<πх=πу<πх*=πу*<σz* характерна для молекулы(O2)
Последовательность заполнения молекулярных орбиталей в порядке возрастания их энергии σs<σs*<πх=πу<σz <πх*=πу*<σz* характерна для молекулы(CO)
Превращения
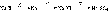 можно
осуществить с помощью следующих
реагентов (процессов): (X
- электролиз расплава, Y - H2O,
Z - H2SO4;)
можно
осуществить с помощью следующих
реагентов (процессов): (X
- электролиз расплава, Y - H2O,
Z - H2SO4;)
Превращения
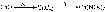 можно
осуществить с помощью следующих
реагентов: (X
- HСl, Y - AgNO3;
)
можно
осуществить с помощью следующих
реагентов: (X
- HСl, Y - AgNO3;
)
Превращения
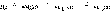 можно
осуществить с помощью следующих
реагентов: (X
- H2SO4,
Y
- Ba(NO3)2,
Z
- Na2CO3.
)
можно
осуществить с помощью следующих
реагентов: (X
- H2SO4,
Y
- Ba(NO3)2,
Z
- Na2CO3.
)
При взаимодействии 6,0 г металла с водой выделилось 3,36 л водорода (н.у.). Определите этот металл, если он в своих соединениях двухвалентен. Химическая формула металла(Ca).
