
- •Для сплава, диаграмма которого приведена на рисунке, характерно(Образование интерметаллического соединения) Желез реагирует с азотнокислым серебром с образованием(Серебра и нитрата железа (II))
- •Золото устойчиво на воздухе ввиду того, что(Имеет большой стандартный электродный потенциал)
- •К сетчатым полимерам не относятся(Резина)
- •Карбоцепным является полимер:(-сf2-)n –тефлон
- •Лавсан (терилен) образуется при взаимодействии(Диметилтерефталата с этиленгликолем) Латунь это сплав(Меди и цинка)
- •Медь реагирует с концентрированной азотной кислотой с образованием(Нитрата меди ( II ) , воды и двуокиси азота )
- •Наиболее активный металл : k , Au , Pt , Fe , Pb(k) Наиболее устойчивым полимером является:Тефлон ( Фторпласт-4)
- •Натуральный каучук это:Цис-полиизопрен
- •Оксид хрома (VI ) проявляет(Кислотные свойства)
- •Органические вмс содержат в своем составе(Углерод, водород, азот, кислород и серу)
- •Пенополиуретаны это(Вспененные полиуретаны)
- •При взаимодействии бромистоводородной кислоы (нВr) с двуокисью марганца образуются(Бром, вода, бромид марганца)
- •При гидролизе капрона образуются(Капроновая кислота)
- •При реакции поликонденсации формальдегида с фенолом не образуется(Резина)
- •Природным полимером является(Желатин)
- •Разбавленная серная кислота не реагирует с(Медью)
- •С водой при комнатной температуре взаимодействует(Калий)
- •Силиконы это(Полисилоксаны)
- •Старательским способом добывают(Золото)
- •Степень полимеризации это(Отношение среднего молекулярного веса полимера к молекулярному весу мономера)
CrO3 проявляет(Окислительые и кислотные свойства)
π-связь образуется при перекрывании(р-орбиталей, оси которых параллельны)
Активность металлов Pt, Au, Na, Fe, Pb, уменьшается в порядке(Na, Fe, Pb, Au, Pt)
Алюминий устойчив на воздухе ввиду того , что(Покрыт с поверхности устойчивой оксидной пленкой)
Алюминий получают в промышленности(Электролизом глинозема в расплаве криолита)
Амфотерными свойствами обладают металлы(Be u Al)
Атмосферная коррозия лужёного железа (покрытого тонким слоем олова) описывается уравнениями(А: Fe – 2ē → Fe2+ K: 2H2O + O2 +4ē → 4OH- )
Атом кальция имеет электронную конфигурацию: (1s22s22p63s23p64s2; )
Атомы изотопов одного элемента отличаются (числом нейтронов; )
Ацетилен объемом 67,2 л при н.у. составляет следующее количество вещества(3моль.)
Бериллий в отличии от элементов второй группы элементов таблицы Д.И. Менделеева проявляет(Амфотерные свойства)
В 250 миллилитрах раствора серной кислоты, имеющего концентрацию 1 моль/л. Содержится(24,5 г кислоты)
В алюмотермическом процессе из оксида железа (III) массой 32 г образовалось железо массой 20 г. Практический выход железа от теоретического составил (89,3%;)
В атоме не может быть …… электронов с одинаковым набором четырех квантовых чисел(двух)
В воде растворили 11,2 г гидроксида калия. Объем раствора довели до 257 мл. Какова молярная концентрация раствора? (0,78 моль/л; )
В водном растворе кислую реакцию среды имеет (NH4Cl; )
В молекуле аммиака NH3 число несвязывающих электронных пар равно(1)
В молекуле аммиака NH3 число связывающих электронных пар равно(3)
В невозбужденном состоянии число электронов на четвертом энергетическом уровне равно пяти у(мышьяка)
В процессе электролиза водного раствора NaClO4 на электродах выделятся следующие проду(H2, O2; )
В реакции, протекающей по схеме Cr2S3 + KNO3 K2CrO4 + K2SO4 + NO, окислению подвер элементы: (S, Cr;)
В реакционной системе в равновесии находятся Чтобы сместить равновесие реакции вправо, необходимо (увеличить давление в системе;)
В
результате превращений
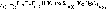 образуется конечный продукт (X3)
состава (Cr2(SO4)3
. )
образуется конечный продукт (X3)
состава (Cr2(SO4)3
. )
В ряду молекул HCl - HBr - HI полярность ковалентной связи (уменьшается; )
В ряду находятся только кислотные оксиды: (SO3, CO2, P2O5;)
В ряду увеличивается восстановительная способность галогенидов: (KF, KCl, KBr, KI. )
В стакан с 60 г 10%-ного раствора хлороводородной кислоты насыпали 9,2 г железных опилок и оставили стоять без доступа воздуха. На следующий день обнаружили, что в стакане образовалось вещество состава (FeOHCl; )
В трех пробирках находятся концентрированные растворы кислот: H2SO4, HCl, HNO3. Реактив, с помощью которого можно распознать все кислоты: (Zn;)
В трех пробирках находятся растворы хлорида калия, бромида калия и иодида калия. Реактив, с помощью которого можно распознать все соли: (AgNO3;)
В узлах кристаллической решетки металлов находятся(положительно заряженные ионы металла)
В уравнении реакции K2O + ZnO сумма коэффициентов равна (3; )
В уравнении реакции SO3 + Al2O3 сумма коэффициентов равна (5;)
В условиях постоянства температуры и давления химическая реакция не может протекать самопроизвольно, если(Δ G> 0,)
В химических реакциях металлы выступают в роли(восстановителей)
В хлориде аммония отсутствуют связи(ковалентные неполярные)
В частице Na+ содержится протонов (11).
В эвдиометре взорвали смесь, состоящую из 4 мл водорода и 6 мл кислорода. Газ, оставшийся после взрыва, представляет собой _____ (O2, ) и имеет объем (4 мл; )
Величина
I
в процессе A(атом)
+ I
A+
+ 1 e
(потенциал
ионизации)
Верное утверждение: (кислород тяжелее воздуха.)
Вещества, в водных растворах которых растворяется Al(OH)3: (KOH, H2SO4; )
Вещества, которые можно использовать для устранения общей жесткости воды: (Na3PO4, Na2CO3; )
Вещество, которое выпадает в осадок при сливании концентрированных водных растворов Na2S и AlCl3: (Al(OH)3;)
Вещество, которое при растворении в воде дает слабощелочную реакцию: (NH3.)
Вещество, не взаимодействующее с оксидом фосфора (V): (оксид углерода (IV); )
Вещество, с которым взаимодействует сульфид натрия с образованием PbS: (Pb(NO3)2; )
Веществом, для которого стандартная энтальпия образования равна нулю, является(кислород)
Внутренняя энергия системы в экзотермических реакциях изменяется следующим образом(уменьшается)
Водород в промышленности получают следующим способом: (конверсией метана; )
Водород проявляет отрицательную степень окисления в соединении: (NaH; )
Водородный показатель (рН) раствора гидроксида калия, имеющего концентрацию 0,01 моль/л, равен(12)
Водородный показатель (рН) 0,01 М раствора азотной кислоты равен(2)
Возможные валентности серы с точки зрения строения атома(2, 4, 6)
Возможные валентности хлора с точки зрения строения атома(1,3,5,7)
Возможным является процесс, описываемый уравнением (Zn + CuSO4 → ZnSO4 + Cu)
Временная жесткость воды обусловлена присутствием в воде (Ca(HCO3)2, Mg(HCO3)2; )
Все аналитические методы основаны на получении и измерении аналитического сигнала, т.е. любого проявления химических или физических свойств вещества. Аналитическим сигналом в кислотно-основном титровании является(Окраска индикатора)
Все возможные значения магнитного квантового числа для d-орбиталей(–2,-1,0,1,2,3)
Все возможные значения магнитного квантового числа для p-орбиталей(–1,0,1)
Все связи ковалентные неполярные в молекуле(О2)
Выделение водорода будет наблюдаться в реакции: (Fe + H2SO4 (разб.)
Выражение «раствор с массовой долей соли 3%» означает(в 100 г раствора содержится 3 г соли)
Галоген, в наибольшей степени проявляющий окислительные свойства: (F2).
Гальванический элемент Вольта состоит из цинковой и медной пластин, опущенных в раствор серной кислоты. На электродах этого гальванического элемента протекают следующие процессыА: Zn – 2 ē → Zn2+ K: 2H+ + 2 ē → H2)
Геометрическая форма молекулы аммиака NH3(пирамидальная)
Геометрическая форма молекулы метана СН4(тетраэдрическая)
Гетероцепным полимером является:(-СН2-СН2О-)n-9полиэтиленоксид)
Даны простые вещества: сажа, озон, графит, кислород, алмаз, красный фосфор. Всего в состав этих веществ входит следующее количество химических элементов: (3)
Две π-связи имеет молекула(СО2)
Двойную связь имеет молекула(O2)
Для осушки аммиака его надо пропустить через (NaOH;)
Для протекторной защиты железа от коррозии в нейтральной водной среде применяется(цинк)
Для реакции, протекающей в стандартных условиях, известны значения энтальпии образования исходных веществ и продуктов реакции:PtCl2 + Cl2 = PtCl4 Δ H0обр -118,0 -226,0 кДж/мольИзменение энтальпии в указанной реакции составляет(ΔН0 реакции = -108 кДж)
Для реакции, протекающей в стандартных условиях, известны значения энтропии исходных веществ и продуктов реакции:N2(г) + 3H2(г) = 2NH3(г)S0298 199,9 130,5 192,6 Дж/моль ∙ К Изменение энтропии в указанной реакции составляет(–206,2 Дж/К)
Для реакции, протекающей в стандартных условиях, известны стандартные энтальпии образования исходных веществ и продуктов реакции:СО(г) + 3Н2(г) = СН4(г) + Н2О(г) Н0обр. –110,6 -74,8 -241,2 кДж/мольИзменение энтальпии в указанной реакции составляет(–205,4 кДж)
Для реакции, протекающей в стандартных условиях, известны значения энтальпии образования исходных веществ и продуктов реакции:2NO2 = N2O4 ΔH0обр. 33,9 9,4 кДж/моль Изменение энтальпии указанной реакции составляет(ΔH0реакции= -58,4 кДж)
Для реакции, протекающей в стандартных условиях, известны значения энтальпии образования исходных веществ и продуктов реакции:С2Н2 + Н2 = С2Н4Δ Н0 обр. 226,8 52,3 кДж/моль Изменение энтальпии в указанной реакции составляет(-174,5 кДж/моль)
Для реакции, протекающей в стандартных условиях, известны значения энтальпии образования исходных веществ и продуктов реакцииСО + Сl2 = СОСl2 ΔН0обр. 110,6 -220,3 кДж/моль Изменение энтальпии в данной реакции составляет(-330,9 кДж)
Для реакции, протекающей в стандартных условиях, известны значения энтальпии образования исходных веществ и продуктов реакции:СО2 + Н2 = СО + Н2ОΔН0обр. –393,8 -110,6 -286,0 кДж/моль Изменение энтальпии в указанной реакции составляет(–2,8 кДж)
Для реакции, протекающей в стандартных условиях, известны значения энтальпии образования исходных веществ и продуктов реакции:4НСl + О2 = 2Н2О + 2Сl2ΔН0обр. –92,5 -242,0 кДж/мольИзменение энтальпии в ходе данной реакции составляет(–114,0 кДж)
Для сплава, диаграмма которого приведена на рисунке, характерно(Образование интерметаллического соединения) Желез реагирует с азотнокислым серебром с образованием(Серебра и нитрата железа (II))
Зависимость осмотического давления раствора от концентрации растворённого вещества описывается законом(Вант-Гоффа)
Золото устойчиво на воздухе ввиду того, что(Имеет большой стандартный электродный потенциал)
Из атомов двух элементов: водорода и гелия - меньший радиус имеет (атом гелия;)
Из перечисленных процессов: к экзотермическим относятся (а, в, г; )
Из приведенных ниже солей гидролизу не подвергается (KNO3 .)
Из приведённых ниже солей гидролизу не подвергается(сульфат натрия)
Из приведённых ниже солей гидролизу не подвергается(хлорид калия)
Из приведённых ниже солей гидролизуется одновременно по катиону и аниону(ацетат аммония)
Из приведённых ниже солей по аниону гидролизуются(сульфид натрия)
Из приведённых ниже солей по катиону гидролизуются(ZnCl2)
Из пяти групп веществ выберите ту, которая содержит только сильные электролиты(K2SO4, HNO3, NaOH)
Из четырех металлов Li , Na , K , Rb наименьший потенциал ионизации имеет(Rb)
Из четырех металлов Mg , Ca , Sr , Ba наименьшую электроотрицательность имеет (Ba)
Изменение энтальпии в данной реакции равно +420,4 кДж, изменение энтропии в реакции равно +1033.6 Дж/К. Рассчитать изменение свободной энергии Гиббса.(+112,3 кДж)
Изотоп одного из элементов не содержит нейтронов. Речь идет о химическом элементе(H).
Изотопами являются(40Ca и 42Ca)
Имеется раствор смеси солей: Na2SO4 и CuSO4. При электролизе этого раствора на катоде будут выделяться следующие вещества в указанной последовательности: (Cu, H2; )
Имеются газы: H2S, Cl2, SO2, CO2. Реактив, являющийся лучшим поглотителем всех этих газов: (NaOH.)
Ион Al3+ имеет электронную конфигурацию: (1s22s22p6; )
Ионную кристаллическую решетку имеет (фторид натрия;)
Ионы Cl- образуются при диссоциации соли(хлорид калия)
К какому семейству элементов относится алюминий: (к семейству p-элементов;)
К сетчатым полимерам не относятся(Резина)
Какие орбитали имеют форму гантели(p-орбитали)
Какова должна быть массовая доля хлороводорода в соляной кислоте, чтобы в ней на 10 моль воды приходился 1 моль хлороводорода? (16,86%; )
Какое электронное состояние возможно(5d 6)
Какую массу медного купороса CuSO4 · 5H2O и воды надо взять для приготовления 40 кг 20%-ного раствора сульфата меди (II)? (12,5 кг CuSO4 · 5 H2O, 27,5 кг H2O.)
Карбонатная жесткость проявляется в результате следующих природных процессов: (при взаимодействии известковой почвы с почвенной и дождевой водой, насыщенной атмосферным диоксидом углерода (IV);)
Карбоцепным является полимер:(-сf2-)n –тефлон
Качественный состав хлорида железа (III) можно установить, используя два раствора, содержащие соответственно ионы (CNS- и Ag+; )
Кислород проявляет положительную степень окисления в соединении(OF2)
Кислота, которую нельзя хранить ни в обычной посуде, ни в посуде из кварцевого стекла: (HF. )
Кислый раствор получается при гидролизе соли(нитрат железа (III))
Ковалентную неполярную связь имеет(Н2)
Ковалентную полярную связь имеет(НСl)
Количественно процессы электролиза подчиняются законам(Фарадея)
Количество вещества и масса гидроксида натрия, необходимые для нейтрализации 14,6%-ного раствора хлороводородной кислоты массой 300 г, равны соответство (1,2 моль, 48 г; )
Количество протонов, нейтронов и электронов в атоме 52Cr (24,28,24)
Количество электронов, находящихся на внешнем энергетическом уровне атома кислорода: (6).
Концентрированная серная кислота не взаимодействует со следующими металлами(Ag u Pt)
Координационное число в кристаллической решетке металлов может быть равным(8 и 12)
Кратность связи в молекуле N2 равна(3)
Кратность связи в молекуле Н2 равна(1)
Кратность связи в молекуле О2 равна(2)
Кристаллическая решетка алмаза (атомная;)
Кристаллогидратами называются (твердые вещества, в состав которых входит химически связанная вода; )
