
- •1. Основные понятия химии: атом, молекула, химический элемент, протон, нейтрон, электрон.
- •2. Изотопы, изотоны, аллотропия.
- •3. Стехиометрия. Основны законы стехиометрии.
- •5. Дальтониды и бертоллиды.
- •6. Атомная масса, относительная атомная масса, связь между атомной и молярной массой.
- •7. Молекулярная масса. Моль. Молярная масса.
- •8. Число Авогадро. Связь между колличеством вещества, массой, объемом, и числом атомов.
- •16. Строение атома: планетарная модель атома Резерфорда.
- •19. Характеристика квантовых чисел.
- •21. Правило Хунда.
- •22. Принцип наименьшей энергии (правило Клечевского)
- •25. Σ, π, δ связь
- •26. Ковалентная, ионная, металлическая и водородная связь.
- •27. Виды и номенклатура комплексных соединений.
- •28. Комплексообразователи и лиганды.
- •Классификация дисперсных систем по агрегатным состояниям фаз.
- •36. Механизм образования жидких растворов. Сольватация и гидратация.
- •37. Автопротолиз воды. Водородный показатель. Кислотность среды.
- •48. Устройство свинцово- кислотного аккумулятора.
16. Строение атома: планетарная модель атома Резерфорда.
Рассеяние
отдельных α-частиц на большие углы
Резерфорд
объяснил тем, что положительный заряд
в атоме не распределен равномерно в
шаре радиусом 10-10м,
как предполагали ранее, а сосредоточен
в центральной части атома (атомном
ядре) в области значительно меньших
размеров. Расчеты Резерфорда показали,
что для объяснения опытов по рассеянию
α-частиц нужно принять радиус атомного
ядра равным примерно 10-15м.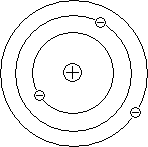
Резерфорд
предположил, что атом устроен подобно
планетарной системе. Как вокруг Солнца
на больших расстояниях от него обращаются
планеты, так электроны в атоме обращаются
вокруг атомного ядра. Радиус круговой
орбиты самого далекого от ядра электрона
и есть радиус атома. Такая модель атома
была названа планетарной
моделью.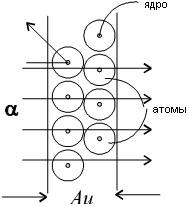
Планетарная модель атома объясняет основные закономерности рассеяния заряженных частиц.
Так как большая часть пространства в атоме между атомным ядром и обращающимися вокруг него электронами пуста, быстро заряженные частицы могут почти свободно проникать через довольно значительные слои вещества, содержащие несколько тысяч слоев атомов.
При столкновениях с отдельными электронами быстрые заряженные частицы испытывают рассеяние на очень большие углы, так как масса электрона мала. Однако в тех редких случаях, когда быстрая заряженная частица пролетает на очень близком расстоянии от одного из атомных ядер, под действием силы электрического поля атомного ядра может произойти рассеяние заряженной частицы на любой угол до 180°.
17. Строение атома: постулаты Бора, модель атома по Бору.
Датский физик Нильс Бор (1885-1962) обосновал планетарную модель атома Резерфорда. Свои представления об особых свойствах атомов (устойчивости атома и спектральных закономерностей его излучения) Бор сформулировал в виде постулатов следующего содержания:
-
Электрон в атоме можеь находиться только в определенных устойчивых состояниях, называемых стационарными или квантовыми, каждому из которых соответствует определенная энергия En. В этих состояниях атом не излучает электромагнитных волн.
-
При переходе атома из одного стационарного состояния в другое испускается или поглощается квант энергии ΔE = hν.
-
Электрон в атоме, не теряя энергии, двигается по определённым дискретным круговым орбитам, для которых момент импульса квантуется. Пребывание электрона на орбите определяет энергию этих стационарных состояний
Все стационарные состояния, кроме одного, являются стационарными лишь условно. Бесконечно долго каждый атом может находиться лишь в стационарном состоянии с минимальным запасом энергии. Это состояние атома называется основным. Все остальные стационарные состояния атома называются возбужденными.
18.Квантово-механическая модель атома Современная модель атома является развитием планетарной модели Бора-Резерфорда. Согласно современной модели, ядро атома состоит из положительно заряженных протонов и не имеющих заряда нейтронов и окружено отрицательно заряженными электронами. Однако представления квантовой механики не позволяют считать, что электроны движутся вокруг ядра по сколько-нибудь определённым траекториям (неопределённость координаты электрона в атоме может быть сравнима с размерами самого атома). Химические свойства атомов определяются конфигурацией электронной оболочки и описываются квантовой механикой. Положение атома в таблице Менделеева определяется электрическим зарядом его ядра (то есть количеством протонов), в то время как количество нейтронов принципиально не влияет на химические свойства; при этом нейтронов в ядре, как правило, больше, чем протонов (см.: атомное ядро). Если атом находится в нейтральном состоянии, то количество электронов в нём равно количеству протонов. Основная масса атома сосредоточена в ядре, а массовая доля электронов в общей массе атома незначительна (несколько сотых процента массы ядра). Массу атома принято измерять в атомных единицах массы, равных 1⁄12 от массы атома стабильного изотопа углерода 12C.
(В 1924г. французский физик Луи де Бройль высказал предположение, что электрон обладает не только свойствами частицы, но и свойствами волны (корпускулярно-волновая двойственность электрона). Согласно уравнению волны де Бройля:
![]() ,
,
(где
h -
постоянная Планка (![]() [Дж.с])),
частице с массой m,
движущейся со скоростью v
соответствует волна длиной λ.
[Дж.с])),
частице с массой m,
движущейся со скоростью v
соответствует волна длиной λ.
Таким образом, любой частице соответствует волна определенной длины, в том числе и потокам электронов соответствует волновой процесс, что было подтверждено экспериментально: потоки электронов, проходя через кристаллическую решетку, подвергаются дифракции, и дифракционная картина соответствует волновому процессу с длиной волны λ. Было доказано, что электрон обладает свойствами и частицы и волны. Корпускулярно-волновое представление об электроне позволяет утверждать, что электрон может находиться в любом месте атома, но вероятность его пребывания неодинакова, т.е. положение его неопределенно.)
(Современная квантово-механическая теория строения атома складывалась постепенно. Делались новые открытия, совершенствовался математический аппарат и, соответственно, выкристаллизовывалась модель атома. Современная квантово-механическая теория гласит, что атом любого элемента имеет сложную структуру. Положительная часть атома /положительный заряд/ сосредоточена в ядре. Отрицательную часть составляют электроны, которые находятся в беспрерывном движении.)
