
- •Варианты контрольных заданий
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Вычислите реакции, протекающей по уравнению, используя значения стандартных теплот образования и абсолютных стандартных энтропий веществ: .
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Составьте молекулярные и ионные уравнения реакций, протекающих при смешивании растворов: а) и ; б) и ; в) и .
- •Составьте уравнения электролитической диссоциации следующих электролитов: . Запишите выражения констант равновесия для слабых электролитов.
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Составьте молекулярные уравнения по ионно-молекулярным: ;
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Вычислите реакции, протекающей по уравнению, используя значения стандартных теплот образования и абсолютных стандартных энтропий веществ: .
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Напишите ионно-молекулярные уравнения реакций:
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Составьте молекулярные уравнения по ионно-молекулярным: ;
- •Составьте уравнения электролитической диссоциации следующих электролитов: . Запишите выражения констант равновесия для слабых электролитов.
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Составьте уравнения электролитической диссоциации электролитов . Объясните, какой из них легче распадается на ионы и почему. Запишите выражение для константы равновесия слабых электролитов.
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
- •Составьте уравнения электролитической диссоциации следующих электролитов: . Запишите выражения констант равновесия для слабых электролитов.
- •Напишите ионно-молекулярные уравнения реакций:
- •Напишите ионно-молекулярные уравнения реакций:
- •Составьте уравнения электролитической диссоциации следующих электролитов: . Запишите выражения констант равновесия для слабых электролитов.
- •Термодинамические свойства некоторых соединений
-
При какой температуре наступит равновесие в системе:
 ;
;
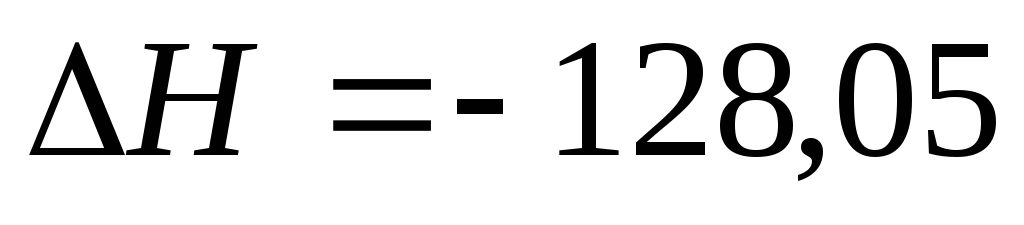 кДж?
кДж? -
Как изменится скорость прямой реакции
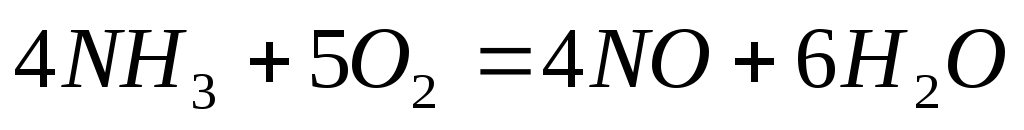 если объем газовой смеси уменьшить в
3 раза?
если объем газовой смеси уменьшить в
3 раза? -
Установите, во сколько раз уменьшится или увеличится равновесная концентрация оксида углерода в реакции:
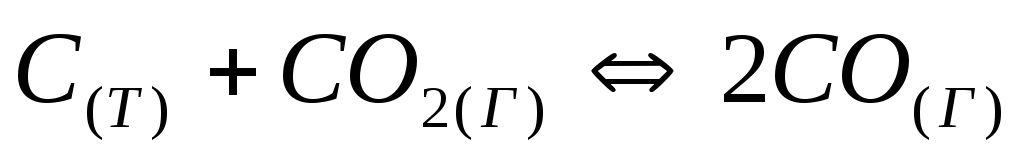 при увеличении значения равновесной
концентрации диоксида углерода в 3
раза.
при увеличении значения равновесной
концентрации диоксида углерода в 3
раза. -
Какой объем 0.1 н.
 можно приготовить из 1,7 л раствора
азотной кислоты с массовой долей 25%
(ρ=1.18г/см3)?
можно приготовить из 1,7 л раствора
азотной кислоты с массовой долей 25%
(ρ=1.18г/см3)? -
Составьте молекулярные уравнения реакций, представленных следующими ионными уравнениями:
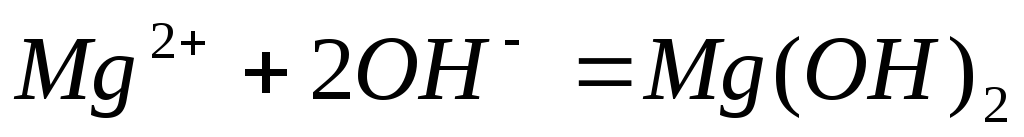 ;
;
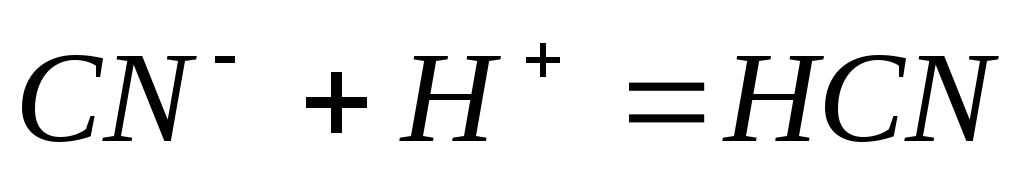 .
. -
Температура кипения эфира 34,6ºС, а его эбуллиоскопическая константа равна 2,16º. Вычислите молекулярную массу бензойной кислоты, если известно, что 5%-ный раствор этой кислоты в эфире кипит при 35,53ºС.
-
Составьте уравнения электролитической диссоциации следующих электролитов:
 .
. -
Составьте уравнения гидролиза в ионно-молекулярной и молекулярной форме для следующих солей: и . Укажите рН среды.
Вариант 16.
-
Вычислите теплоту образования
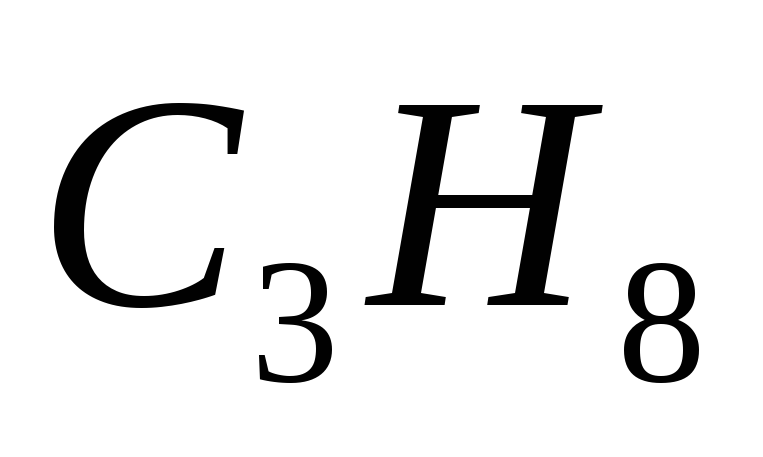 , если известно, что при сгорании 11г его
выделилось 552 кДж.
, если известно, что при сгорании 11г его
выделилось 552 кДж. -
Вычислите температуру, при которой система находится в равновесии, считая, что
 и
и
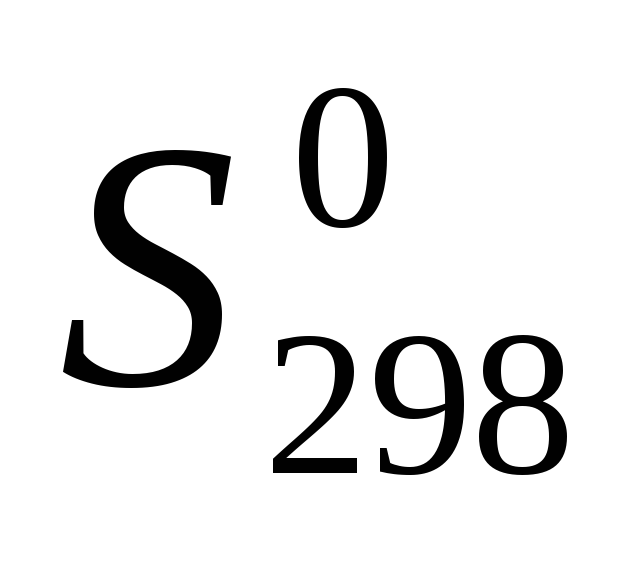 не зависят от температуры:
не зависят от температуры:
![]()
-
При повышении температуры на 30°С скорость химической реакции увеличилась в 64 раза. Вычислите, во сколько раз увеличится скорость этой реакции при повышении температуры на каждые 10°.
-
Как увеличить выход продуктов следующих реакций:
![]()
![]()
за счет изменения концентрации реагентов, давления, температуры?
-
Сколько граммов 30%-ного (по массе) раствора
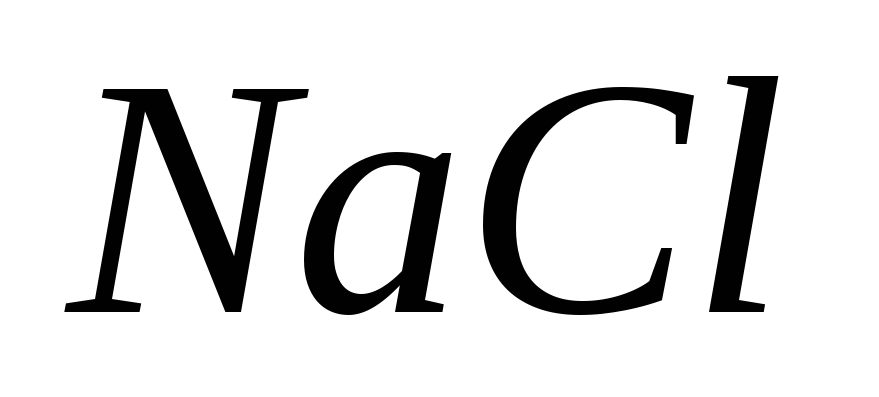 нужно добавить к 300 г воды, чтобы получить
10%-ный раствор соли?
нужно добавить к 300 г воды, чтобы получить
10%-ный раствор соли? -
Закончите молекулярные и составьте ионно-молекулярные уравнения процессов, проходящих по схемам:
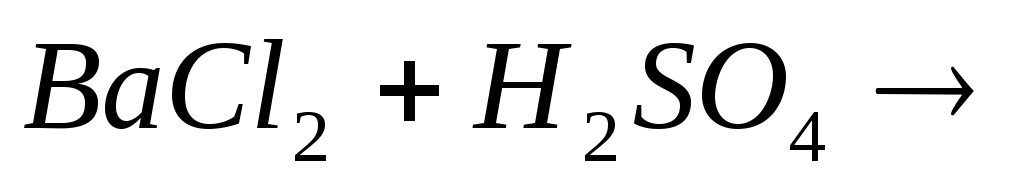 …;
…;
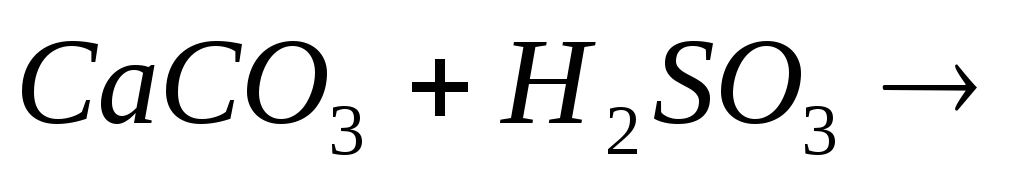 ….
…. -
Раствор, содержащий 0,512 г вещества в 100 г бензола, кристаллизуется при 5,296ºС. Вычислите мольную массу вещества, если известно, что температура кристаллизации бензола составляет 5,5ºС, а криоскопическая константа равна 5,1º
-
Составьте уравнения электролитической диссоциации следующих электролитов: . Запишите выражения констант равновесия для слабых электролитов.
-
Какие из солей
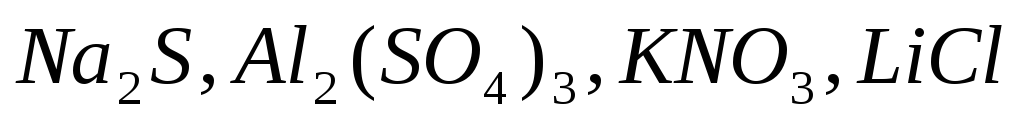 подвергаются гидролизу? Составьте
ионно-молекулярные и молекулярные
уравнения гидролиза, укажите значение
рН растворов этих солей.
подвергаются гидролизу? Составьте
ионно-молекулярные и молекулярные
уравнения гидролиза, укажите значение
рН растворов этих солей.
Вариант 17.
-
Процесс выражается термохимическим уравнением
![]()
Вычислите теплоту сгорания этилена, если теплота его образования
равна 52,3 кДж/моль. Каков тепловой эффект сгорания 5 л этилена?
-
Вычислите
 образования
метана, этана и аммиака, исходя из
значений
образования
метана, этана и аммиака, исходя из
значений
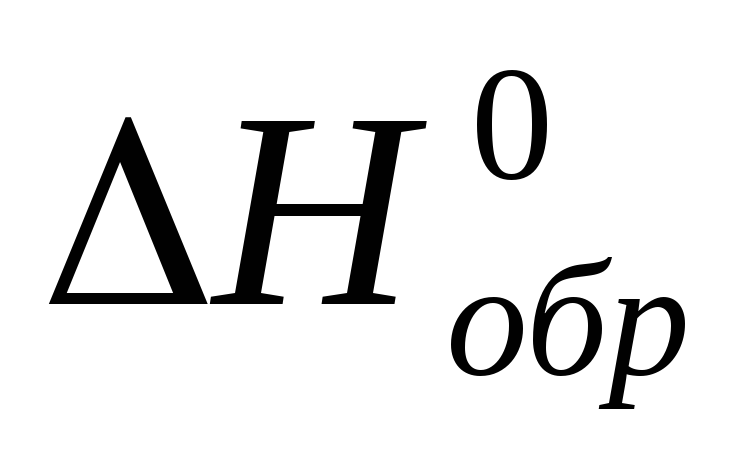 и изменения энтропии
и изменения энтропии
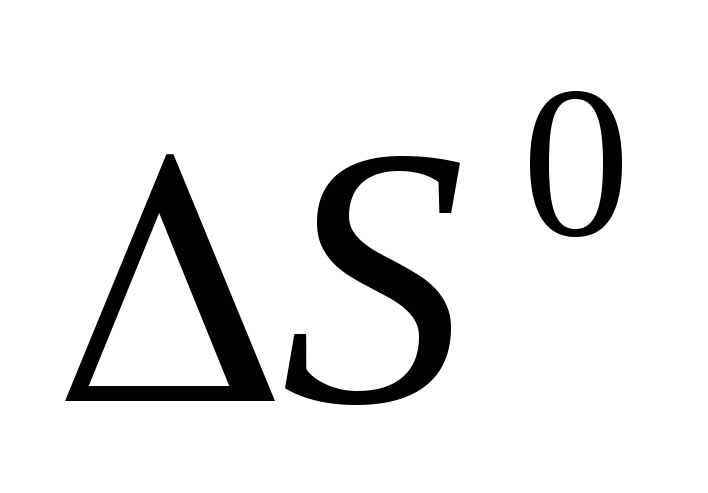 .
Полученные величины сравните со
справочными данными.
.
Полученные величины сравните со
справочными данными. -
Рассчитайте температурный коэффициент реакции, если при нагревании системы от 40° до 80° скорость возросла в 64 раза.
-
Вычислите константу равновесия для следующей реакции
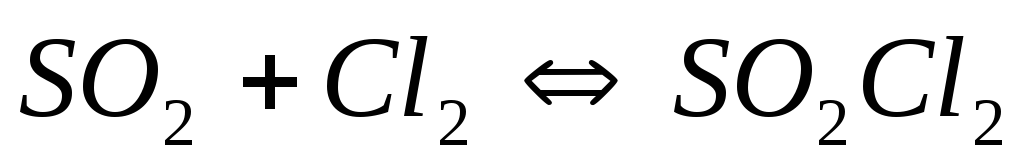 , если при некоторой температуре
образовалось 2,3 моль
, если при некоторой температуре
образовалось 2,3 моль
 ,
а исходные концентрации двуокиси серы
и хлора соответственно составляли 6,2
моль/л и
5,5 моль/л.
,
а исходные концентрации двуокиси серы
и хлора соответственно составляли 6,2
моль/л и
5,5 моль/л. -
Рассчитайте молярную концентрацию эквивалента концентрированной соляной кислоты (плотность 1,18 г/см3), содержащей 38 % (масс.)
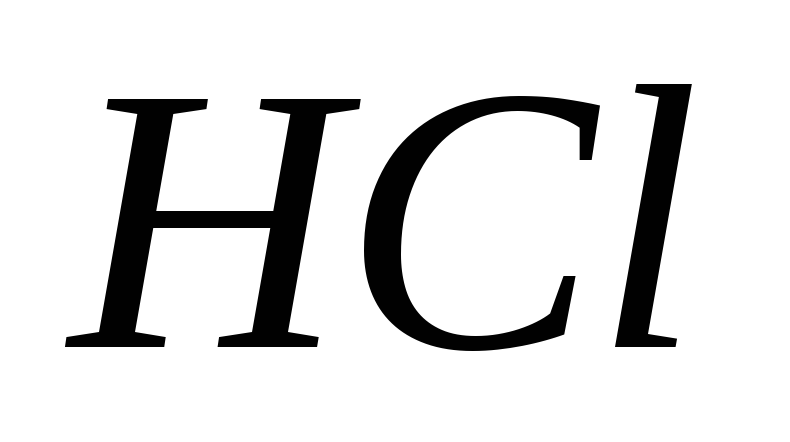 .
. -
Составьте по три молекулярных уравнения реакций, которые выражаются ионно-молекулярными уравнениями:
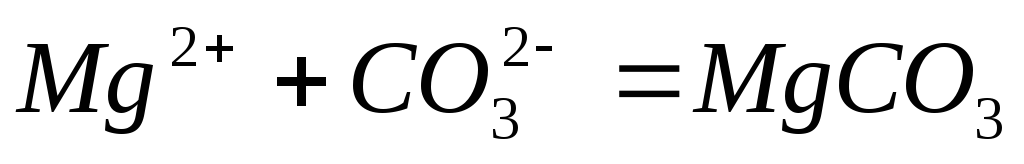 ;
;
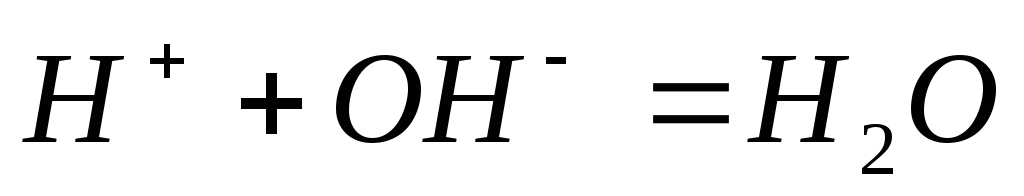 .
. -
Разбавленный раствор сахара
 кипит при 100,065ºС. Вычислите осмотическое
давление раствора при 0ºС, приняв
плотность раствора равной единице.
кипит при 100,065ºС. Вычислите осмотическое
давление раствора при 0ºС, приняв
плотность раствора равной единице. -
Составьте уравнения полной электролитической диссоциации для сильных электролитов:
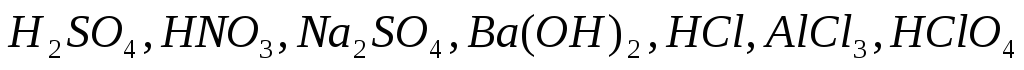 .
. -
Какие из солей
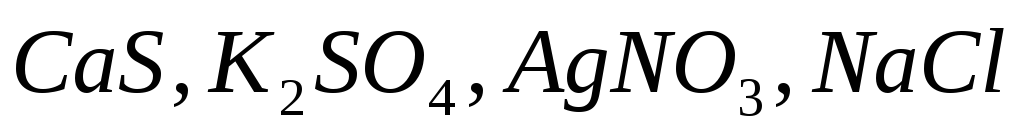 подвергаются гидролизу? Составьте
ионно-молекулярные и молекулярные
уравнения гидролиза, укажите значение
рН растворов этих солей.
подвергаются гидролизу? Составьте
ионно-молекулярные и молекулярные
уравнения гидролиза, укажите значение
рН растворов этих солей.
Вариант 18.
-
Вычислите теплоту образования карбида кальция
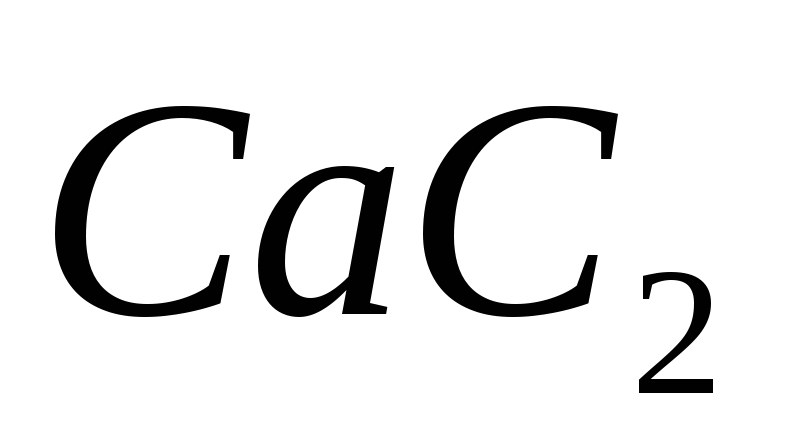 ,
пользуясь термохимическим уравнением:
,
пользуясь термохимическим уравнением:
 ;
;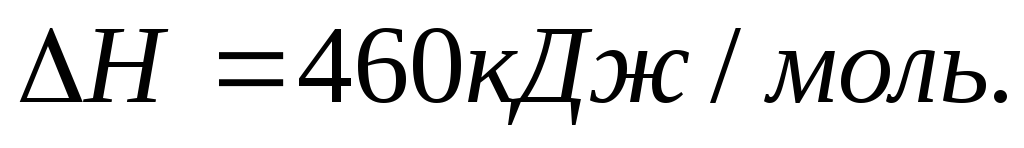
-
Вычислите энергию Гиббса следующих реакций и определите, в каком направлении они будут протекать, если все вещества взяты при стандартных условиях:
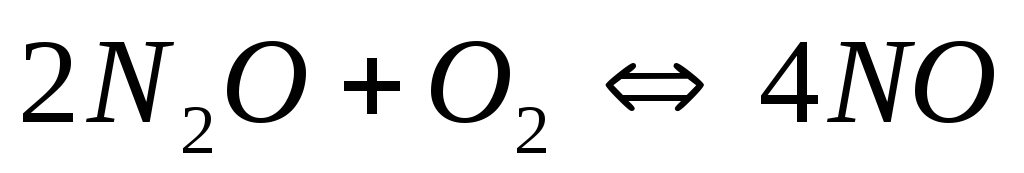 ;
;
-
Температурный коэффициент реакции равен 3. При какой температуре следует проводить эту реакцию, чтобы скорость реакции, идущей при 100°С, уменьшилась в 27 раз?
-
Вычислите константу равновесия реакции
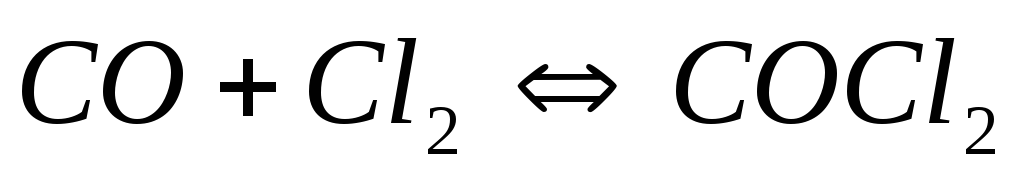 ,
если исходные концентрации оксида
углерода и хлора составляли соответственно
6 и 8 моль/л, а равновесие установилось,
когда образовалось 3 моль
,
если исходные концентрации оксида
углерода и хлора составляли соответственно
6 и 8 моль/л, а равновесие установилось,
когда образовалось 3 моль
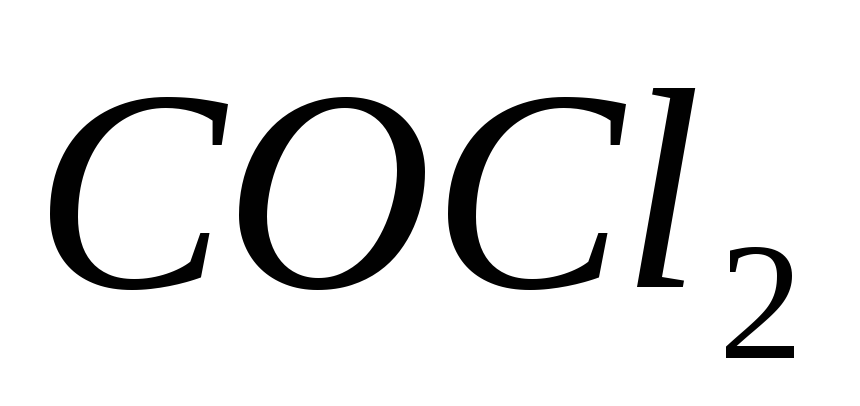 .
. -
До какого объема нужно довести раствор, содержащий 250 г медного купороса
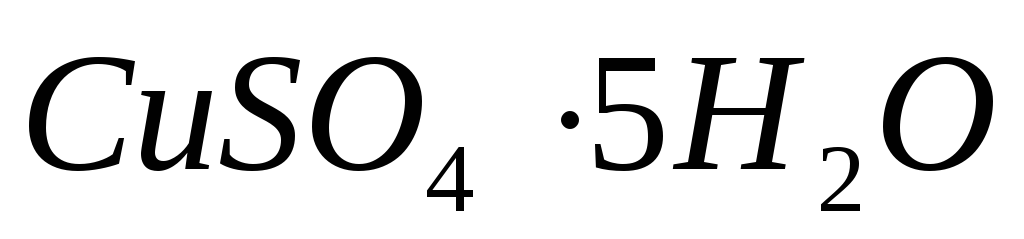 ,
чтобы молярная концентрация эквивалента
(нормальность) полученного раствора
была 0.5 н?
,
чтобы молярная концентрация эквивалента
(нормальность) полученного раствора
была 0.5 н? -
Какое из веществ: гидроксид алюминия, серная кислота, гидроксид бария - будет взаимодействовать с гидроксидом натрия? Составьте уравнения соответствующих реакций в молекулярном и ионно-молекулярном виде.
-
Вычислите температуру кристаллизации раствора мочевины
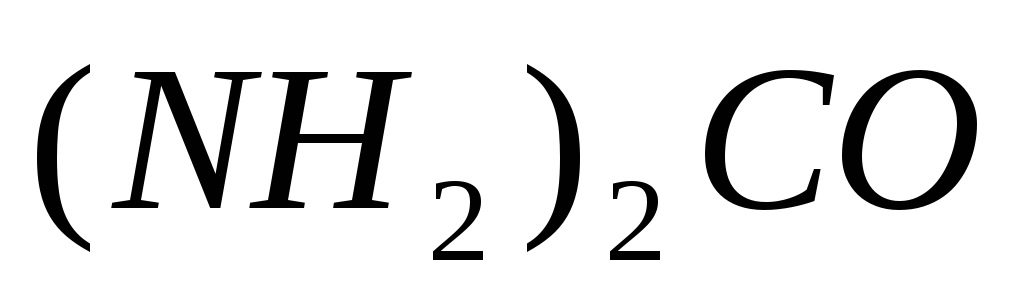 ,
содержащего 10 г мочевины в 150 г воды.
Криоскопическая константа воды равна
1,86º.
,
содержащего 10 г мочевины в 150 г воды.
Криоскопическая константа воды равна
1,86º. -
Увеличится или уменьшится концентрация ионов водорода в растворах кислот при введении в них одноименных анионов: а)
 ; б)
; б)
 ; в)
; в)
 ; г)
; г)
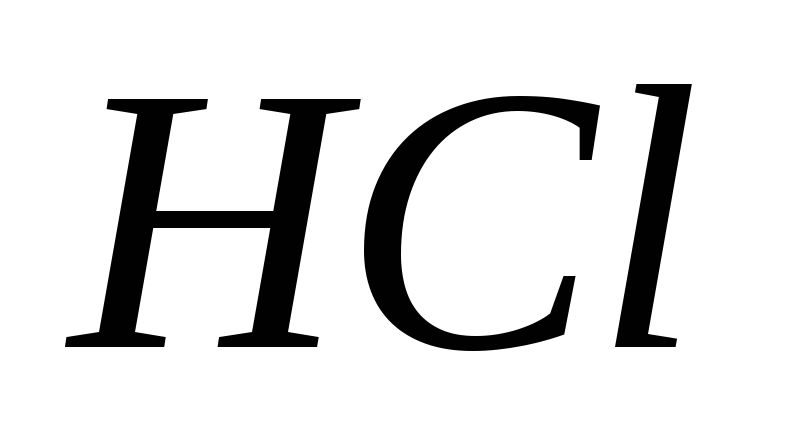 .
. -
Какие из солей
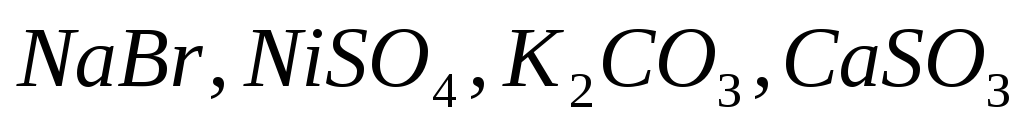 подвергаются гидролизу? Составьте
ионно-молекулярные и молекулярные
уравнения гидролиза, укажите значение
рН растворов этих солей.
подвергаются гидролизу? Составьте
ионно-молекулярные и молекулярные
уравнения гидролиза, укажите значение
рН растворов этих солей.
Вариант 19.
