- •12. Свойства металлов подразделяются на физические, химические, механические и технологические.
- •14. 2. Неполная с температурой нагрева на 30…50 oС выше критической температуры а1:
- •15. Деформация — изменение формы и размеров тела под действием напряжений. Напряжение – сила, действующая на единицу площади сечения детали.
- •19. Влияние нагрева на структуру и свойства металлов
- •Т а б л и ц а 1. Механические свойства высокопрочных чугунов (гост 7293-79)
- •21. Нормализация стали
- •Диаграмма состояния
- •Фазы диаграммы железо — цементит
- •2.2. Диаграммы состояния двойных сплавов
- •2.2.1. Порядок построения диаграмм
- •Температуры начала и конца кристаллизации сплавов
- •2.2.2. Диаграмма состояния сплавов, компоненты которой образуют механические смеси (ι рода)
- •2.2.3. Правило отрезков
- •2.2.4. Диаграмма состояния сплавов, компоненты которой неограниченно растворимы в жидком и твердом состояниях (ιι рода)
- •2.2.5. Диаграмма состояния сплавов, компоненты которой неограниченно растворимы в жидком состоянии и ограниченно в твердом (III рода)
- •2.2.6. Диаграмма состояния сплавов, компоненты которой в твердом виде образуют устойчивые химические соединения (IV рода)
- •2.2.7. Связь между диаграммами состояний и свойствами двухкомпонентных сплавов
Диаграмма состояния
Железо образует с углеродом химическое соединение Fe3C цементит. Так как на практике применяют металлические сплавы с содержанием углерода до 6,67 %, то рассматриваем часть диаграммы состояния от железа до цементита. Поскольку цементит - фаза метастабильная, то и соответствующая диаграмма называется метастабильной (сплошные линии на рисунке).
Для серых чугунов и графитизированных сталей необходимо рассматривать стабильную диаграмму железо-графит (Fe-Гр), поскольку именно графит является стабильной фазой. Цементит образуется намного быстрее графита и во многих сталях и белых чугунах может существовать достаточно долго. В серых чугунах графит существует обязательно.
На рисунке тонкими пунктирными линиями показаны линии стабильного равновесия (то есть с участием графита), там где они отличаются от линий метастабильного равновесия (с участием цементита), а соответствующие точки обозначены штрихом. (Отметим, что обозначения фаз и точек на этой диаграмме подчиняются неофициальному международному соглашению.)

Фазы диаграммы железо — цементит
В системе железо — углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
1. Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
2. Феррит — Твёрдый раствор внедрения углерода в α-железе с ОЦК (объёмно-центрированной кубической) решёткой.
Феррит имеет переменную предельную растворимость углерода: минимальную — 0,006 % при комнатной температуре (точка Q), максимальную — 0,02 % при температуре 700 °C (точка P). Атомы углерода располагаются в центре грани или (что кристаллогеометрически эквивалентно) на середине рёбер куба, а также в дефектах решетки.При температуре выше 1392 °C существует высокотемпературный феррит, с предельной растворимостью углерода около 0,1 % при температуре около 1500 °C (точка I)Свойства феррита близки к свойствам чистого железа. Он мягок (твердость — 130 НВ) и пластичен, магнитен (при отсутствии углерода) до 770 °C.
3. Аустенит (γ) — твёрдый раствор внедрения углерода в γ-железе с ГЦК (гране-центрированной кубической) решёткой.
Атомы углерода занимают место в центре гранецентрированной кубической ячейки.
Предельная растворимость углерода в аустените — 2,14 % при температуре 1147 °C (точка Е).
Аустенит имеет твёрдость 200—250 НВ, пластичен, парамагнитен.
При растворении других элементов в аустените или в феррите изменяются свойства и температурные границы их существования.
4. Цементит (Fe3C) — химическое соединение железа с углеродом (карбид железа), со сложной ромбической решёткой, содержит 6,67 % углерода. Он твёрдый (свыше 1000 HВ), и очень хрупкий. Цементит фаза метастабильная и при длительным нагреве самопроизвольно разлагается с выделением графита.
В железоуглеродистых сплавах цементит как фаза может выделяться при различных условиях:
— цементит первичный (выделяется из жидкости),
— цементит вторичный (выделяется из аустенита),
— цементит третичный (из феррита),
— цементит эвтектический и
— эвтектоидный цементит.
Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зёрен аустенита (после эвтектоидного превращения они станут зёрнами перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зёрен.
Эвтектический цементит наблюдается лишь в белых чугунах. Эвтектоидный цементит имеет пластинчатую форму и является составной частью перлита.Цементит может при специальном сфероидизируюшем отжиге или закалке с высоким отпуском выделяться в виде мелких сфероидов.Влияние на механические свойства сплавов оказывает форма, размер, количество и расположение включений цементита, что позволяет на практике для каждого конкретного применения сплава добиваться оптимального сочетания твёрдости, прочности, стойкости к хрупкому разрушению и т. п.
5. Графит — фаза состоящая только из углерода со слоистой гексагональной решёткой. Плотность графита (2,3) много меньше плотности всех остальных фаз (около 7,5 — 7,8) и это затрудняет и замедляет его образование, что и приводит к выделению цементита при более быстром охлаждении. Образование графита уменьшает усадку при кристаллизации, графит выполняет роль смазки при трении, уменьшая износ, способствует рассеянию энергии вибраций.
Графит имеет форму крупных крабовидных (изогнутых пластинчатых) включений (обычный серый чугун) или сфероидов (высокопрочный чугун).
Графит обязательно присутствует в серых чугунах и их разновидности — высокопрочных чугунах. Графит присутствует также и в некоторых марках стали — в графитизированных сталях.
24. С незапамятных времен люди, совершенствуясь в обращении с металлами, сделали очень важное открытие: если расплавить два металла (или их руды) вместе и дать жидкой массе застыть, то получится новый сплав со свойствами отличными от свойств исходного материала. Так были открыты древние бронзы – сплавы меди с оловом, свинцом, мышьяком. Орудия из бронзы намного превосходили медные и долго удерживали за собой пальму первенства. Но в третьем тысячелетии до нашей эры началось постепенное вытеснение бронз железом, которое было еще практичнее. Вначале его распространение сдерживалось исключительной дороговизной – железо ценилось буквально на вес золота. Открытие дешевых способов выплавки положило начало триумфальному шествию железа и особенно его сплавов, которое продолжается и по сей день.
Чистые металлы в технических устройствах используются крайне редко по причине их фиксированных физико-химических и эксплуатационных свойств. Последние можно существенно изменять в широком диапазоне с помощью добавки в них других элементов, т. е. путем создания сплавов. Такие добавки, иногда даже в незначительном количестве, кардинально изменяют свойства металлов. Например, чистый цирконий легко пропускает нейтроны. Поэтому из него изготавливают оболочки урановых стержней для реакторов. Однако, присутствие в цирконии гафния в количестве всего 0,02 % снижает нейтронную прозрачность в 6…7 раз. Добавки того же циркония в стали и бронзы повышает их тепло и электропроводность до уровня меди.
Сплавами называются материалы, полученные путем диффузии элементов одного компонента в другой, то есть взаимное проникновение их атомов с образованием новых однородных веществ, называемых фазами. Следовательно, фаза – это однородная часть сплава, имеющая определенный состав, свойства, тип кристаллической решетки и границу раздела, при переходе которой свойства скачкообразно изменяются (рис. 12).

Рис.
12. Виды систем сплавов: а –
однофазная; б –
трехфазная; в –
двухфазная;
![]() –
жидкий расплав;
–
жидкий расплав; ![]() –
кристаллы компонента А;
–
кристаллы компонента А; ![]() –
кристаллы компонента Б
–
кристаллы компонента Б
Диффузия компонентов может происходить в жидком, твердом или газообразном состоянии. Как правило, металлические сплавы получают путем расплавления двух или нескольких компонентов с последующей кристаллизацией.
В зависимости от числа компонентов, сплавы могут быть двух, трех или многокомпонентными. Компоненты в сплаве, находящиеся в жидком виде, пребывают обычно в атомарном состоянии, образуя неограниченный раствор с одинаковыми химическими свойствами по всему объему (однофазная система).
В процессе кристаллизации атомы образуют твердый сплав, при этом взаимодействие между ними может быть различным (рис. 13).

Рис. 13. Виды сплавов
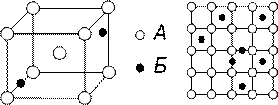
При образовании сплавов в виде механической смеси атомы каждого компонента формируют свои кристаллические решетки и образуют смесь кристаллов двух или нескольких чистых компонентов (рис. 14). Свойства механических смесей – средние между свойствами элементов, которые их образуют. Так, если один элемент имеет высокую твердость, а другой низкую, то чем больше будет твердого элемента, тем выше твердость сплава.
Твердые растворы являются системами однородными, имеют кристаллическую решетку элемента растворителя, то есть компонента, на основе которого формируется сплав, а атомы компонента растворимого или внедряются в решетку растворителя, или частично замещают его места. В первом случае образуется твердый раствор внедрения, а во втором – твердый раствор замещения.
Образование общей кристаллической решетки из атомов разных элементов, имеющих различные диаметры, ведет к искажению решетки, изменению энергетического состояния атомов. В этой связи свойства сплавов отличаются от свойств элементов, из которых они состоят.
В твердых растворах внедрения атомы растворенного элемента распределяются в решетке растворителя (рис. 15). Это возможно, если внедряемые атомы имеют малые размеры. Все твердые растворы внедрения обладают ограниченной растворимостью.
|
|
|
|
Рис.
14. Схема микроструктуры механической
смеси: |
Рис. 15. Схема решетки твердого раствора внедрения: А – атом компонента растворителя; Б – атом компонента растворимого |
|
|
В твердых растворах замещения атомы компонента растворимого занимают часть узлов в кристаллической решетке компонента растворителя. При образовании таких твердых растворов размеры решетки изменяются в зависимости от диаметров растворителя и растворенного элемента. Если атом растворенного элемента меньше атома растворителя (рис. 16, а) элементарная ячейка решетки уменьшается, если больше (рис. 16, б), то увеличивается. Твердые растворы замещения могут быть неограниченными и ограниченными. В первом случае любое количество атомов одного элемента может быть замещено атомами другого и если увеличивать его концентрацию все больше, то плавно совершится переход от одного элемента к другому через ряд сплавов. Такое явление возможно в том случае, когда оба металла имеют одинаковую кристаллическую решетку, несущественно отличающиеся радиусы атомов и свойства растворителя и растворимого. |
Если у металлов с одинаковыми кристаллическими решетками атомные радиусы отличаются существенно, то это ведет к большому искажению решетки и накоплению в ней упругой энергии. Когда искажения достигают очень большой величины, решетка становится неустойчивой и наступает предел растворимости. Твердые растворы вычитания образуются на основе химических соединений. В этом случае при кристаллизации формируется решетка химического соединения АmBn, а избыточное количество атомов одного из компонентов (например, А) заменяет в решетке какое-то количество атомов компонента В. Возможно растворение в химическом соединении и третьего элемента С. В этом случае атомы компонента С заменяют в узлах решетки атомы компонентов А или В.
Иногда твердые растворы на основе химического соединения получаются путем образования пустых мест в узлах кристаллической решетки. Такие растворы называются твердыми растворами вычитания.
Твердые растворы внедрения и замещения обозначаются символами А(В), где А – компонент растворитель, а В – компонент растворимое. Например, ограниченный твердый раствор углерода в железе обозначается Fe(С). При кристаллизации такого раствора формируется решетка железа, а атомы углерода внедряются в эту решетку.
Химическое соединение – это однородная система, у которой кристаллическая решетка отличается от решеток формирующих ее компонентов.
При образовании химического соединения соотношение атомов элементов его составляющих соответствует стехиометрической (от греч. stoicheion – элемент и …метрия) пропорции, то есть имеет место количественное соотношение между массами веществ, вступающих в химическую реакцию. В общем виде химическое соединение двух элементов можно обозначить простой формулой АnВm.
Химическое соединение имеет определенную температуру плавления. Его свойства (изменяющиеся скачкообразно) резко отличаются от свойств входящих в него элементов.
В случае образования химического соединения только металлическими элементами образуется металлическая связь, а при образовании соединения металла с неметаллом – ионная.