
лекции_1 / Молекулярка / Распределение Максвелла,теория теплоемкости
.pdfЛекция 12.
Термодинамические функции состояния. Функции распределения. Классическая и квантовая статистики. Статистические распределения. (2 часа)
12.1.Микроскопические параметры. Вероятность и флюктуации. Распределение молекул /частиц/ по абсолютным значениям скорости. Распределение Максвелла.
12.2.Средняя кинетическая энергия частицы. Скорости теплового движения частиц.
12.3.Распределение Больцмана.
12.4.Теплоемкость многоатомных газов. Ограниченность классической теории теплоемкостей.
12.5.Статистический смысл термодинамических потенциалов и температуры. Роль свободной энергии.
12.6.Распределение Гиббса для системы с переменным числом частиц.
12.7.Принцип Нернста и его следствия.
Демонстрации:
1.Распределение молекул по скоростям.
2.Атмосферное давление.
Распределение молекул по скоростям. Распределение Максвелла
Основные понятия теории вероятностей
Впервые решил задачу распределения молекул по скоростям Максвелл в
1859 году.
Пусть мы имеем ансамбль из N молекул
Параметр Х - принимает значения |
Х1;X2;X3.........Xi........ |
которые выпали соответственно |
N1,N2,N3 ........Ni ......раз.. |
Ni -- число молекул у которых параметр Х принимает значение Хi , тогда
отношение
Pi = Ni / N
вероятность того что параметр Х имеет значение Xi
Пример : ИГРАЛЬНАЯ КОСТЬ Кость имеет 6 граней, она должна быть однородной. Будем бросать кость 6
000 раз. События Хi -выпадание той или иной цифры от 1 до 6
Пусть 1 выпадает 999 раз |
P1=999/6000=1/6 |
|
2- выпадает 1001 |
раз |
P2=1001/6000= 1/6 |
3- выпадает 998 |
раз |
P3=998/6000 = 1/6 |
4- выпадает 1003 |
раз |
P4=1003/6000= 1/6 |
5- выпадает 996 |
раз |
P5=996/'6000 = 1/6 |

6- выпадает 1000 раз P6=1000/6000 =1/6
----------------------------------
Сумма общего числа испытаний равняется 6 000, а вероятность каждого из событий равна 1/6
Если же за N возьмем не 6 000 а 60 000, то вероятность Pi каждого из событий еще ближе к 1/6.
СВЯЗЬ СРЕДНЕГО ЗНАЧЕНИЯ С ВЕРОЯТНОСТЬЮ
|
|
|
x1n1 x2 n2 |
x3n3 |
........xN nN |
x |
n1 |
x |
n2 |
x |
n3 |
.......x |
|
nN |
|
|||||
x |
|
|||||||||||||||||||
|
n n |
n ..........n |
|
|
|
|
|
|
|
|
||||||||||
|
|
|
N |
1 |
N |
2 |
N |
3 |
N |
|
N |
N |
|
|||||||
1 |
2 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
x1 p1 x2 p2 |
x3 p3 .......xN pN |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
Если же случайные события или параметр Х изменяется не дискретно а |
|
|||||||||||||||||||
непрерывно, то |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
dP(x)=F( X )dx |
|
|
|
|
|
|
|
|
|
|||
представляет собой вероятность нахождения параметра Х в интервале от Х до Х+dX
F(X)-- плотность вероятности или функция распределения вероятности . Тогда число молекул, у которых значение параметра Х принадлежат интервалу от X до dX определяется соотношением:
dN=NdP(x)=NF(х)dх
РАСПРЕДЕЛЕНИЕ МАКСВЕЛЛА
Скорость молекулы тоже случайная величина , тогда число молекул ( dNv ) модуль
скорости которых лежит в интервале от V до dV определяется соотношением:
dNv=NdP : dPv=F(V)dV : dN=NF(V)dV
где F(V) -- функция распределения вероятности значения скорости
Основное уравнение молекулярно-кинетической теории приводит к выводу о том, что средний квадрат скорости
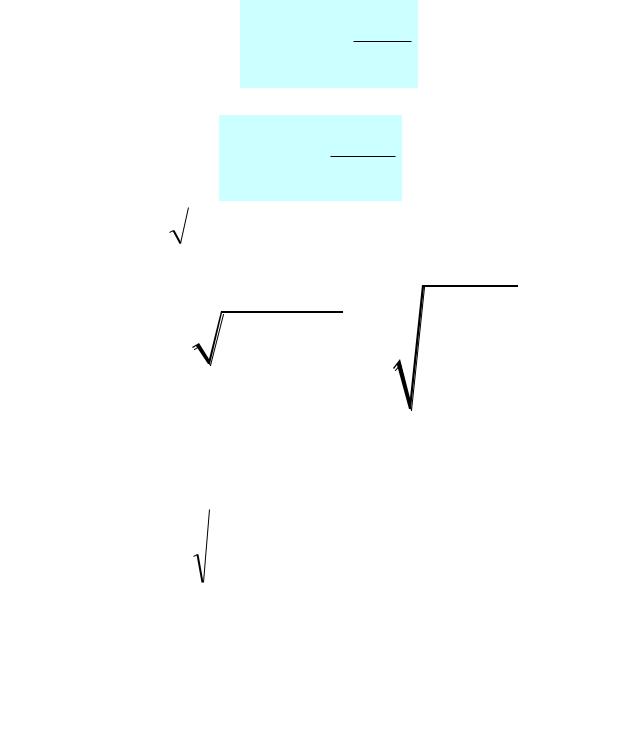
молекул зависит от температуры газа и определяется формулой
2 3kT mo ,
которую можно также представить в виде
2 3RT
.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Величину |
|
2 |
- называют среднеквадратичной |
|||||||||||
скоростью. Будем обозначать ее |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3RT |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
кв |
2 |
|
|||||||||||
|
|
|
|
|
||||||||||
|
|
. |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Расчеты показывают, что величина среднеквадратичной скорости молекул азота (воздуха) при нормальных условиях равна
|
|
|
|
3 8,314 273,15 |
|
|
|
кв |
|
500 м / с |
|||||
0 ,028 |
|||||||
|
|
|
|
|
|
||
Очевидно, что при хаотическом движении молекулы газа имеют не одинаковые скорости. Их величина с течением времени непрерывно изменяется. Скорости молекул могут принимать любые значения в интервале от 0 и до бесконечности. Однако средние характеристики этого движения имеют вполне определенные численные значения, зависящие только от температуры газа. Впервые
закон распределения скоростей молекул был получен Дж.
Максвеллом в 1859 году. В соответствии с этим законом доля молекул, скорости которых принадлежат заданному

интервалу скоростей от |
до , определяется |
соотношением |
|
f ( )
|
|
3 |
|
|
|
|
|
|
mo |
|
2 |
f ( ) |
|
|
|
|
|||
|
2 kT |
||
mo 2 e 2 kT -
функция распределения Максвелла
|
|
|
|
|
|
|
|
|
3 |
|
|
|
m 2 |
|
|
|
|
|
mo |
|
|
|
|
|
|
||||||
|
|
2 |
|
|
|
||||||||||
2 |
|
|
|
|
|
o |
|
||||||||
N 4 N |
|
|
|
|
e |
2 kT |
|
||||||||
2 kT |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
3 |
|
|
|
|
m 2 |
|
||
2 |
|
|
mo |
|
|
|
|
|
|
||||||
|
|
2 |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
o |
|
|
|
dN 4 N |
|
|
|
e |
2kT d |
||||||||||
|
|
|
|
||||||||||||
|
|
|
2 kT |
|
|
|
|
|
|
|
|
|
|||
Здесь N - число всех молекул в сосуде, N - число молекул, скорости которых принадлежат заданному
интервалу скорости (от до ), mo - масса молекулы, T - абсолютная температура, k - постоянная Больцмана.
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
mo 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
mo |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|||||
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
dN NF ( )d 4 |
N |
|
|
|
e 2 kT |
|
d |
||||||||||
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
2 kT |
|
|
|
|
|||
F ( ) 4 2 f ( ) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
3 |
|
|
|
m 2 |
|
|
|
|
|
|
|||
mo |
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
||||||||
2 |
|
|
|
o |
|
|
|
|
|
|
|
|
|||||
f ( ) |
|
|
|
|
e |
2 kT |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
2 kT |
|
|
|
|
|
|
- плотность вероятности |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
F ( )d 1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Приведенное |
соотношение |
|
называют |
законом |
|||||||||||||
распределением Максвелла по скоростям молекул. Как оказалось распределение Максвелла справедливо не только для газов. По закону Максвелла распределены скорости молекул жидкостей и твердых тел. Распределение Максвелла удобно проанализировать с помощью
диаграммы, на которой представлена зависимость функции |
|||||||||||
распределения |
f ( ) |
от |
скорости |
|
. Функция |
||||||
распределения Максвелла имеет вид: |
|
|
|
|
|
|
|||||
|
|
2 |
|
|
|
3 |
|
|
2 |
||
|
|
mo |
|
|
m |
||||||
|
|
2 |
|||||||||
|
|
|
o |
||||||||
f ( ) 4 |
|
|
|
|
e |
2 kT |
|
||||
|
2 kT |
||||||||||
|
|
|
|
|
|
|
|
|
|||
На приведенной диаграмме площадь узкой полоски численно равна доле молекул, скорости которых принадлежат заданному интервалу скоростей, а площадь под кривой численно равна единице, т.к. характеризует молекулы, скорости которых принимают любые значения
от 0 до .
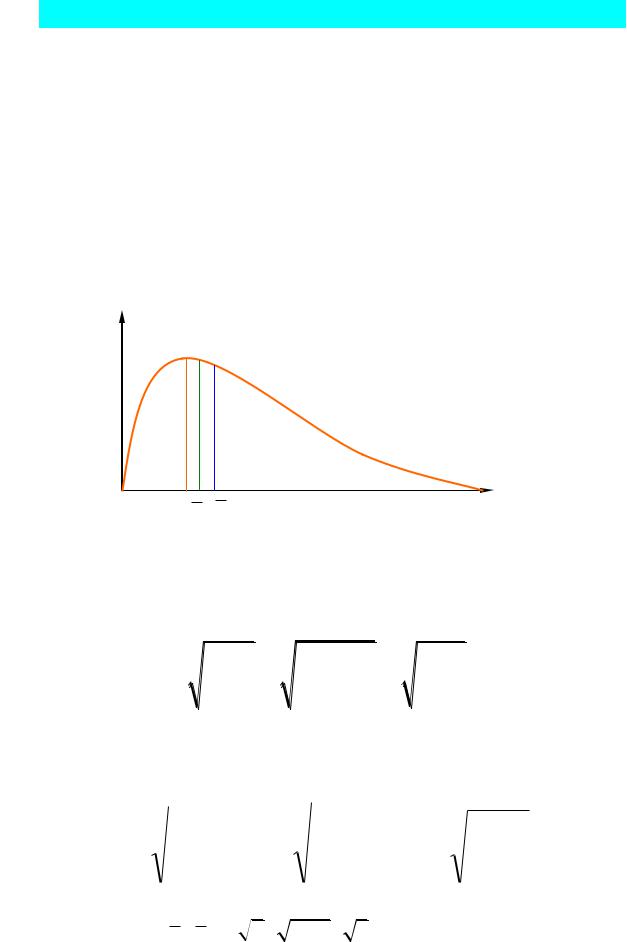
Функция распределения Максвелла имеет максимум. Скорость, соответствующую максимуму функции распределения называют наиболее вероятной скоростью. Величину наиболее вероятной скорости можно определить из условия экстремума функции распределения. Дифференцируя функцию распределения и приравнивая полученный результат нулю, получим:
|
m |
|
m |
|
|
3 |
|
|
mo 2 |
|
|
2 |
|
2kT |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
( 8 4 2 |
o |
) |
|
o |
2 e |
|
2 kT |
0 |
|
в |
|
|
|
. |
||
|
|
|
|
|
|
|||||||||||
|
kT |
|
|
|
|
|
|
|
|
|
|
|
|
mo |
||
|
|
2 kT |
|
|
|
|
|
|
|
|
|
|||||
f ( )
в кв
Как видим, наиболее вероятная скорость меньше среднеквадратичной скорости. С помощью распределения Максвелла можно рассчитать также среднюю скорость молекул газа. Ее величина определяется формулой
|
|
|
8kT |
|
8kNAT |
|
8RT |
|
||
|
|
|
||||||||
m |
m N |
A |
. |
|||||||
|
|
|
o |
|
o |
|
|
|
||
Более удобными для расчетов среднеквадратичной, наиболее вероятной и средней скоростей молекул формулы приведены ниже:
|
|
|
|
|
|
|
|
|
8RT |
|
в |
2RT |
|
|
|
|
|
||||
|
|
|
|
|||||||
|
|
|
|
|||||||
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3RT |
|
|
кв |
|
|
||
|
|||||
|
|
|
|
||
в : : кв 
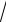 2 :
2 : 
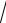 8 / :
8 / : 
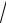 3 1:1,13:1, 22
3 1:1,13:1, 22

Отношение скорости молекулы к наиболее вероятной скорости ансамбля молекул называют приведенной или
относительной скоростью молекулы u |
|
|
|
|
|
|
|
|
в |
||
|
|
|
|
Распределение Максвелла для приведенной скорости:
dN 4 Ne u2 u2 du
u |
|
|
|
|
|
|
|
u |
|
|
|
|
N 2 |
4 |
|
Ne u2 u2 du |
4 |
|
N 2 e u2 u2 du |
1 |
ue u2 |
|
|||
|
|
|
|
|
|
|
||||||
|
|
2 |
||||||||||
u1 |
|
|
|
u1 |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|||
1 u2 e u2 du !&!&!&!& 2 u1
u2 e u2 du интеграл вероятности или Пуассона
u1
|
|
( 1) |
т |
u |
2 m 1 |
||
e u2 |
|
|
|
|
|
||
т! |
|
2m 1 |
|||||
|
т 0 |
|
|
||||
Сколько молекул в моле имеют скорости меньшие наиболее вероятной не более чем на 0.1 B
N 6.02 1023 |
u |
|
0.9 |
u=0.1 |
|||||
B |
|||||||||
|
|
|
|
|
|
|
|
||
N=N1.0 |
4 |
|
Ne u2 u2 du интеграл табулирован Волькенштейн стр. 50 |
||||||
|
|
|
|||||||
|
|
||||||||
0.9 |
|
|
|
|
|
|
|
||
N |
0.81 N 0.81N u 0.81 6.02 1023 0.1 50 1021 молекул |
|
N u |
||
|
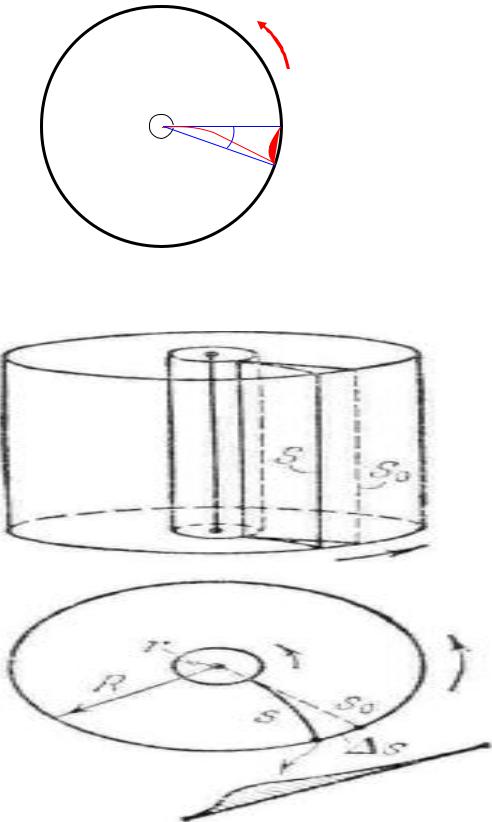
Распределение Максвелла получило экспериментальное подтверждение в 1920 г. в опытах Штерна.
|
|
R |
|
|
, |
|
s |
|
O . |
|
|
|
|||||
A |
|
|
|
R |
|
|||
R |
|
s |
|
|
R |
2 |
||
|
s |
|
|
|
|
|||
R |
A’ |
|
|
|
s . |
|||
|
R |
|
||||||
|
|
|
|
|
|
|
|
|
Опыты Штерна сводились к следующему. Два коаксиальных цилиндра приводились в быстрое вращение. На внутренней поверхности большого цилиндра осаждались пары серебра, которые в виде узкого пучка выходили из узкой щели малого цилиндра. Внутри большого цилиндра поддерживался глубокий вакуум. Вдоль оси малого цилиндра располагалась тонкая нить, покрытая тонким слоем серебра и нагреваемая электрическим током. В соответствии с представлениями молекулярнокинетической теории скорости атомов серебра распределены по закону Максвелла. Величину скорости атомов серебра можно определить по формуле:
|
|
|
R2 |
|
|
|
|
|
s |
, |
|
|
|
|
|
|
|
|
||
в которой |
R - радиус большого цилиндра, |
- угловая |
||||
скорость |
вращения цилиндров, |
s |
- величина, |
|||
характеризующая положение осажденного атома серебра. Прямые измерения указанных величин и анализ плотности осажденных атомов серебра приводят к выводу о том, что Максвелловский закон распределения по скоростям полностью подтверждается данным экспериментом.
Барометрическая формула. Распределение Больцмана
Сравним атмосферное давление на двух близких горизонтальных уровнях. В соответствии с известными законами гидростатики давление на более низком уровне

p dp
p  dh
dh
превосходит давление на более высоком уровне на
величину gdh. В силу этого получим
dp gdh.
В соответствии с уравнением Менделеева-Клапейрона плотность воздуха будет равна
p . Учитывая это, далее получим
RT
dp |
p |
|
|
|
dp |
|
|
mo gdh |
||||||||||||||||
|
gdh |
|
|
|
|
|
|
|
|
|
. |
|||||||||||||
RT |
|
p |
|
|
kT |
|||||||||||||||||||
Выполняя интегрирование приведенного соотношения, |
||||||||||||||||||||||||
получим |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
p |
dp |
|
h |
m gdh |
|
|
|
|
|
|
p |
|
m gh |
|||||||||||
|
p |
|
kT |
|
ln p |
|
kT . |
|||||||||||||||||
|
|
|
|
|
o |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
o |
|
po |
|
|
o |
|
|
|
|
|
|
|
|
|
|
o |
|
|
|
|
|
|
|
|||
После потенцирования получим известную |
|
|
|
|
|
|
|
|||||||||||||||||
барометрическую формулу Больцмана |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
p p e |
mo gh |
|
|
|
|
|
P0 |
|
|
|
|||||||||||
|
|
|
|
kT |
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
mo gh |
|
|
|
|||||||||||||
|
|
|
|
|
|
o |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
e kT |
|
|
|
||||||
|
|
|
|
|
|
|
|
gh |
|
|
|
|
|
P0 |
|
|
|
|||||||
|
|
|
P p e |
RT |
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
gh |
|
|
|
|
|||||||||||||
|
|
|
|
|
|
o |
|
|
|
|
|
|
|
|
|
(1) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
e kT
