
лекции_1 / Молекулярка / лк кл теория теплоемкости 2010
.DOCКлассическая и квантовая теория теплоемкости газов.
Классическая теория основана на предположении, что к атомно-молекулярным системам применимы законы классической механики.
![]()
![]()
-
Одноатомные газы.
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() теория
теория
Практика
Газ |
Т(k) |
|
|
Hg |
527 |
1.666 |
|
He |
290 |
1.660 |
|
He |
93 |
1.670 |
|
Ne |
292 |
1.640 |
|
Ar |
288 |
1.650 |
|
Ar |
98 |
1.690 |
-
Двухатомный газ.
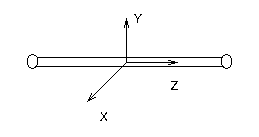
Жёстко! i=5
![]()
![]()
![]()
![]()
![]()
![]()
Эксперимент
Газ |
Т |
|
H2 |
280 |
1.407 |
N2 |
293 |
1.398 |
|
N2 |
92 |
1.419 |
|
O2 |
293 |
1.398 |
|
O2 |
197 |
1.411 |
|
O2 |
92 |
1.404 |
Хуже!
Ещё хуже практика согласуется с теоретическими результатами для трёх и более атомных газов.
-
Теплоёмкость твёрдых тел.
Кристаллическая решётка + электронный газ.
Узлы решётки колеблются
![]()
Все атомы одинаковы колебательных 3 степени свободы
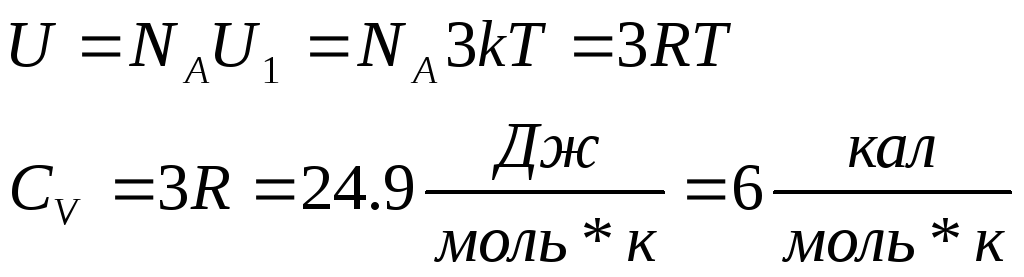
1819 Дьюлонг (1785-1838) и Пти (1791-1820)
произведение удельной теплоёмкости химического элемента в твёрдом состоянии на его атомную массу одинаково для всех элементов и составляет около 3R.
C * = Cоnst = 3R
Закон Джоуля-Коппа 1864.
Молярная теплоёмкость твёрдого соединения равна сумме молярных теплоёмкостей элементов из которых оно состоит.
-
Недостатки классической теории теплоёмкости.
-
Не даёт объяснения зависимости С от Т.
-
Непоследовательность: н-р двухатомная молекула и твёрдое тело (атом не точка!) i = 3+3 = 6, если атомы рассматривать как твёрдые тела, то i = 12. Атомные системы представляются (моделируются) как макро системы с наложенными связями.
-
Для металлов С = 3R, электронов газ. Его С не учитывается. Но по теории она должна была быть равной теплоёмкости решётки. Опыт –свободные электроны не вносят никакого вклада в теплоёмкость металлов.
-
Опыт –эффективный вклад в теплоёмкость вносят не все, а только некоторые степени свободы.
Квантовая теория теплоёмкости.
-
Может принимать лишь дискретные значения.
Гармонический осциллятор
![]()
v – частота осциллятора
n = 0,1,2,3, …
h = 6,626176*10-34Дж*С
-
Пусть кТ hv. Газ = гармонических осцилляторов. Здесь должны происходить нулевые колебания и Ек 0, тогда как классическая теория совсем исключает их (считая молекулу абсолютно жёсткой). Энергия нулевых колебаний не зависит от температуры. С ростом Т начинают возбуждаться первый и более высшие энергетические уровни.
![]() - характеристическая температура
- характеристическая температура
H2 TV = 6000 K
-
Вращение молекул
![]()
J=mr2
l = 0,1,2,3,…(n-1)
l = 0 Eв = 0
l = 1
![]()
![]()
Если kT << Eв1 то теплоёмкость можно вычислять не учитывая вращение молекул.
Если kT << Eв1 то уже дискретность уровней энергии слабо связывается и применима классическая теория.
![]()
- характеристическая температура.
-
Дискретность энергетических уровней не совместима с классической теоремой о равнораспределении молекул по степеням свободы.
