
Химические свойства
Альдегиды и кетоны - реакционноспособные органические соединения: альдегиды > активнее кетонов.
Особенности строения карб. группы: связь между атомами С и О осуществляется 2-мя парами е, состоит из - и -связей.
Из-за большей электроотриц-ательности атома О плотность е -связи смещена в его сторону, в результате у него создается повышенная электронная плотность, у атома С - пониженная:
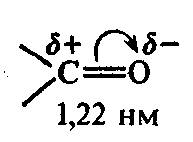
Атом С активно взаимодействует с нуклеофильными реагентами, атом О - с электрофильными.
Атом С карб. группы находится в состоянии sр2-гибридизации, эта часть молекулы плоская (все атомы группы лежат в одной плоскости), поэтому доступна для реагентов сверху и снизу.
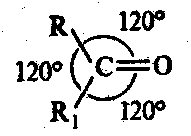
Введение в радикал заместителя, снижающего электронную плотность у атома С карбонильной группы, увеличивает его способность взаимодействовать с нуклеофильными реагентами, и, наоборот, электронодонорные заместители, повышающие электронную плотность у С атома, снижают ее. Этим объясняется большая реакционная способность альдегидов и кетонов алифатического ряда, по сравнению с ароматическими.
С увеличением объема молекулы реакционная способность снижается, поэтому альдегиды, карбонильная группа которых связана с одним радикалом и атомом водорода, обладают большей реакционной способностью, чем кетоны:
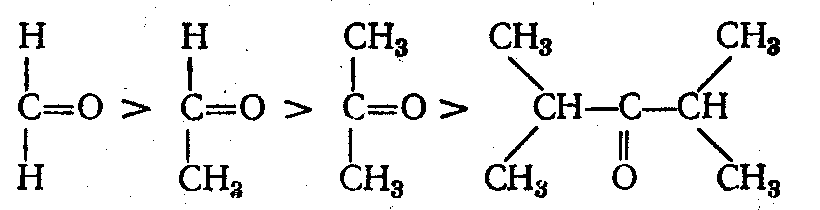
Характерные реакции:
присоединения
замещения
окисления
конденсации и полимеризации
Реакции присоединения (AdN).
Аатом С карбонильной группы взаимодействует с нуклеофильным реагентом (I), двойная связь разрывается с образованием аниона (II), который, взаимодействуя с протоном, дает гидроксисоединения:
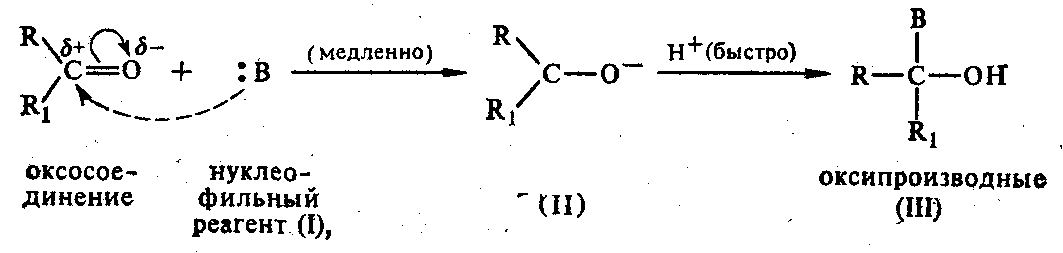
Примеры:
взаимодействие с синильной кислотой, спиртами, гидросульфитом натрия.
1. Присоединение синильной кислоты в присутствии основания:
- образование нуклеофила - цианид-иона:

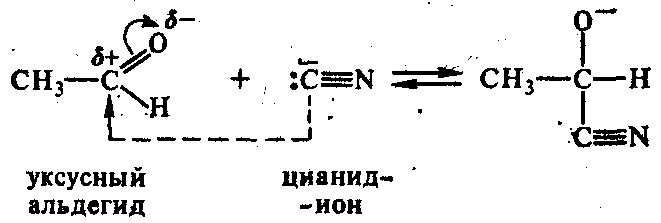
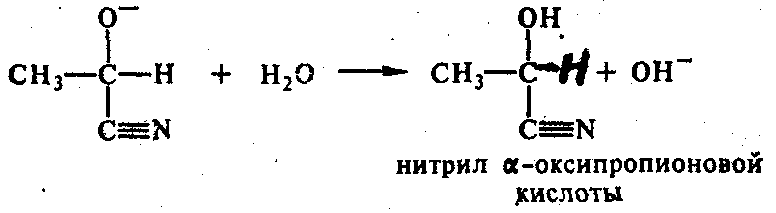
2. Присоединение гидросульфита натрия (NаНSО3):
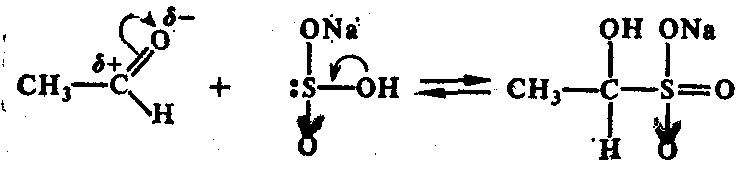
Из кетонов в реакцию вступают метилкетоны и кетоны ациклического ряда (циклогексанон):

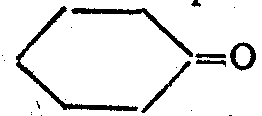
Реакция обратима, при добавлении кислоты или основания образуются исходные продукты. Применяется для установления содержания оксосоединений в ароматических и вкусовых веществах пищевых продуктов.
3. Присоединение металлорганических соединений (см спирты);
4. Действие аммиака на альдегиды и кетоны:
- альдегиды с NH3 образуются альдегидоаммиаки:
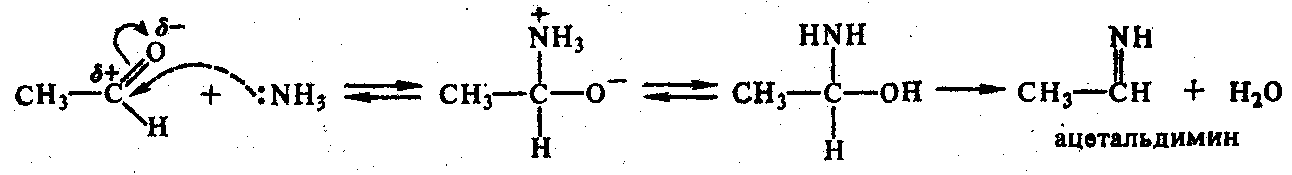
Полимеризация альдимина с образованием альдегидаммиака:
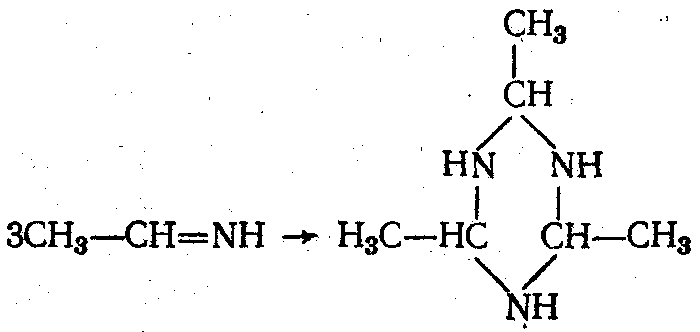
Кетоны не взаимодействуют с аммиаком в этих условиях.
5. Присоединение спиртов и образование полуацеталей и ацеталей - как простые эфиры, образованные диолом, содержащим две ОН группы у одного С атома, и двумя молекулами спирта при Т и Н+:

Участвуют в образовании запаха пищевых продуктов (вино, хлеб и т.д.). Для получения кеталей применяют специальные методы.
6. Восстановление альдегидов и кетонов и образование первичных вторичных, соответственно, спиртов:
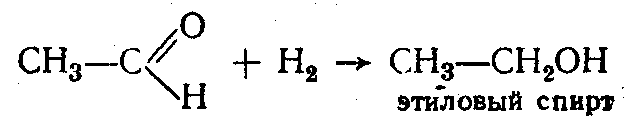
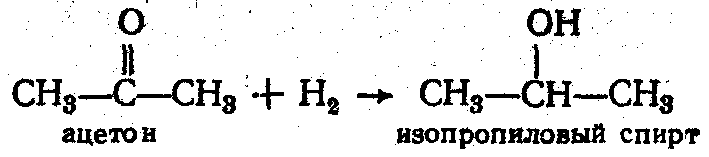
Кат.: Ni, Co, Pt, Pd, восстановление LiAlH4 или H2 в момент выделения.
Реакции замещения- обмен атома О на другие атомы:
1. Взаимодействие с пентахлоридом и бромидом фосфора:
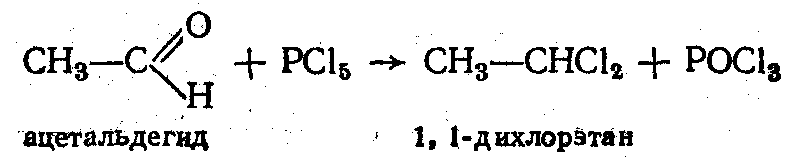

2. Взаимодействие с гидроксиламином:
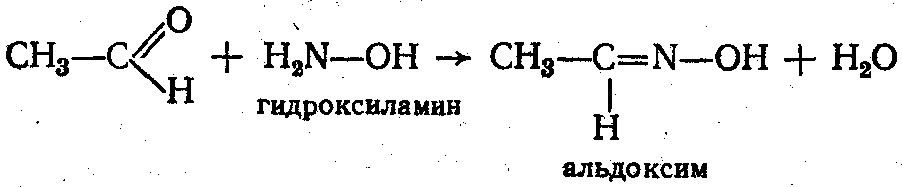
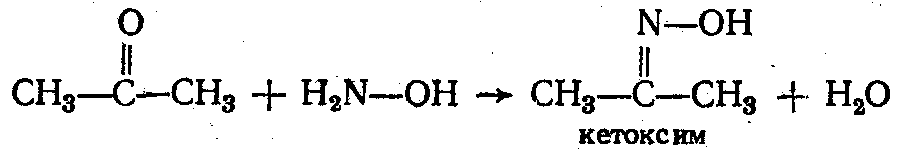
Применяется солян. гидроксиламин NH2OHHCl, и выделяющаяся НСl оттитрована, что используется для количественного определения альдегидов и кетонов.
3. Взаимодействие с гидразином и его производными - с 1 мол. H2N–NН2 образуют гидразоны, затем - азины:
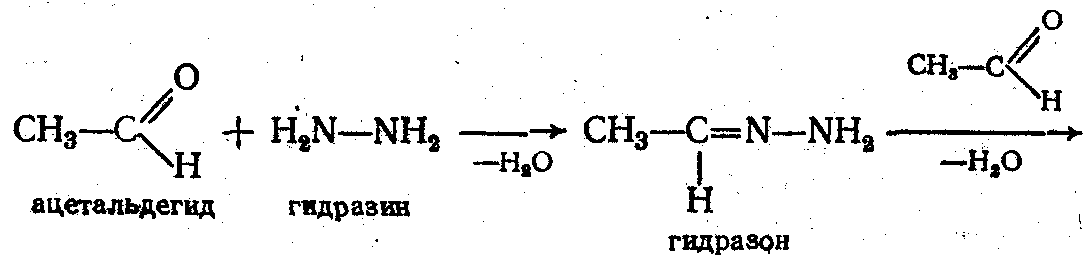
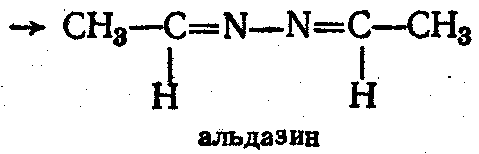
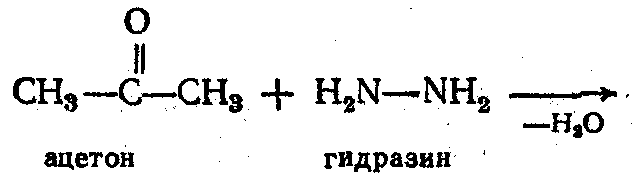
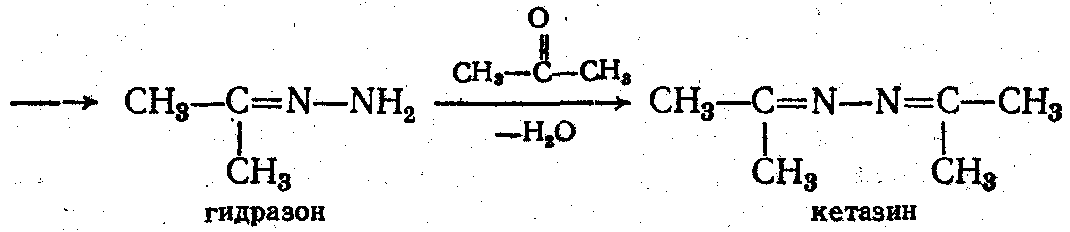
С фенилгидразином С6Н5–NH–NH2;
С 2,4-динитрофенилгидразином (О2N)2C6H3–NH—NH2;
С
семикарбазидом
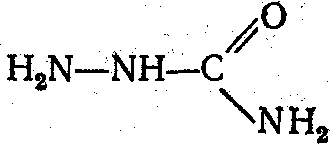
Применение- выделение и разделение альдегидов и кетонов.
Отнесение реакций к реакциям замещения условно. По существу это реакции присоединения (AdN).
4. Окисление альдегидов и кетонов.
4.1 Слабыми окислителями до одноосновных карбоновых кислот с тем же числом атомов углерода (р-ция Аg зеркала и с реактивом Фелинга):

4.2 Окисление кетонов протекает с сильными окислителями при T с разрывом С-ной цепи с образованием смеси кислот (правило Вагнера и Попова). Применение- для установления строения.
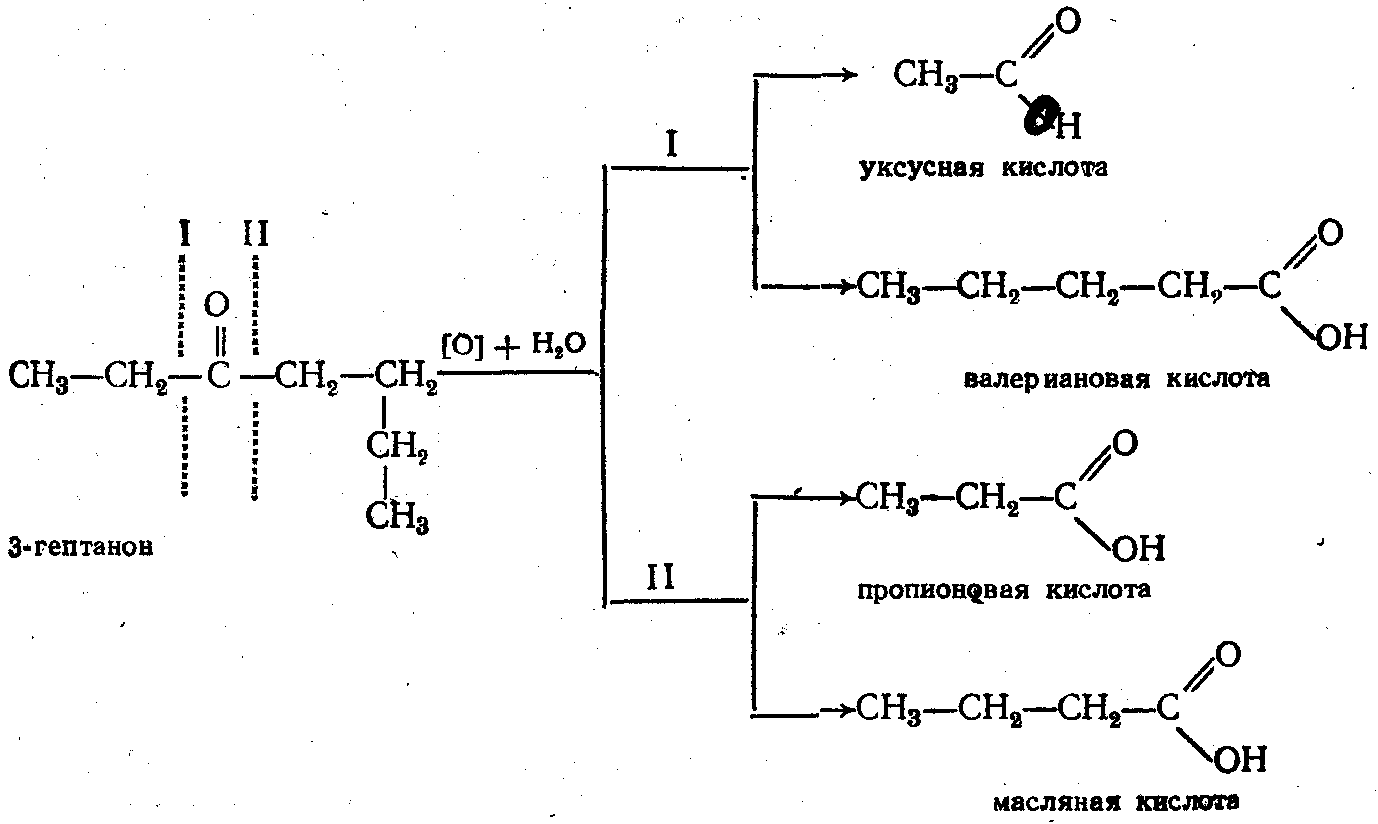
4.3 Реакция Канниццаро: молекула альдегида в присутствии конц. щелочей может окисляться за счет другой мол. альдегида, которая при этом восстанавливается до спирта:
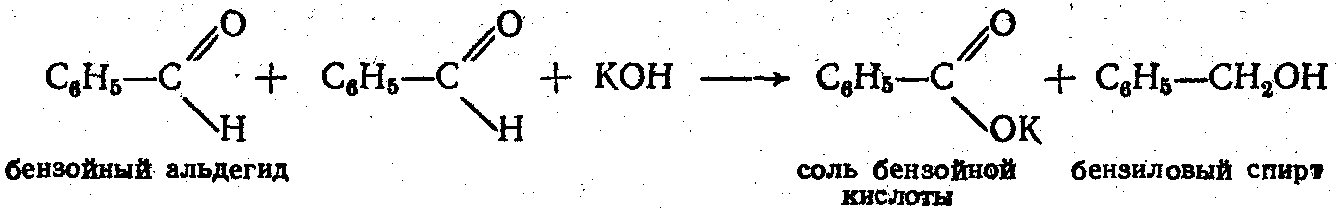
5. Реакция Тищенко. Алифатические альдегиды под действием этилата алюминия в неводной среде образуют сложные эфиры:
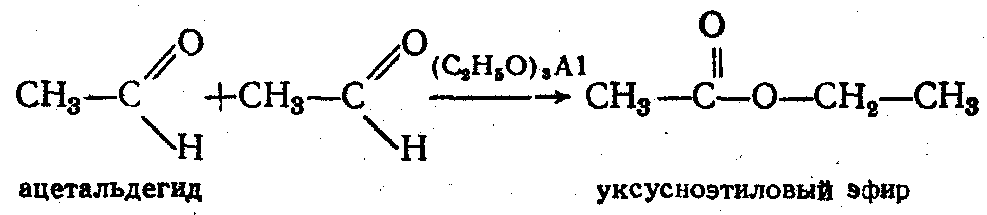
6. Реакции, связанные-с подвижностью атомов водорода в -положении. Атомы Н в -положении к карбонильн. группе протонизированы из-за снижения е плотности у С атома (эффект сопряжения и индуктивный эффект), поэтому в присутствии оснований с Гал образуются -галогенпроизводные:
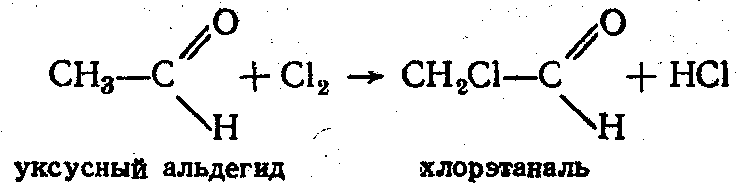
Образование промежуточное аниона:
Первая лимит-щая стадия медленная:
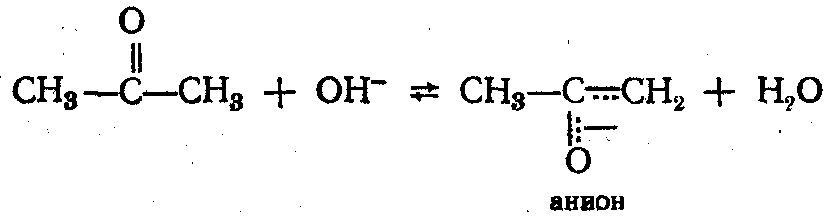
Вторая – быстрая:
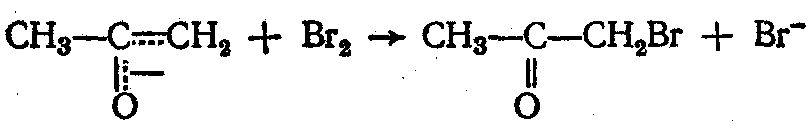
Структура аниона с 2 граничными формулами:
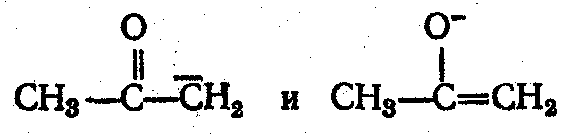
5 Реакции поликонденсации
Альдольная коденсация:
На 1-м этапе под действием ОН- отщепляется протон от С в -положении, образуется карбанион, вступающий в реакцию со второй молекулой альдегида:
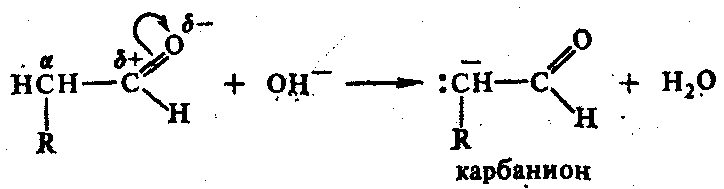
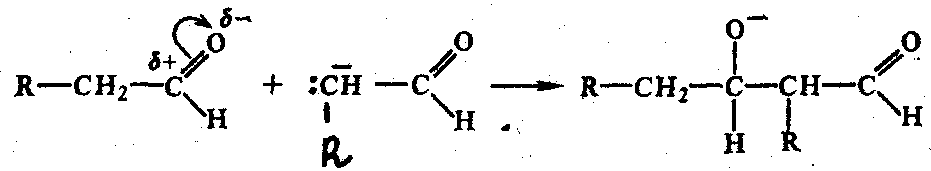
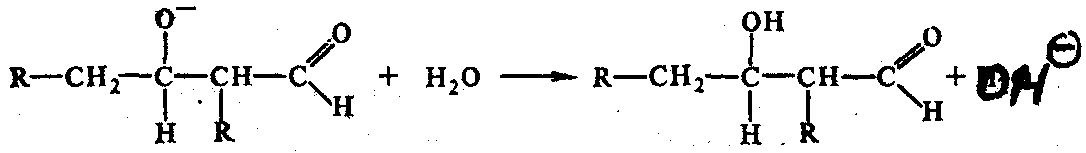
Димер содержит 2 функциональные группы, получил название альдоль:
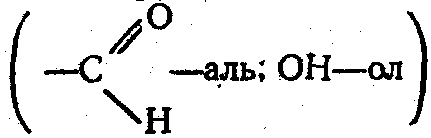
6. Кротоновая конденсация -взаимодействие при нагревании с потерей молекулы воды. По аналогии с образовавшимся простейшим продуктом конденсация получила название кротоновой:
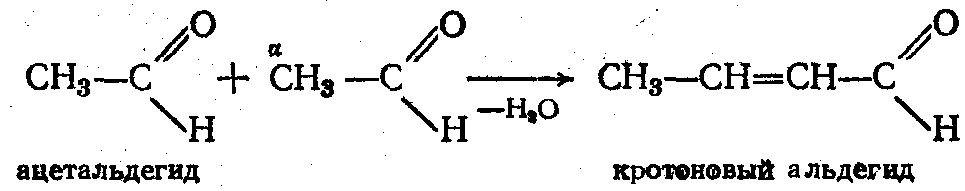
От предельных к непредельным.
Низкомолекулярные кетоны также вступают в реакции альдольной и кротоновой конденсации:

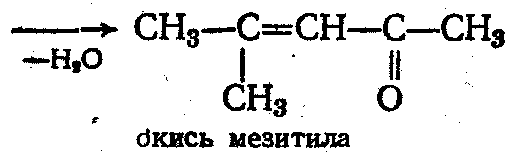
7. Взаимодействие альдегидов с фенолами кислой или щелоч. среде и образование фенолформальдегидных смол.
Образование фенолоспиртов:
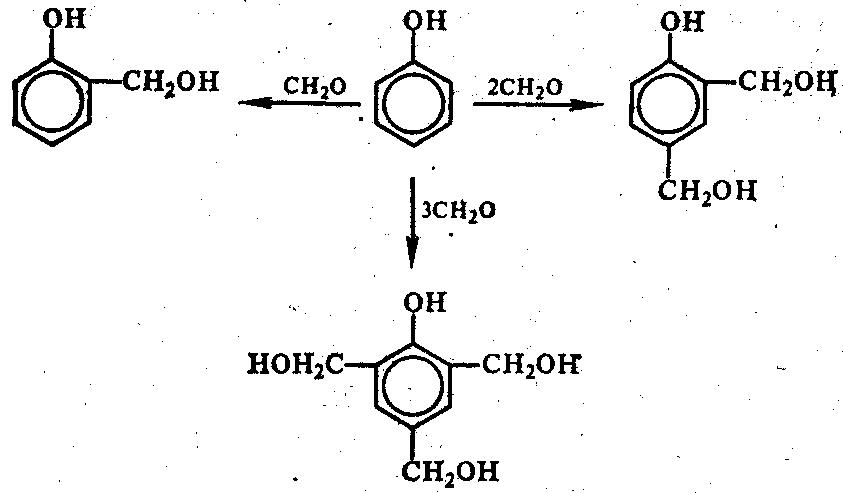
Молекула формальдегида направляется в о- и п-положения.
При нагревании фенолоспирты конденсируются с образованием, в зависимости от условий, различных продуктов:
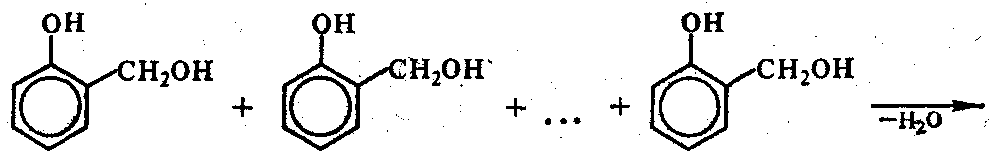
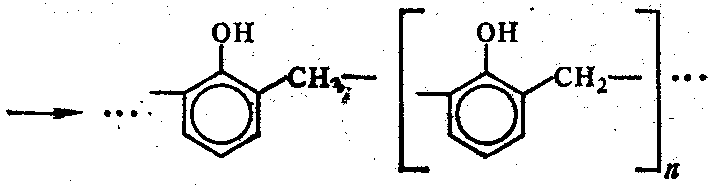
Продукт с М.М до 1000 - ризол. Применение - в качестве лаков и приготовление пресс-порошков с наполнителями: древесная мука, стеклянное волокно, графит и т.д.
