
Ado_A_D_Patologicheskaya_fiziologia
.pdfКонтроль и регуляция иммунного ответа 1. Способность к иммунному ответу контролируется генетически. Уро
вень ответа на конкретные антигены определяется генами, локализован ными в главном комплексе гистосовместимости (МНС), эффект которых реализуется на уровне обработки и «представления» антигенных пепти дов антигенпрезентирующими клетками Т-хелперам.
2.Регуляция уровня иммунного ответа осуществляется гормонами и медиаторами вегетативной нервной системы, а также регуляторными пеп тидами. Характер действия гормонов определяется их концентрацией в крови. При физиологической концентрации они, как правило, способству ют развитию иммунного ответа. При высокой (фармакологической) кон центрации некоторые из них по преимуществу ингибируют иммунные про цессы (это относится к гормонам коры надпочечников, являющимся классическими индукторами апоптоза лимфоцитов, АКТГ, адреналину, по ловым гормонам, (3-эндорфинам, адренергическим медиаторам), другие (гормон роста, пролактин, гормоны щитовидной железы, инсулин, а-эн- дорфины, холинергические медиаторы), как правило, стимулируют им мунный ответ. В то же время ряд цитокинов (особенно ИЛ-1) оказывает влияние на активность нервной и эндокринной систем. Пептидные гор моны, выделяемые эпителиальными клетками вилочковой железы — тимулин, тимозины, тимопоэтины — могут быть отнесены одновременно к продуктам иммунной и эндокринной систем.
3.Иммунный ответ подвержен ауторегуляции. Накопление 1дС-анти- тел в свободном и особенно связанном с антигенами виде подавляет даль нейшее развитие гуморального ответа, действуя через Яс-рецепторы регуляторных и эффекторных клеток. Ингибирование достигается также по механизму идиотипического контроля — через образование антител к эпитопу антигенраспознающей части молекулы антител (их идиотопу).
4- Основной клеточный механизм иммунорегуляции реализуется с участием супрессорных Т-клеток. Супрессорную функцию выполняют в основном С08+ - клетки. Главным объектом ихантигенспецифическогоин-
гибирующего влияния являются Т-хелперы. С08+ -Т-супрессоры оказыва ют свое влияние как путем контактных взаимодействий, так и через выде ление гуморальных факторов. С04+ -клетки также могут выступать в роли супрессоров, что проявляется во взаимном подавлении активности Т Ы - и Т112-хелперов. Супрессорной активностью обладают также активиро ванные макрофаги и ЫК-клетки.
4.2. Общая стратегия иммунной защиты
Существует два основных направления защитной деятельности им мунной системы при патологических ситуациях — формирование рези
стентности к инфекциям и предотвращение развития опухолей.
В случае внедрения патогенов инфекционной природы роль иммун ных механизмов на первых порах состоит в срочном ограничении их раз множения и распространения. Это достигается благодаря включению
108
факторов естественной резистентности, которые активируются самими микроорганизмами и их продуктами. Механизмы естественной резистен тности обеспечивают выживание организма в ранний период агрессии, но не способны эффективно устранить агрессивный агент. Поэтому в дальнейшем защита строится на сочетании факторов естественной ре зистентности и адаптивного иммунитета. При этом очень существенна адекватность выбора пути адаптивного ответа, направляемого хелперами первого или второго типов (ТМ, ТИ2) (табл. 4.1).
|
|
Таблица 4.1 |
Свойства С04-клеток (Т-хелперов) типов ТМ и ТЬ2 |
||
|
|
|
Показатели |
Т М |
ТИ2 |
|
|
|
Факторы, |
Высокие или низкие дозы |
Промежуточные дозы |
благоприятст |
антигена, высокая плотность |
антигена, низкая плотность |
вующие индукции |
антигена на поверхности АПК, |
антигена на поверхности |
|
действие ИЛ-12 и ИФН у |
АПК, действие ИЛ-4 |
Ключевые |
ИФНу, ИЛ-2, |
ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-10 |
цитокины |
Фнор |
|
Функции |
Обусловливают развитие ГЗТ, |
Обусловливают развитие |
|
цитотоксического ответа, |
гуморального иммунного |
|
активацию макрофагов, |
ответа, активацию эозино- |
|
подавление гуморального |
филов и тучных клеток, |
|
ответа |
подавление клеточного |
|
|
ответа |
Защитная роль |
При внутриклеточных |
При гельминтозах, |
|
инфекциях (вирусы, |
внеклеточных инфекциях |
|
микобактерии,лейшмании |
(энтеробактерии, клост- |
|
и т.д.), опухолях |
ридии, вибрионы), защита |
|
действия |
от эзотоксинов |
Повреждающая |
При аутоиммунных процессах, |
При аллергии, некоторых |
роль |
отторжении трансплантатов |
аутоиммунных процессах |
|
|
|
Условные обозначения: АПК — антигенпрезентирующие клетки, ИФН — интерферон, ФНО — фактор некроза опухоли.
I |
Т М - з а в иси м ы й клеточный ответ защищает организм от |
|
внутриклеточных патогенов, включая вирусы и микобакте- |
|
рии; он же обусловливает специфическую противоопухоле |
|
вую резистентность. ТЬ2-зависимая гуморальная защита |
|
эффективна при инфицировании внеклеточными патогена |
|
ми, в частности микроорганизмами, выделяющими экзоток- |
| |
сины, а также при паразитарных инвазиях. |
Неадекватное направление дифференцировки Т-хелперов обычно приводит к неэффективности иммунной защиты, что четко показано на примере лейшманиоза и проказы, при которых защита обусловлена уча стием ТМ-клеток, и преобладание ТИ2-зависимых механизмов опреде ляет неблагоприятное течение заболевания. Более подробно взаимодей ствие иммунной системы и инфекционных агентов рассматривается в курсе микробиологии.
109
В основе учения о противоопухолевом иммунитете лежит концеп ция иммунного надзора, согласно которой иммунная система постоянно контролирует «правильность» антигенной структуры собственных клеток организма, выявляет измененные молекулы и удаляет клетки, которые их несут. Включение иммунных механизмов при опухолевых процессах обус ловлено экспрессией при многих опухолях антигенов, не свойственных зрелому организму (не обязательно истинно чужеродных, чаще — эмб риональных), в том числе продуктов онкогенных вирусов
Основой противоопухолевой иммунной защиты служат мо билизация и активация естественных киллеров, атакжеТМ - ' зависимых механизмов, приводящих к формированию цитотоксичных Т-лимфоцитов и активированных макрофагов.
Антитела не выполняют защитной функции и могут ослабить клеточ- но-опосредованную защиту.
Опухолевые клетки располагают механизмами, которые позволяют им успешно избегать действия иммунных факторов. К этим механизмам относятся маскировка или утрата опухолеассоциированных антигенов, ослабление экспрессии молекул МНС-1, которые презентируют эти анти гены, отсутствие костимулирующих молекул, необходимых для активации Т-клеток, индукция супрессорных клеток, секреция ингибирующих фак торов различной природы, индукция специфической неотвечаемости (им мунологической толерантности) к антигенам опухоли
В конечном счете эффективность иммунной защиты против опухолей определяется балансом иммунных механизмов и средств самозащиты и маскировки опухолевых клеток.
На усилении иммунных механизмов основан ряд подходов к тера пии опухолей, в частности лечение цитокинами, некоторые методы генотерапии. Очевидно, частота злокачественных опухолей была бы значи тельно выше, если бы иммунный надзор отсутствовал. В пользу этого свидетельствует повышение частоты развития опухолей при подавлении иммунитета.
Таким образом, при биологической агрессии иммунная система вна чале мобилизует факторы естественной защиты, а затем подключает механизмы адаптивного иммунного ответа, развивающегося при поступ лении конкретных антигенов. При этом осуществляется выбор пути им мунного ответа, способного обеспечить наиболее эффективную защиту Известно четыре таких пути, обусловленных включением гуморальных и клеточных иммунных механизмов (два из них могут стать основой реак ций гиперчувствительности). Характеристика этих главных разновиднос тей иммунного ответа представлена в табл. 4.2.
|
|
|
Таблица 4 2 |
|
Основные типы иммунного ответа |
||
|
|
|
|
Тип ответа |
Т-хелперы |
Эффекторы |
Назначение |
|
|
|
|
Гуморальный |
Th2 |
Антителообразующие |
Защита от внеклеточных |
|
|
клетки (плазмоциты) |
микроорганизмов |
|
|
|
и токсинов |
110
Тип ответа |
Т-хелперы |
Эффекторы |
Назначение |
|
|
|
|
Гиперчувстви |
ТЬ2 |
1дЕ-продуцирующие, |
Защита от внеклеточных |
тельность |
|
тучные клетки, |
паразитов |
немедленного |
|
эозинофилы |
|
типа |
|
|
|
Цитотокси- |
ТЬО,ТМ |
Цитотоксические |
Защита от вирусов |
ческий |
|
С08+ -Т-клетки |
и опухолевых клеток |
Гиперчувстви- |
Т М |
С04+ -Т-клетки, |
Защита |
тельиость |
|
макрофаги |
от внутриклеточных |
замедленно! о |
|
|
микробов и паразитов |
типа |
|
|
|
|
|
|
|
И м м у н о л о г и ч е с к а я т о л е р а н т н о с т ь . Оптимальный исход при трансплантации несовместимых тканей связан с формированием имму нологической толерантности.
Под |
иммунологической |
толерантностью |
понимают |
отсутствие |
им |
|
мунной реакции |
на конкретный |
антиген, т.е. |
«терпимость» организма |
в |
||
отношении |
этого |
антигена. Наиболее ярким примером |
иммунологичес |
|||
кой толерантности является отсутствие иммунных реакций на собствен ные антигены организма
Биологический смысл и значимость этого феномена стали особен но очевидными после его искусственного воспроизведения при исполь зовании чужеродных антигенов. Эмбрионам мышей генетически чистой линии вводили суспензию клеток, полученных из селезенки и других ор ганов мышей другой линии. Через 1,5—2 мес после рождения им переса живали кожу от доноров той же линии. Лоскут не отторгался, тогда как в контроле отторжение происходило в течение 10—12 дней Аналогичные результаты получены в опытах с объединением кровеносной системы ку риных эмбрионов. Позже было показано, что у других животных толеран тность может быть индуцирована введением аллогенных клеток в первые сутки после рождения. Толерантность удалось индуцировать также у взрослых реципиентов при условии предварительной обработки факто рами, повреждающими лимфоидные клетки, — радиацией или введени ем иммунодепрессантов, например циклофосфамида.
Иммунологическая толерантность — это не простое состояние
иммунодепрессии, поскольку неотвечаемость распространяется только на антигены, использованные для индукции толерантности, при сохране нии способности к нормальному иммунному ответу на посторонние анти гены По-видимому, во всех случаях условием поддержания иммуноло гической толерантности к аллогенным тканям является установление химеризма кроветворных клеток. Отмена иммунологической толерантно сти может произойти спонтанно после удаления антигена, особенно в со четании с воздействиями, повреждающими лимфоциты, например облу чением.
Основой формирования иммунологической толерантности служит удаление клонов лимфоцитов, специфичных к соответствующим антиге-
111
нам, или индукция их устойчивой анергии. В индукции толерантности при нимают участие также супрессорные Т-лимфоциты, о чем свидетельст вуют данные о возможности переноса с Т-клетками состояния толе рантности. Искусственная иммунологическая толерантность может рассматриваться как аналог и экспериментальная модель естественной толерантности организма к собственным антигенам, которая также фор мируется в определенные периоды онтогенеза в результате процессов отрицательной селекции клонов Т-лимфоцитов.
4 . 3, Иммунодефицитные состояния
Как и любые системы организма, иммунная система подвержена па тологическим процессам. Выделяют четыре основных типа иммунопато логии:
—иммунная недостаточность (иммунодефициты) вследствие дефек тов развития или действия повреждающих факторов;
—гиперчувствительность, или измененная реактивность, основной формой которой является аллергия;
—аутоиммунная патология;
—опухоли иммунной системы, прежде всего лимфопролиферативные процессы.
Ниже будут кратко охарактеризованы иммунодефициты, аутоиммун ные и лимфопролиферативные процессы.
Иммунодефициты разделяют на две группы — первичные (врожден
ные), как правило, имеющие наследственную природу, и вторичные (при обретенные), вызванные различными воздействиями, как эндогенными (болезни), так и экзогенными (действием агрессивных физических и хи мических факторов). Наиболее характерным клиническим проявлением иммунодефицитов служит высокая подверженность заболеваниям, вы зываемым микроорганизмами, в частности простудным; для иммунодефицитных состояний характерна связь инфекционных заболеваний с оп портунистическими агентами (т.е. сапрофитами, в норме непатогенными). При некоторых формах иммунодефицитов повышается риск развития опухолей.
4 . 3 . 1 . Первичные иммунодефициты
|
Гоуппу первичных |
иммунодефицитов |
образуют |
заболевания, |
в |
ос |
|
нове |
которых лежит наследственно |
обусловленная |
дефектность |
структу |
|||
ры и |
функционирования |
иммунной |
системы, |
которая |
проявляется |
в |
нару |
шении |
иммунной защиты. |
|
|
|
|
|
|
Первичные иммунодефициты — это очень редкие состояния (при мерно 1 больной на 1 ООО ООО человек). Они являются почти исключитель но уделом детского возраста, поскольку значительная часть больных с тяжелыми формами иммунодефицитов не доживает до 20 лет, а при бо лее легких формах иммунологические дефекты с возрастом в определен ной степени компенсируются.
112
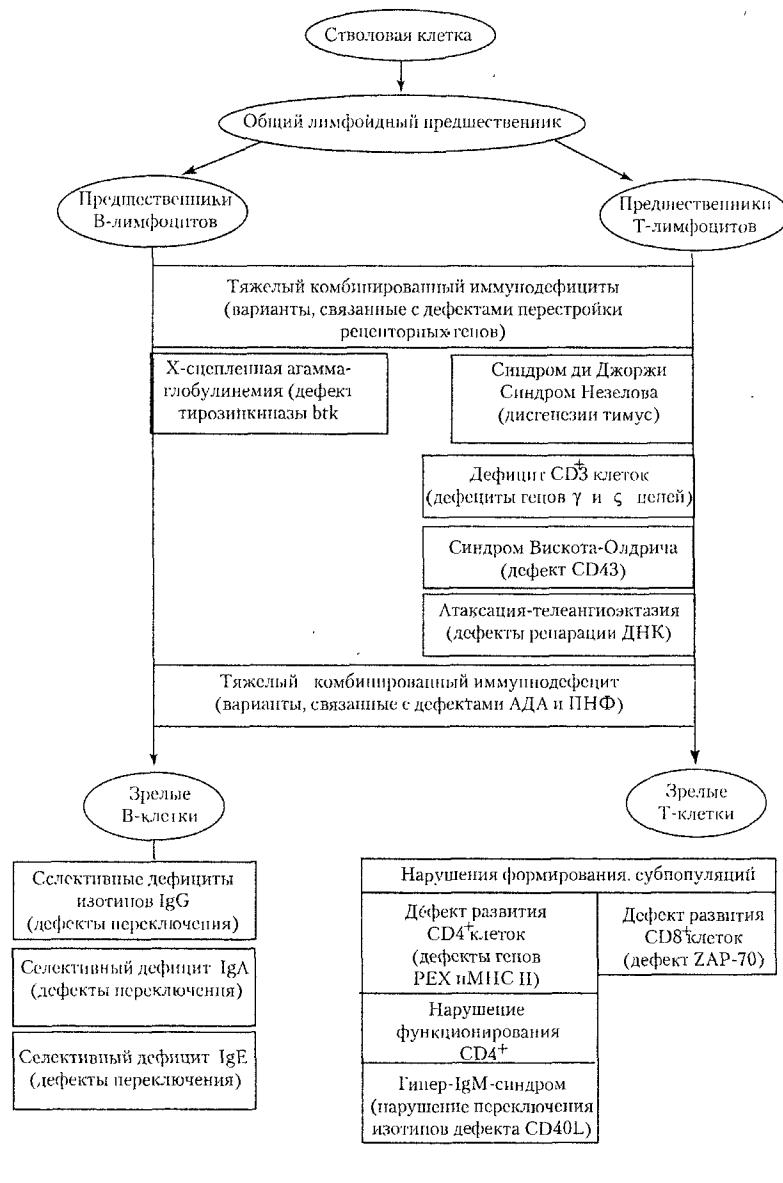
Как правило, в основе первичных иммунодефицитов лежит генети чески обусловленный блок развития клеток иммунной системы или выпа дение важных иммунных процессов вследствие дефекта определенных молекул, например ферментов или мембранных структур (схема 4.3).
Схема 4.3. Связь первичных иммунодефицитов с нарушением развития лимфоцитов на определенных стадиях.
113
Первичные иммунодефициты можно разделить по преобладающему типу поражений звеньев иммунной системы на 3 типа:
—комбинированные иммунодефициты;
—иммунодефициты с преимущественным поражением клеточного иммунитета;
—преимущественно гуморальные иммунодефициты.
Кпервым относят заболевания, в основе которых лежат генетичес кие дефекты, затрагивающие различные линии дифференцировки лим фоцитов, а также ранние этапы их развития, общие для Т- и В-линий. Во вторую группу входят иммунодефициты, при которых нарушается разви тие Т-клеток и страдают опосредуемые ими реакции клеточного иммуни тета; к этой же группе относятся дефекты фагоцитирующих клеток. В груп пу гуморальных иммунодефицитов включают патологию, в основе которой лежит нарушение развития В-клеток и Т-хелперов гуморального ответа, а также патологию компонентов комплемента.
Впоследние годы выясняются молекулярные основы поражения при первичных иммунодефицитах. Одной из первых была расшифрована при рода комбинированных иммунодефицитов, связанных с недостаточ ностью ферментов пуринового метаболизма. Известны варианты таких дефектов, обусловленные мутациями генов, кодирующих аденозиндезаминазу и пуриннуклеотидфосфорилазу. Основой другой формы тяжело го комбинированного иммунодефицита, затрагивающего Т- и В-ростки лимфопоэза, служит дефект процесса перестройки генов антигенраспознающих рецепторов, связанный с отсутствием ферментов рекомбиназ, которые катализируют этот процесс.
Очень разнообразен спектр генетически обусловленных нарушений выработки антител. Их причиной может быть как поражение В-лимфоци тов (их развития или экспрессии генов иммуноглобулинов), так и дефект ность Т-клеток (ослабление хелперной активности). Примером первого рода может служить агаммаглобулинемия Брутона, сцепленная с Х-хро- мосомой. Ее основой являются мутации гена, детерминирующего фер мент тирозинкиназу Ык, которая связана с антигенраспознающим ре цептором В-лимфоцитов. Отсутствие этой тирозинкиназы делает невозможным развитие В-лимфоцитов уже на самых ранних стадиях.
В основе другого первичного иммунодефицита — гипер-1дМ-синд- рома лежит дефект С0154 — молекулы, появляющейся на поверхности Т-клеток при их активации; в результате ее взаимодействия с молекулой СР40 поверхности В-лимфоцитов в эти клетки передается сигнал, обес печивающий их дифференцировку в антителообразующие клетки, а так же переключение изотипов секретируемых антител. В отсутствие этого сигнала происходит синтез иммуноглобулинов только одного изотипа — 1дМ, что сопровождается ослаблением гуморального иммунного ответа. Существуют формы гуморальных иммунодефицитов, при которых нару шено образование иммуноглобулинов какого-либо одного изотипа. Сре ди таких селективных дефектов наиболее частым является дефицит 1дА.
114
При нем присутствуют В-лимфоциты, несущие мембранный 1дА, однако не образуются плазматические клетки, секретирующие 1дА-антитела.
РЯД комбинированных иммунодефицитов возникает при локализо ванных дефектах генов мембранных молекул адгезии. Следствием таких мутаций является нарушение миграции клеток, в первую очередь нейтрофилов и моноцитов/макрофагов, а также их взаимодействий с клетками других типов. Примером могут служить сходные поражения, развиваю щиеся как результат наследственных дефектов экспрессии (Р2 -интегри- нов и углеводных детерминант, распознаваемых селектином 1_. Эти пора жения представляют собой два варианта (-АО-синдрома — дефицит адгезии лейкоцитов, признаком которого является ослабление функции нейтрофилов, и повышение чувствительности к гнойным инфекциям.
Дефекты компонентов комплемента представлены вариантами с по ражением практически всех основных факторов классического и альтер нативного путей активации комплемента. Как правило, выпадение еди ничных компонентов системы комплемента проявляется в умеренном снижении устойчивости к некоторымвозбудителям. Лишь дефицит инги битора С1 ц сопровождается развитием ангионевротического отека, обус ловленного накоплением вазоактивных пептидов С5а и СЗа.
Иммунодефициты, в основе которых лежит дефект генов цитокинез, немногочисленны, что связано с «избыточностью» системы цитокинов, которая обусловлена взаимозаменяемостью их функций. Лишь когда ге нетический дефект затрагивает функцию многих цитокинов, это прояв ляется в тяжелых расстройствах иммунитета, что происходит, например, при дефекте гена у-Цвпи, общей для рецепторов интерлейкинов 2, 4, 7, 13и 15.
В результате дефекта, затрагивающего ген мембранного сиалопротеина С043, развивается синдром Вискотта—Олдрича, о чем свидетель ствует тромбоцитопения с геморрагическим синдромом в сочетании с экземой и комбинированным иммунодефицитом. При этом заболевании аномально функционирует цитоскелет, что отражается на подвижности клеток и межклеточных взаимодействиях, важных для осуществления иммунных процессов.
При атаксии-телеангиэктазии наблюдается поражение различных функций, обусловленное слабостью аппарата репарации ДНК и неста бильностью хромосом, а также дефектами клеточного цикла. Это дает неожиданное сочетание симптомов: комбинированный иммунодефицит (недоразвитие вилочковой железы, дефицит Т-клеток и иммуноглобули нов «поздних» изотипов — 1д02, 1д04, 1дЕ, 1дА), неврологические откло нения (атаксия), поражение сосудистой стенки (телеангиэктазии), нару шение пигментации.
Помимо рассмотренных «точечных» поражений иммунной системы известны первичные иммунодефициты, развитие которых обусловлено множественными дефектами, затрагивающими формирование в эмбри огенезе различных органов, включая органы иммунной системы. Так, нас ледственный порок, приводящий к нарушению развития у эмбрионов ч^-
ловека производных 3 и 4 жаберных щелей, служит основой синдрома Ди Джорджи с дефектом развития вилочковой железы (она не заселяется предшественниками Т-клеток, развитие которых прерывается на костно мозговой стадии) и гистогенетически родственных органов (паращитовидных желез и т.д).
Основным симптомокомплексом, отражающим нарушение иммун ной защиты при первичных иммунодефицитах, является инфекционный синдром, т.е. понижение резистентности к инфекционным агентам, в том числе сапрофитным (Pneumocystis cannii, Candida, цитомегаловирус, не которые энтеровирусы). Характер нарушений иммунной защиты опреде ляется локализацией поражения в иммунной системе. Так, при блокаде процесса перестройки рецепторных генов отсутствуют как Т-, так и В-клет ки и не развиваются ни клеточные, ни гуморальные формы иммунного ответа. При селективных дефектах определенных классов лимфоцитов, а также их субпопуляций выпадают именно те иммунологические функции, за которые ответственны поражаемые типы клеток. При блокаде разви тия В-клеток развивается агаммаглобулинемия с нарушением гумораль ной защиты от внеклеточных бактерий и их токсинов, а при дефицитах Т-лимфоцитов страдает клеточная защита от вирусов и микобактерий. При некоторых формах первичных иммунодефицитов (атаксия-телеангиэкста- зия, синдром Вискотта-Олдрича и т.д.) значительно повышается риск раз вития злокачественных опухолей (до 10—15%). Нередко нарушения им мунологических функций регистрируются при нормальной численности соответствующих клеток.
Клинико-иммунологическое обследование дает четкие результаты лишь при тех формах первичных иммунодефицитов, при которых точно локализован дефект. Так, при тяжелом комбинированном иммунодефи ците отсутствуют как Т-, так и В-клетки, при синдроме Ди Джорджи резко снижено содержание Т-лимфоцитов, а при агаммаглобулинемиях— В-лимфоцитов. По изменению концентрации иммуноглобулинов в сыво ротке или компонентов комплемента различных изотипов может быть ус тановлена локализация дефекта в системе гуморального иммунитета. Все большую диагностическую значимость приобретает определение конк ретных мембранных маркеров клеток иммунной системы (молекул адге зии, CD154, CD43 и т.д.), а также методы, позволяющие выявить мутации конкретных генов.
4.3.2. Вторичные иммунодефициты
Вторичные, |
или |
приобретенные, |
иммунодефициты |
определяют как |
||||||
нарушение |
иммунной |
защиты |
организма, |
развивающееся |
в |
пост- |
||||
натальном |
периоде |
вследствие |
действия |
внешних |
или |
внутренних |
||||
факторов, |
непосредственно |
не |
связанных с генетическим |
аппа |
||||||
ратом. |
|
|
|
|
|
|
|
|
|
|
Фактически эти иммунодефициты лишены самостоятельности и рас сматриваются как состояния, сопутствующие известным заболеваниям или действию повреждающих факторов.
116
Роль наследственного фактора в развитии вторичных иммунодефи цитов не исключается, поскольку чувствительность иммунной системы к действию факторов, вызывающих формирование иммунодефицитных состояний, варьирует часто и зависит от наследственности. Однако на следственные факторы сами по себе, без действия индуктора, недоста точны для проявления вторичного иммунодефицита.
Вторичные иммунодефицитные состояния чрезвычайно широко рас пространены: в большей или меньшей степени отклонения в иммунной системе сопутствуют всем заболеваниям, особенно вирусным, ряду эн докринных и метаболических поражений и т.д. Они проявляются при дей ствии большинства экстраординарных внешних агентов (классический пример — пострадиационный иммунодефицит), втом числе неблагопри ятных экологических факторов. Известны физиологические иммунодефи циты, свойственные раннему постнатальному и старческому возрастам, а также иммунодефициты, связанные со стрессом. Главное проявление вторичных (как и первичных) иммунодефицитов состоит в понижении ус тойчивости к инфекционным агентам, в частности к оппортунистическим, со склонностью кхронизации воспалительных процессов. В ряде случаев регистрируется повышение частоты развития злокачественных опухолей.
Основой многих проявлений вторичных иммунодефицитов является гибель клеток иммунной системы, которая может реализоваться в форме некроза (гибель вследствие наруше ния целости мембраны) или апоптоза (гибель в результате деградации ДНК, обусловленной собственными фермента ми клетки).
Апоптоз лимфоцитов развивается при действии многих лечебных химиопрепаратов, облучения, а также кортикостероидов, уровень которых существенно повышается при стрессовых состояниях. Другой механизм инактивации клеток иммунной системы состоит в их функциональной бло каде, достигаемой связыванием с поверхностью клетки или накоплени ем внутри клетки агентов, ингибирующих их активность. Их роль могут выполнять аутоантитела, цАМФ, простагландины и другие медиаторы воспаления, некоторые цитокины, супрессорные и «блокирующие фак торы» опухолей, ингибирующие продукты патогенов.
Наконец, основой вторичных иммунодефицитных состояний может стать дисбаланс клеток иммунной системы — эффекторныхи супрессорных клеток, субпопуляций С04+ - и С08+ Т-лимфоцитов, Т-хелперов ТМ - и ТИ2-типов. Снижение соотношения С04+ /С08+ , иногда обозначаемого как иммунорегуляторный индекс, регистрируется при ряде заболеваний; это может быть обусловлено какснижением численности С04+-хелперов вслед ствие ослабления функции вилочковой железы и других причин, так и по вышением содержания С08+ -лимфоцитов, которое может сопровождать ся превалированием супрессорной активности. Дисбаланс хелперов типов ТМ и ТИ2 приводит к преобладанию гуморального или клеточного типа иммунной защиты, который может оказаться неадекватным при конкрет ной форме инфекции, о чем уже говорилось выше. Среди заболеваний,
117
