
- •Лабораторная работа №2. Получение казеина из молока. Метод формольного титрования. Материал, реактивы, оборудование.
- •Лабораторная работа №4. Определение содержания белков колометрическими методами. Материал, реактивы, оборудование.
- •1. Осаждение белков раствором тху.
- •2. Осаждение белков при изменении pH среды.
- •Лабораторная работа 3. Экстракция, выделение и очистка белков от примесей гель-фильтрацией на сефадексе g-50.
- •1. Калибровка колонки.
- •Фракционирование водного экстракта олода.
- •Лабораторная работа №1. Выделение кофеина из чая и перекристаллизация его из воды.
- •Лабораторная работа №5. Идентификация углеводов по функциональным группам.
- •Функциональный анализ.
- •Лабораторная работа №6. Определение углеводов методом тонкослойной хроматографии.
- •Лабораторная работа №7. Кислотный гидролиз крахмала.
- •Методика проведения анализа.
- •Лабораторная работа №8. Синтез слизевой кислоты.
- •Лабораторная работа №9. Определение физико-химических показателей качества жиров и масел.
- •Лабораторная работа №10. Анализ группового состава пищевых жиров и масел.
- •Экстракция липидов из пищевого объекта и определение их группового состава.
Экстракция липидов из пищевого объекта и определение их группового состава.
Материалы и реактивы: пищевое сырьё и пищевые продукты, гексан, хлороформ, диэтиловый эфир, уксусная кислота ледяная, 5%-ный раствор фосфорно-молибденовой кислоты в этаноле, хроматографические пластины «Силуфол», фильтровальная бумага.
Приборы и химическая посуда: весы лабораторные, денситометр, термостат, водяная баня, качалка, колбы стеклянные конические плоскодонные вместимостью 100 см3 с притёртой пробкой, воронка коническая, колба круглодонная одногорлая вместимостью 100 см3, насадка Вюрца, прямой холодильник (Либиха), аллонж, приёмная колба, термометр, микрошприц, хроматографическая камера с прошлифованной крышкой.
Цель работы: выделение липидов методом экстракции из конкретного пищевого объекта, определение количественного содержания липидов в объекте и анализ группового состава липидов.
Экстракция липидов из пищевого объекта.
Методика выполнения анализа. Навеску измельчённого продукта массой 4г помещают в стеклянную колбу с притёртой пробкой вместимостью 100 см3. В колбу приливают 40 см3 гексана, закрывают колбу притёртой пробкой и интенсивно встряхивают на качалке в течение 30 мин. По истечении указанного времени полученный экстракт фильтруют через складчатый фильтр на конической воронке.
Отфильтрованный экстракт переносят в сухую, предварительно взвешенную круглодонную колбу вместимостью 100 см3, собирают прибор для прямой перегонки и отгоняют растворитель на водяной бане при температуре ~80ОС до полного испарения гексана. Затем колбу с липидами высушивают в вакуум-сушильном шкафу при температуре не выше 70ОС в течение 50 мин.
Колбу взвешивают и определяют количество липидов в пробе. Полученные данные вносят в табл. 3.1.
Таблица 3.1
|
Наименование образца |
Масса, г |
Количество липидов | |||
|
образца |
пустой колбы |
колбы с липидами |
г |
% | |
|
Зерно |
|
|
|
|
|
|
Мука свежая |
|
|
|
|
|
|
Хлеб |
|
|
|
|
|
|
Макаронные изделия |
|
|
|
|
|
Определение группового состава липидов.
Извлекаемое растворителями из пищевого объекта смесь состоящая из различных групп липидов и растворённых в них сопутствующих веществ, условно называется сырым жиром. Сырой жир включает три-, ди- и моноацилглицерины, свободные жирные кислоты, стерины, фосфолипиды, жирорастворимые пигменты, жирорастворимые витамины, возки, углеводороды и другие группы или фракции липидов. Для анализа качественного и количественного группового (фракционного) состава липидов часто применяют метод тонкослойной хроматографии на пластинах «Силуфол».
Методика выполнения анализа. Выделенные из пищевого объекта липиды растворяют в хлороформе до получения 2%-ного раствора.
Пластинки «Силуфол» предварительно окрашивают фосфорно-молибденовой кислотой, опуская их в 5%-ный раствор кислоты в этаноле, и затем высушивают на воздухе.
На подготовленную пластину «Силуфол» с помощью микрошприца наносят 1мкл (10-6 см3) 2%-ного раствора липидов в хлороформе в виде сплошной узкой полосы длиной до 7мм на линию старта. Линию старта предварительно намечают на расстоянии ~10мм от нижнего и боковых краёв пластины.
Разделение проводят в стеклянной камере с прошлифованной крышкой. Камеру заполняют системой растворителей до высоты не более 5мм для того, чтобы растворитель не касался стартовой линии пластины. Пластину с нанесёнными образцами липидов помещают в камеру, вертикально погружая в разделительную смесь, и оставляют в ней до тех пор, пока высота подъёма фронта растворителя не достигнет отмеченной длины разделительного пути. Разделительный путь (расстояние от линии старта до линии фронта растворителя фронта) равен для пластины «Силуфол» ~90мм.
Разделение проводят в системе растворителей гексан-диэтиловый эфир-уксусная кислота в соотношении 80:20:1. После окончания хроматографического разделения пластину вынимают из камеры и сушат в горизонтальном положении до полного испарения остатков растворителей.
Проявление пластин проводят в термостате в течение 5-10 минут при температуре 60ОС. Идентификацию фракций проводят с помощью стандартных веществ – свидетелей или по значению Rf для данной системы растворителей.
Результаты идентификации приводят в табл. 3.2.
Таблица 3.2
Идентификация группового состава липидов исследуемых образцов.
|
№№ п/п |
Группы липидов |
Значение Rf | ||||
|
по литератур-ным данным |
исследуемых образцов липидов | |||||
|
образец №1 |
образец №2 |
образец №3 | ||||
|
1 |
Полярные липиды (глико- и фосфолипиды) |
на старте |
|
|
| |
|
2 |
Моноацилглицерины |
0,02 |
|
|
| |
|
3 |
1,2-диацилглицерины 1,3-диацилглицерины |
0,13-0,21 |
|
|
| |
|
4 |
Свободные жирные кислоты |
0,39 |
|
|
| |
|
5 |
Триацилглицерины |
0,60 |
|
|
| |
|
6 |
Эфиры стеринов, углеводороды |
0,94 |
|
|
| |
Количественную оценку группового состава липидов осуществляют на специальном приборе – денситометре, позволяющем получить результат измерений в виде графической записи (денситограммы).
При расчёте концентраций компонентов исследуемой смеси используют метод внутренней нормализации.
Концентрация каждого компонента смеси в относительных процентах вычисляется по формуле:
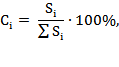
где Si – геометрическая площадь соответствующего пика на денситограмме.
Результат вычислений приводится в табл. 3.3.
Таблица 3.3
Количественный групповой состав липидов (по данным денситограмм).
|
№№ п/п |
Группы липидов |
Относительное содержание групп липидов в исследуемых образцах, % | ||
|
Исследуемые образцы липидов | ||||
|
образец №1 |
образец №2 |
образец №3 | ||
|
1 |
Полярные липиды (глико- и фосфолипиды) |
| ||
|
2 |
Моноацилглицерины |
| ||
|
3 |
1,2-диацилглицерины 1,3-диацилглицерины |
| ||
|
4 |
Свободные жирные кислоты |
| ||
|
5 |
Триацилглицерины |
| ||
|
6 |
Эфиры стеринов, углеводороды |
| ||
На основании результатов работы делают выводы о содержании липидов в исследуемых пищевых объектах, групповом составе липидов и относительном содержании отдельных групп липидов.
