
- •Методические указания к самостоятельной работе
- •1. Строение вещества
- •1.1 Краткие теоретические сведения по номенклатуре химических соединений
- •1.2. Задачи для решения
- •1.2.1. По названию вещества написать его формулу.
- •1.2.2. Назвать соединения:
- •1.2.3. Написать в молекулярной и ионно-молекулярной формах уравнения реакций.
- •1.2.4. Закончить и уравнять реакцию; уравнение реакции представить в молекулярной и ионной формах:
- •2. Окислительно-восстановительные реакции
- •2.1. Примеры решения задач
- •2.2. Задачи для решения
- •2.2.1. Уравнять окислительно-восстановительную реакцию методом полу-реакций.
- •2.2.2. Написать уравнения окислительно-восстановительных реакций и расставить коэффициенты, пользуясь методом полу-реакций.
- •3. Общие закономерности химических процессов
- •3.1 Примеры решения задач
- •3 Моль NaOh1 мольFeCl3
- •0,24 Моль NaOhх мольFeCl3,
- •3.2 Задачи для решения
- •3.2.1. Выполнить расчеты по химической формуле вещества
- •3.2.2. Выполнить расчеты с использованием закона эквивалентов
- •3.2.3. Решить задачу с использованием расчетов по уравнению реакции
- •4. Растворы
- •4.1 Примеры решения задач
- •4.2 Задачи для решения
- •4.2.1. Выразить концентрацию заданного раствора всеми возможными способами
- •4.2.2. Выполнить расчет приготовления раствора.
- •4.2.3. Выполнить расчет концентрации раствора с учетом протекания химической реакции
- •5. Равновесия в растворах электролитов
- •5.1 Примеры решения задач
- •5.2 Задачи для решения
- •5.2.1. Вычислить рН раствора сильного электролита
- •5.2.2. Определить pH и степень диссоциации предложенного раствора слабого электролита
- •Темы контрольной работы
- •Пример задания контрольной работы
4. Растворы
4.1 Примеры решения задач
Пример 1. Раствор серной кислоты в воде с концентрацией 16 % (мас.) имеет плотностьd= 1,109 г/см3. Выразить концентрацию этого раствора всеми способами.
Решение. Выделим мысленно 1 кг раствора и найдем его объем:
![]()
![]() .
.
Найдем массу растворенного вещества (H2SO4):
![]()
Вычислим концентрацию раствора серной кислоты в г/л:
![]()
Найдем количество молей серной кислоты:

и вычислим молярную концентрацию раствора серной кислоты:
![]()
Найдем массу растворителя (Н2О):
![]()
и вычислим моляльную концентрацию раствора серной кислоты:
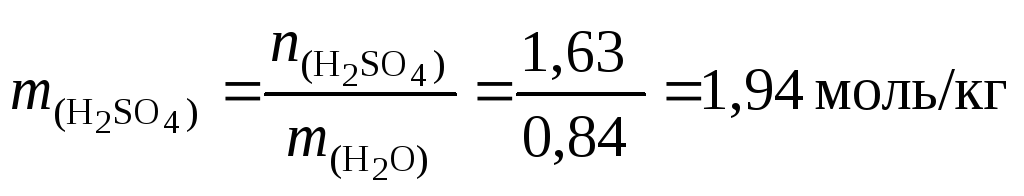 .
.
Найдем количество молей воды:
 .
.
Найдем мольную долю серной кислоты:
 .
.
Определим нормальную концентрацию раствора серной кислоты (для серной кислоты количество обменных эквивалентов в одном моле вещества z= 2):
![]() .
.
Пример 2.Какой объем раствора серной кислоты концентрацией 10 % (d = 1,066 г/см3) требуется для приготовления 200 мл 1 н. раствора?
Решение. Найдем массу серной кислоты, содержащейся в 200 мл 1 н. раствора. Для этого вычислим молярную концентрацию раствора:
![]() ,
,
количество вещества серной кислоты
![]()
и ее массу
![]() .
.
Вычислим объем 10 % раствора:
 .
.
Пример 3.Какой объем раствора серной кислоты концентрацией 0,42 моль/л потребуется для нейтрализации 20 мл раствора гидроксида калия концентрацией 6 % (d= 1,053 г/см3)?
Решение. Составим уравнение реакции:
2KOH+H2SO4=K2SO4+ 2H2O
Найдем количество вещества KOH
![]()
По уравнению реакции на 2 моль KOHприходится 1 моль Н2SO4, следовательно, для реакции с 0,02 моль гидроксида калия требуется 0,01 моль серной кислоты.
Найдем объем раствора серной кислоты:

4.2 Задачи для решения
4.2.1. Выразить концентрацию заданного раствора всеми возможными способами
|
|
Al2(SO4)3 |
0,15 экв/л |
1,009 |
|
|
Al(NO3)3 |
5,47 г/л |
1,01 |
|
|
AlCl3 |
0,041 моль/кг |
1,007 |
|
|
BaCl2 |
1,69 моль/л |
1,28 |
|
|
Ba(NO3)2 |
0,525 моль/л |
1,092 |
|
|
CaCl2 |
22 % |
1,203 |
|
|
Ca(NO3)2 |
2% |
1,01 |
|
|
CdCl2 |
0,5 моль/л |
1,08 |
|
|
CrCl3 |
0,6 экв/л |
1,022 |
|
|
Cr2(SO4)3 |
0,3 моль/л |
1,021 |
|
|
Cr(NO3)3 |
3% |
1,02 |
|
|
CuSO4 |
1,037 моль/кг |
1,206 |
|
|
CuCl2 |
0,04 моль/л |
1,009 |
|
|
Cu(NO3)2 |
1,037 экв/л |
1,20 |
|
|
FeSO4 |
0,3 экв/л |
1,02 |
|
|
Fe2(SO4)3 |
0,3 моль/л |
1,03 |
|
|
Fe(NO3)3 |
0,3 % |
1,0 |
|
|
H2SO4 |
15 % |
1,1 |
|
|
H3PO4 |
24 % |
1,14 |
|
|
HCl |
0,4 мол. % |
1,002 |
|
|
Hg(NO3)2 |
0,25 моль/л |
1,174 |
|
|
K2Cr2O7 |
0,18 моль/кг |
1,033 |
|
|
KMnO4 |
0,25 экв/л |
1,027 |
|
|
KOH |
6,3 мол. % |
1,147 |
|
|
MgSO4 |
20 % |
1,219 |
|
|
MgCl2 |
2 % |
1,02 |
|
|
Mg(NO3)2 |
0,05 моль/л |
1,01 |
|
|
MnSO4 |
1 % |
1,0 |
|
|
Na2CO3 |
41,34г/л |
1,019 |
|
|
NaBr |
26 % |
1,21 |
|
|
NaCl |
4,5% |
1,03 |
|
|
NaOH |
13 % |
1,142 |
|
|
NH4OH, |
9 % |
0,961 |
|
|
Pb(NO3)2 |
30 % |
1,328 |
|
|
ZnSO4 |
87 г/л |
1,084 |
