
- •Министерство образования и науки рф
- •Предмет коллоидной химии
- •Глава I.Дисперсные системы:
- •1.1 Основные свойства дисперсных систем
- •1.2 Классификация дисперсных систем
- •Классификация по степени дисперсности
- •Классификация по агрегатному состоянию
- •Классификация по структурно-механическим свойствам
- •Раздел II. Поверхностные явления. Адсорбция
- •2.1 Классификация поверхностных явлений
- •Классификация поверхностных явлений
- •2.2 Поверхностное явление – адсорбция
- •2.2.1 Основные понятия и определения
- •2.2.2 Адсорбция на границе жидкость-газ
- •2.2.3. Адсорбция на твердом адсорбенте
- •2.3 Адгезия и смачивание
- •Раздел III. Электрические свойства дисперсных
- •3.1 Возникновение электрического заряда
- •3.2 Современные представления о строении
- •3.3Строение мицеллы гидрофобного золя
- •3.4. Факторы, влияющие на электрокинетический потенциал
- •3.4.1 Влияние температуры
- •3.4.2 Влияние электролитов
- •3.4.3 Влияние рН среды
- •3.4.4 Влияние природы дисперсионной среды
- •3.5 Электрокинетические явления
- •3.5.1 Электрофорез
- •3.5.2 Потенциал седиментации
- •3.5.3 Электроосмос
- •3.5.4 Потенциал течения
- •Раздел IV. Устойчивость и нарушение устойчивости лиофобных золей
- •4.1. Седиментационная устойчивость
- •4.2 Агрегативная устойчивость и коагуляция
- •4.2.1 Теория устойчивости гидрофобных золей длфо
- •4.2.2 Факторы, определяющие агрегативную устойчивость
- •4.3. Коагуляция гидрофобных дисперсных систем
- •4.3.1 Коагуляция золей электролитами
- •Явление неправильных рядов
- •4.3.2 Кинетика коагуляции
- •Теория быстрой коагуляции Смолуховского
- •Константа скорости медленной коагуляции
- •Раздел V. Оптические свойства дисперсных систем
- •5.1. Рассеяние света
- •Теория светорассеяния Рэлея
- •5.2. Поглощение света и окраска золей
- •5.3. Оптические методы исследования коллоидных растворов
- •Раздел VI. Молекулярно-кинетические свойства
- •6.1. Броуновское движение
- •6.2. Диффузия
- •6.3. Осмос
- •Раздел VII. Виды дисперсных систем
- •7.1. Растворы высокомолекулярных соединений (вмс)
- •7.1.1. Классификация вмс
- •7.1.2. Особенности строения полимеров
- •7.1.3. Набухание вмс
- •Термодинамика набухания
- •Кинетика набухания
- •Факторы, влияющие на набухание
- •7.1.4. Свойства растворов вмс
- •7.2. Коллоидные пав. Мицеллообразование в растворах пав
- •Применение коллоидных пав
- •7.3. Эмульсии
- •7.3.1. Классификация эмульсий
- •7.3.2. Методы получения эмульсий
- •7.3.3. Устойчивость эмульсий
- •Типы эмульгаторов
- •7.3.4. Применение эмульсий
- •7.4. Пены
- •7.4.1. Основные характеристики и классификация пен
- •7.4.2. Устойчивость пен
- •7.4.3. Методы разрушения пен
- •7.4.4. Практическое применение пен
- •7.5. Золи и суспензии
- •7.6. Порошки
- •7.6.1. Основные свойства и устойчивость порошков
- •7.6.2. Практическое применение порошков
- •Раздел VIII. Структурообразование в дисперсных системах
- •8.1. Типы структур в дисперсных системах
- •8.2. Особенности структурообразования в растворах вмс. Студни и студнеобразование
7.1.3. Набухание вмс
При контакте полимера с растворителями происходит его набухание.
Набухание– это самопроизвольный процесс поглощения низкомолекулярного растворителя высокомолекулярным веществом, сопровождающийся увеличением массы и объёма полимера.
Явление набухания обусловлено сильным различием подвижностей молекул растворителя и ВМС: малые молекулы растворителя быстро проникают в полимер, раздвигая цепи. Полярные полимеры набухают в полярных жидкостях (например, белки в воде), неполярные – в неполярных (каучук в бензоле).
Количественная характеристика набухания – степень набухания i– величина, показывающая относительное увеличение массы ВМС при набухании:
![]() или
или![]()
где m0,V0– масса и объём сухого полимера;m,V– масса и объём набухшего полимера.
Набухание может быть ограниченным и неограниченным.
При ограниченном набуханииmиiдостигают постоянных при данных условиях (температуре, концентрации, рН) предельных значенийm∞иi∞и далее не меняются (рис. 51, кривая1).
При неограниченном набуханииmиiдостигают максимальных значений, которые затем уменьшаются за счёт растворения полимера (рис. 51, кривая2). Таким образом, в этом случае набухание является первой стадией растворения.

Набухание протекает в две стадии.
Первая – стадия гидратации(сольватации); на этой стадии молекулы
растворителя адсорбируются на поверхности
ВМС, происходит сольватация макромолекул.
При этом выделяется т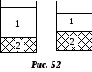 еплота
набухания
(ΔH< 0), и
наблюдаетсяконтракция– уменьшение
объёма системы в результате сжатия
растворителя1в сольватных оболочках
и образованием связанной жидкости
наряду с увеличением объёма полимера2 (рис. 52).
еплота
набухания
(ΔH< 0), и
наблюдаетсяконтракция– уменьшение
объёма системы в результате сжатия
растворителя1в сольватных оболочках
и образованием связанной жидкости
наряду с увеличением объёма полимера2 (рис. 52).
Вторая стадия – осмотическая. Растворитель диффундирует внутрь матрицы ВМС, внутри ВМС возникает большое осмотическое давление. На этой стадии теплота не выделяется. Если межмолекулярные связи сильные и их много, ВМС набухает, достигаяm∞иi∞. Происходит ограниченное набухание. Если все связи слабые, полимер набухает и полностью растворяется.
Ограничено набухают полимеры, имеющие разветвлённую и пространственную структуру, а также химические связи между молекулами – “мостики”, которые не позволяют молекулам полимера отделиться друг от друга. Образуется студень.
Жидкость, заполняющую сетку студня, называют интермицеллярной. Она состоит из связанной, образующей гидратные (сольватные) оболочки, и свободной, или капиллярной. Количество связанной воды зависит от гидрофильности макромолекул. Чем больше полярных групп, тем больше связанной воды. С течением времени наблюдается старение набухших полимеров, проявляющееся в постепенном сжатии сетки (матрицы), в результате чего отделяется мицеллярная жидкость. Этот процесс называетсясинерезисом.
Термодинамика набухания
Процесс набухания идёт самопроизвольно, т.е при р,Т=const
ΔG< 0,
ΔG= ΔH–TΔS. (7.1)
На первой стадии энтропия практически не меняется или незначительно уменьшается за счёт контракции, т.е ΔSI≈ 0. Поэтому снижение энергии Гиббса в самопроизвольном процессе происходит за счет уменьшения энтальпии: ΔНI< 0, следовательно, происходит выделение теплоты. Таким образом, на стадии сольватации преобладает энтальпийный фактор.
На второй стадии выделение теплоты уменьшается, но возрастает энтропия системы ΔSII> 0, т.к. разрыхление сетки полимера увеличивает число возможных конформаций. Таким образом, энергия Гиббса системы снижается за счет увеличения энтропии:
ΔGII = –TΔSII< 0,
Следовательно, вторая стадия набухания обусловлена энтропийным фактором.
