
- •Дисциплина: Общая и неорганическая химия
- •1 Моль вещества э(эквивалента) - содержит 6,02*1023э(эквивалентов)
- •Объединенный газовый закон
- •Уравнение Клайперона-Менделеева
- •Закон Дальтона
- •3.Окислительно-восстановительные реакции. Степень окисления. Окислители, восстановители. Типы окислительно-восстановительных реакций
- •Основные положения теории о-в процессов:
- •Окислительно-восстановительные свойства элементов
- •Виды окислительно-восстановительных реакций
- •4. Растворы. Насыщенные и ненасыщенные растворы. Способы выражения содержания растворенного вещества в растворе (массовая и мольная доли; молярная, эквивалентная, моляльная концентрации; титр)
- •Способы выражения концентрации растворов
- •Теории растворов
- •5.Гидролиз растворов солей. Степень гидролиза и факторы, влияющие на нее. Типичные случаи гидролиза (показать на примерах).
- •Соль слабого основания и сильной кислоты (nh4no3, ZnCl2, Al2(so4)3)
- •6.Электролиз расплавов и растворов солей. Катодные и анодные процессы. Законы Фарадея.
- •Электролиз расплавов
- •Электролиз водных растворов
- •Законы электролиза
- •Выход по току
- •Координационная теория Вернера (1893 г.)
- •Номенклатура комплексных соединений
- •8. Строение атома. Квантовые числа. Принципы наименьшей энергии. Правило Клечковского, принцип Паули, правило Хунда. Составление электронных формул.
- •Строение атома по Бору (1913):
- •9.Периодический закон и система д.И. Менделеева
- •Структуры периодической системы:
- •Периодическая система и электронная структура атома
- •10. Типы химической связи (ковалентная , ионная, металлическая, водородная)
- •11. Химия элементов и их соединений I группа пс. Водород: особенности электронной структуры, изотопы. Получение и применение водорода и щелочных металлов. Получение и применение меди, серебра, золота.
- •Водород
- •Получение
- •Химические свойства водорода
- •Применение
- •Щелочные металлы
- •Медь, серебро и золото
- •Способы получения металлов d-элементов I группы:
- •Применение
- •12. II группа пс. Амфотерность бериллия и его соединений. Общая характеристика подгруппы d- элементов.
- •Соединения Ве и Mg
- •Щелочноземельные металлы
- •Цинк, кадмий и ртуть
- •13. Жесткость воды и способы ее устранения.
- •16. V группа пс. Особенности химической связи в молекуле азота. Важнейшие соединения азота (аммиак, оксиды азота, азотная и азотистая кислота и их соли). Взаимодействие азотистой кислоты с Ме и неМе.
- •17. Элементы 6 группы пс. Кислород: оксиды, пероксиды. Строение и свойства озона. Сера: оксиды, кислоты, соединения серы с Ме и неМе.
- •18. Свойства серной кислоты. Особенности взаимодействия разбавленной и концентрированной серной кислоты с Ме и неМе.
- •20. Элементы VII группы пс. Химические свойства галогенов: степени окисления, галогенводороды, соединения с кислородом, кислоты, содержащие хлор и их соли.
- •22. VIII группа пс. Подгруппа d- элементов: триоды элементов и их химические свойства. Оксиды, гидроксиды и комплексные соединения этих элементов.
Теории растворов
Физическая теория растворов (Вант – Гофф, Аррениус – ученые внесшие вклад в развитие) рассматривала, растворитель, как инертную среду и приравнивала растворы к простым механическим смесям.
Недостатки теории: а) не объясняла энергетический эффект растворителя; б) не объясняла изменения объема в процессе растворения; в) не объясняла изменение окраски в процессе растворения
Химическая теория растворов (Д.И.Менделеев) Растворы рассматривались, как химические соединения. Однако, в растворах нет строгого соотношения между веществом и растворителем, т.е. растворы не подчиняются закону постоянства состава. Кроме того в свойствах растворов можно обнаружить многие свойства, его отдельных компонентов, чего не наблюдается в случае химического соединения.
Физико-химическая теория растворов (Каблуков) С этой точки зрения растворы занимают промежуточное положение, между механическими смесями и химического соединения.
Процесс растворения тесно связан с диффузией, под влияние растворителя от поверхности твердого вещества, постепенно отрываются молекулы или ионы и в растворе диффузий распределяются по всему объему растворителя. С поверхности затем снимается новый слой молекул и т.д. Перешедшие в растворе ионы остаются связанными с молекулами воды и образуют гидраты ионов. В общем случае любого растворителя эти соединения называют сольватами ионов. Одновременно происходит обратный процесс выделения молекул из раствора. Обратный процесс тем больше, чем выше концентрация раствора при динамическом равновесии, сколько молекул растворяются, столько же выделяется из раствора.
5.Гидролиз растворов солей. Степень гидролиза и факторы, влияющие на нее. Типичные случаи гидролиза (показать на примерах).
Взаимодействие ионов соли с водой приводящее к образованию слабого электролита называется гидролизом соли. Различают несколько случаев гидролиза:
Соль сильного основания и слабой кислоты. (CH3COONa, NaCO3, KCN, Na2S)
В водном растворе соль сначала диссоциирует на катионы и анионы
диссоциация:

Анион слабой кислоты взаимодействует с водой, создавая щелочную среду (гидролиз по аниону):
гидролиз:
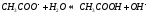
молекулярное
уравнение гидролиза:

Константа диссоциации уравнения гидролиза:
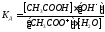
т.к.
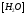 =const,
то КД
[H2O]
=
КГ
(константе гидролиза)
=const,
то КД
[H2O]
=
КГ
(константе гидролиза)
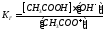
т.к. Кводы = [H+]·[OH-], то [OH-]= Кводы/[H+]
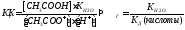
Т.е. чем слабее кислота, тем меньше ее Кд, тем сильнее будет гидролизована соль.
Гидролиз солей многоосновных кислот протекает ступенчато:
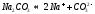
1
ступень:
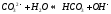
2
ступень:
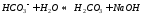
В растворах обычной концентрации гидролиз этой соли идет лишь по первой ступени с образованием кислой соли. В сильно разбавленных растворах гидролиз частично идет по 2 ступени с образованием свободной угольной кислоты. Гидролиз по 2 ступени не значителен, т.к. велика концентрация ионов ОН.
Соль слабого основания и сильной кислоты (nh4no3, ZnCl2, Al2(so4)3)
диссоциация:

Катион слабого основания взаимодействует с водой, создавая кислую среду:
гидролиз:
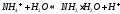
молекулярное
уравнение гидролиза:
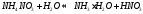
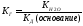
Чем слабее основание, тем сильнее будет гидролизована соль.
Соли многокислотных оснований гидролизуются ступенчато:
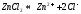
1
ступень: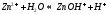
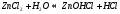
2
ступень:
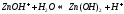
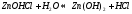
В обычных условиях гидролиз этой соли идет только по первой ступени.
Соль слабой кислоты и слабого основания (CH3COONH4, Al2S3, (NH4)2CO3)
В данном случае гидролизу подвергается и катион, и анион соли (гидролиз по катиону и аниону)
Диссоциация:
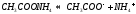
Гидролиз:
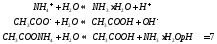
Среда гидролиза определяется тем ионом соли, у которого степень гидролиза выше (кислая, щелочная, нейтральная)
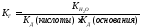
Соли сильного основания и сильной кислоты (NaOH, CaCl2, NaNO3)
Эти соли при растворении в воде не гидролизуются, их растворы имеют нейтральную реакцию.
Полный (совмещенный) гидролиз
Протекает при сливании 2х растворов разных солей, причем одна из солей гидролизована по катиону, а другая по аниону, при этом образуется слабая кислота и слабое основание.
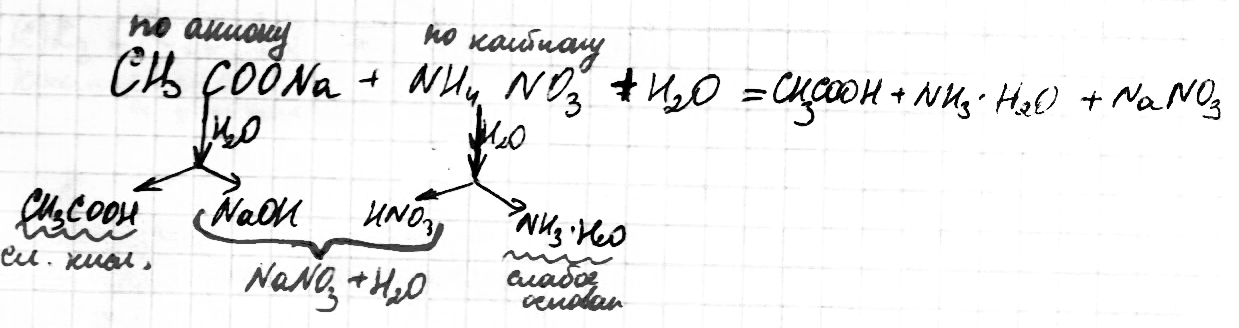
Степень гидролиза
Под степенью гидролиза подразумевается отношение части соли, подвергающейся гидролизу, к общей концентрации её ионов в растворе.
Степень гидролиза соли тем выше, чем слабее кислота или основание, её образующие.
h связано с КГ уравнением аналогичным закону разбавления Оствальда
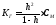
Чаще всего гидролизованная часть соли очень мала и концентрация продуктов гидролиза не значительна, тогда h<1, а 1-h≈1
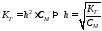
т.е. при разбавлении раствора соли степень ее гидролиза возрастает.
Кроме разбавления раствора усилить гидролиз можно нагреванием раствора, а также добавлением специальных реагентов.
